Contents
Tami H Skoff、Amy E Blain、James Watt、Karen Scherzinger、Melissa McMahon、Shelley M Zansky、Kathy Kudish、Paul R Cieslak、Melissa Lewis、Nong Shang……显示更多
摘要
1 岁以下婴儿是百日咳相关疾病和死亡的高危人群。2012 年,建议孕妇在每次怀孕期间接种 Tdap(破伤风类毒素、减量白喉类毒素和无细胞百日咳疫苗),以保护婴儿出生后的头几个月;但目前关于该策略有效性的数据有限。
我们对 2011 年 1 月 1 日至 2014 年 12 月 31 日期间,来自美国新发感染项目网络(Eerging Infection Program Network)6 个州的、出现咳嗽症状的 2 个月以下婴儿百日咳病例进行了一项病例对照研究。对照组病例与病例组病例在医院进行匹配,并根据出生证明进行选择。我们对母亲进行了访谈,以收集人口统计学信息、家庭特征和医疗保健提供者信息。我们获得了母亲和婴儿的经医疗保健提供者核实的免疫接种史。如果母亲在分娩前≥14 天接种了 Tdap 疫苗,则认为其在孕期已接种疫苗;孕期阶段的计算依据为 Tdap 疫苗接种日期、婴儿出生日期和胎龄。我们使用多变量条件 logistic 回归计算了比值比(OR);疫苗有效性(VE)估计为(1 – 比值比)× 100%。
共纳入 240 例病例和 535 例对照;17 例(7.1%)病例组母亲和 90 例(16.8%)对照组母亲在妊娠晚期接种了百白破疫苗。妊娠晚期接种百白破疫苗的多变量疫苗有效性估计值为 77.7%(95%置信区间[CI],48.3%–90.4%);与住院病例相比,疫苗有效性提高至 90.5%(95% CI,65.2%–97.4%)。
孕期接种疫苗是保护婴儿出生后最初几个月免受感染的有效方法。鉴于百日咳疫情持续反弹,应重点提高孕妇接种 Tdap 疫苗的率。
尽管疫苗对降低美国百日咳杆菌的感染负担产生了显著影响,但百日咳仍然流行,自 20 世纪 80 年代末以来,报告病例数持续上升。2012 年,美国报告了 48000 例百日咳病例,是自 20 世纪 50 年代中期以来的最高数字。虽然病例增加的原因可能是多方面的,但无细胞百日咳疫苗接种后免疫力的减弱已被证实是其中一个重要因素[ 1 ]。
婴儿是百日咳相关并发症和死亡的高危人群,尤其是在出生后的头几个月[ 1 ]。儿童百日咳疫苗(白喉类毒素、破伤风类毒素和无细胞百日咳疫苗)的 5 剂次接种从 2 月龄开始,这使得婴幼儿极易感染百日咳。在 2-2 月龄的病例中,约 75%需要住院治疗,死亡率约为 1%[ 2 ]。研究表明,父母和兄弟姐妹在将百日咳传播给易感婴儿的过程中起着重要作用[ 3,4 ]。
2005 年,两种破伤风类毒素、减量白喉类毒素和无细胞百日咳联合疫苗(Tdap)获准在美国青少年和成人中作为单剂加强针使用[ 5 , 6 ]。尽管 Tdap 免疫接种的主要目标是为接种者提供直接保护,但相关建议也侧重于通过为密切接触者接种疫苗来间接保护婴儿,这种策略被称为“茧式保护”[ 5 , 6 ]。2011 年,免疫实践咨询委员会(ACIP)建议在单次妊娠期间为妇女接种 Tdap 疫苗,以此作为通过胎盘转移母体抗体来保护婴儿的策略[ 7 ]。由于母体抗体持续时间短,可能不足以保护后续妊娠的婴儿,因此该建议在 2012 年扩大到每次妊娠期间都接种一剂 Tdap 疫苗[ 8 , 9 ]。由于建议在孕期接种疫苗的数据有限,因此实施后的评估对于监测该策略的有效性和长期成功至关重要。
我们进行了一项多州病例对照评估,以确定孕妇在怀孕期间接种 Tdap 疫苗对预防美国 2 个月以下婴儿百日咳的有效性。
方法
百日咳病例定义为:2011 年 1 月 1 日至 2014 年 12 月 31 日期间,年龄≥3-2 个月的婴儿出现咳嗽症状,并符合以下至少一项:实验室确诊(培养或聚合酶链反应)百日咳、与实验室确诊病例存在流行病学关联,或临床表现符合百日咳(咳嗽≥2 周,伴有阵发性咳嗽、吸气性鸡鸣或咳嗽后呕吐)。病例通过 6 个新发传染病项目网络(Emerging Infection Program Network)站点的监测发现[ 10 ]。新发传染病项目网络是由美国疾病控制与预防中心(CDC)与州和地方卫生部门、学术机构和实验室合作建立的网络,旨在为新发传染病的监测、预防和控制提供国家资源。这项病例对照评估在加利福尼亚州、康涅狄格州、明尼苏达州和新墨西哥州全州范围内进行,并在纽约州(奥尔巴尼县、阿勒格尼县、卡特罗格斯县、肖托夸县、切芒县、克林顿县、哥伦比亚县、特拉华县、伊利县、埃塞克斯县、富兰克林县、富尔顿县、杰纳西县、格林县、汉密尔顿县、利文斯顿县、蒙哥马利县、门罗县、尼亚加拉县、安大略县、奥尔良县、奥齐戈县、伦斯勒县、萨拉托加县、斯克内克塔迪县、斯科哈里县、斯凯勒县、塞内卡县、斯托本县、沃伦县、华盛顿县、韦恩县、怀俄明县和耶茨县)和俄勒冈州(克拉克马斯县、穆尔特诺马县和华盛顿县)的部分县进行。如果婴儿在咳嗽发作当天至少出生 2 天,居住在服务区域内,出生在居住州的医院,出生时妊娠期 ≥37 周,未被收养或寄养,且不住在寄宿护理机构,则符合入组条件。 对于每例入组的病例婴儿,我们尝试从与该病例婴儿在同一家医院出生的婴儿的出生证明中招募3名对照婴儿,这些对照婴儿在病例婴儿咳嗽发作日期时年龄均在3个月至2个月之间;一旦所有符合这些标准的潜在对照婴儿都被招募完毕,该病例婴儿的对照招募即告结束。对照婴儿的入选标准与病例婴儿相同,此外,如果对照婴儿在相应病例婴儿咳嗽发作日期之前已被诊断为百日咳,则该对照婴儿也被视为不符合入选条件。
研究人员通过电话采访了病例组和对照组婴儿的母亲,收集了人口统计学信息、母婴医疗保健提供者信息以及婴儿的家庭接触信息。病例组婴儿及其匹配对照组的参考期定义为病例组婴儿咳嗽发作日期前30天。用于比较已登记和未登记的百日咳患儿的数据来自监测病例报告表、母亲访谈和出生证明记录;监测病例报告表数据(包括住院情况)是通过对患者和医生的访谈收集的。
所有入组的病例组和对照组婴儿及其母亲的百日咳疫苗接种情况,包括品牌、生产商和批号,均通过医疗机构或州免疫登记处收集。如果登记处没有完整的疫苗接种史,则联系访谈中确定的所有医疗机构。此外,还联系了分娩医院,以获取病例组和对照组母亲的 Tdap 疫苗接种史。如果病例组婴儿咳嗽发作日期前至少 2 周接种了 Tdap 疫苗,则认为该剂次有效;对于对照组婴儿,则使用与其匹配的病例组婴儿的咳嗽发作日期。当所有医疗机构均已完成随访时,则认为母亲的疫苗接种史完整;如果与医疗机构的随访不完整,但至少确定了一剂有效的 Tdap 疫苗,则将这些个体纳入分析。如果联系了所有医疗机构但均未提供 Tdap 疫苗接种记录,且在免疫登记处也未找到 Tdap 疫苗接种记录,则认为母亲未接种疫苗。当确认接种过 Tdap 疫苗后,分析中纳入了最近一次有效接种的剂量。如果母亲在怀有病例或对照婴儿之前的任何时间接种过 Tdap 疫苗,则归类为孕前接种;如果母亲在分娩前≥14 天接种过 Tdap 疫苗,则归类为孕期接种;如果母亲在病例或对照婴儿出生后 2 个月内或分娩前 14 天内接种过 Tdap 疫苗,则归类为产后接种。Tdap 疫苗接种的孕期根据接种日期、婴儿出生日期和婴儿出生时的胎龄计算得出。如果可以获得批号,则与疫苗生产商核实以确认疫苗类型和品牌。 当母亲访谈、婴儿和母亲疫苗接种史全部完成后,该婴儿即被视为已入组。
数据分析采用 SAS 9.3 版软件。优势比采用多变量条件逻辑回归计算;疫苗有效性 (VE) 估计为 (1 – 优势比) × 100%。在双变量分析中与母亲接种百白破疫苗相关的变量( P < 0.05)被纳入多变量模型;经向后逐步回归法剔除后,在多变量分析中仍具有显著性的变量被纳入最终模型。尽管婴儿年龄(周)不显著,但由于病例组和对照组的年龄不匹配,我们仍将其保留在最终模型中。未接种疫苗的病例组和对照组母亲被用作参考组。比例差异采用 Pearson 卡 方检验或 Fisher 精确检验进行检验;中位数差异采用 Wilcoxon 秩和检验进行评估。
结果
共识别出 788 名 3 个月至 2 个月大的百日咳患儿;其中,29 名(3.7%)为早产儿,6 名(0.76%)为被收养或寄养儿童,5 名(0.63%)出生于居住州以外的医院,3 名(0.38%)未在医院出生。在 745 名符合入组条件的婴儿中,251 名(33.7%)入组。其余 494 名(66.3%)未入组的原因如下:354 名(71.7%)的母亲无法联系,100 名(20.2%)不同意参与,31 名(6.3%)母亲疫苗接种史随访不完整,7 名(1.4%)不会说英语或西班牙语,2 名(0.4%)因其他原因未入组。与未登记的百日咳婴儿相比,登记婴儿的母亲更有可能接受过高中后教育;在性别、种族、民族、住院、结果或保险类型方面未观察到显著差异( 表 1 )。
| 特征 | 入组人数(%)(n = 251) | 未登记人数(%)(n = 537) | 值 P |
|---|---|---|---|
| 性别 a ,男性 | 123 (49.0) | 258 (49.3) | .99 |
| 种族 b | .07 | ||
| 白色的 | 199 (80.9) | 356 (77.5) | |
| 黑色的 | 22 (8.9) | 30 (6.5) | |
| 其他 | 25 (10.2) | 73 (15.9) | |
| 西班牙裔 | 156 (62.2) | 297 (60.0) | .57 |
| 住院 | 164 (66.1) | 305 (67.6) | .69 |
| 死亡 | 0 | 7 (1.3) | … |
| 状态 | .0001 | ||
| 加利福尼亚州 | 172 (68.5) | 418 (77.8) | |
| 康涅狄格州 | 14 (5.6) | 9 (1.7) | |
| 明尼苏达州 | 19 (7.6) | 30 (5.6) | |
| 新墨西哥州 | 22 (8.7) | 17 (3.2) | |
| 纽约 | 12 (4.8) | 42 (7.8) | |
| 俄勒冈州 | 12 (4.8) | 21 (3.9) | |
| 病例分类 | .31 | ||
| 实验室确认 | 235 (93.6) | 492 (91.6) | |
| 流行病学关联 | 1 (0.4) | 9 (1.7) | |
| 临床相容性 | 15 (6.0) | 35 (6.5) | |
| 保险类型f | .05 | ||
| 医疗补助或无保险 | 131 (59.8) | 299 (67.5) | |
| 私人、自费或其他 | 88 (40.2) | 144 (32.5) | |
| 母亲教育 g | .001 | ||
| 高中或以下学历 | 120 (53.6) | 295 (66.6) | |
| 高中以上 | 104 (46.4) | 148 (33.4) |
a 根据已知性别者计算得出(n = 251 名已登记;n = 523 名未登记)。
b 根据已知种族的人群计算得出(n = 246 名已登记人员;n = 459 名未登记人员)。
c 根据已知种族的人群计算得出(n = 251 名已登记人员;n = 495 名未登记人员)。
d 根据已知住院状态的人员计算得出(n = 248 名已登记人员;n = 451 名未登记人员)。
e 根据已知病例分类的病例计算得出(n = 251 名已登记病例;n = 536 名未登记病例)。
f根据已知保险类型的人计算得出(n = 219 已参保;n = 443 未参保)。
g 根据已知母亲受教育程度的人群计算得出(n = 224 名已入学;n = 443 名未入学)。
我们确定了 5507 名符合纳入对照组条件的婴儿,其中 682 名(12.4%)被纳入评估。其余 4825 名婴儿未纳入研究的原因如下:4124 名(85.5%)婴儿的母亲无法联系,623 名(12.9%)婴儿不同意参与研究,53 名(1.1%)婴儿的母亲疫苗接种史随访不完整,6 名(0.1%)婴儿在相应病例婴儿咳嗽发作日期居住在研究区域之外,4 名(0.1%)婴儿不会说英语或西班牙语,15 名(0.3%)婴儿因其他原因未纳入研究。纳入研究的病例组和对照组婴儿的人口统计学特征见表 2 。由于在 3-2 周龄的婴儿中,对照组婴儿的入组人数与病例组婴儿的入组人数不成比例,我们将分析范围限定于咳嗽发作日年龄≥2 周的病例组婴儿,以及与其对应病例组婴儿咳嗽发作日年龄≥2 周的对照组婴儿( 表 2 );11 例(4.4%)病例组婴儿和 147 例(21.6%)对照组婴儿被排除在外。最终纳入分析的婴儿共 240 例病例组婴儿和 535 例对照组婴儿。
| 特征 | 病例数(%)(n = 251) | 对照组,数量(%)(n = 682) | 值 P |
|---|---|---|---|
| 性别,男性 | 123 (49.0) | 330 (48.4) | .87 |
| 赛跑 | |||
| 白色的 | 199 (80.9) | 543 (81.9) | .62 |
| 黑色的 | 22 (8.9) | 47 (7.1) | |
| 其他 | 25 (10.2) | 73 (11.0) | |
| 西班牙裔 | 156 (62.2) | 344 (50.4) | .002 |
| 年龄,第 b 周 | |||
| 0–1 | 11 (4.4) | 147 (21.6) | <.0001 |
| 2-3 | 66 (26.3) | 147 (21.6) | |
| 4-5 | 70 (27.9) | 153 (22.4) | |
| 6-7 | 79 (31.5) | 178 (26.1) | |
| 8 | 25 (9.9) | 57 (8.3) | |
| 接种过 DTaP 疫苗的婴儿 | 2 (0.8) | 3 (0.4) | .62 |
缩写:DTaP,白喉类毒素、破伤风类毒素和无细胞百日咳疫苗。
a 根据已知种族的婴儿计算得出(病例组婴儿 n = 246;对照组婴儿 n = 663)。
b 咳嗽发作时的年龄(对于病例婴儿)或匹配病例婴儿咳嗽发作时的年龄(对于对照婴儿)。
总体而言,136 例(56.7%)病例组母亲和 358 例(66.9%)对照组母亲至少接种过 1 剂有效的百白破疫苗。136 例接种过疫苗的病例组母亲中有 18 例(13.2%)报告接种过 1 剂有效的百白破疫苗,358 例接种过疫苗的对照组母亲中有 50 例(14.0%)报告接种过 1 剂有效的百白破疫苗( P = 0.83);61 例母亲有 2 剂有记录的百白破疫苗接种记录,7 例母亲有 3 剂。在 61 例接种过 2 剂百白破疫苗的女性中,两剂之间的中位接种时间为 1022 天(范围:7-2744 天),病例组和对照组母亲之间的接种间隔时间无显著差异( P = 0.32)。
图 1A–C 显示了最终模型中包含的 Tdap 剂量分布及其与妊娠相关的给药时间。在妊娠期间接种的 Tdap 剂量(与 22 例病例和 117 例对照相关)中,约 77% 是在妊娠晚期接种的,其中大部分是在 ACIP 推荐的妊娠 27–36 周期间接种的( 图 1A )。在妊娠前接种的 24 例病例相关剂量和 67 例对照相关剂量中,6 例(25.0%)病例母亲和 46 例(68.7%)对照母亲在妊娠前 ≤2 年接种了 Tdap( 图 1B )。对于归类为产后接种的剂量,75.9% 的对照相关剂量和 74.4% 的病例相关剂量是在分娩后最初 2 天内接种的;病例组母亲中有 5 剂(5.6%),对照组母亲中有 7 剂(4.0%)是在妊娠的最后 2 周内接受的,因此被归类为产后( 图 1C )。
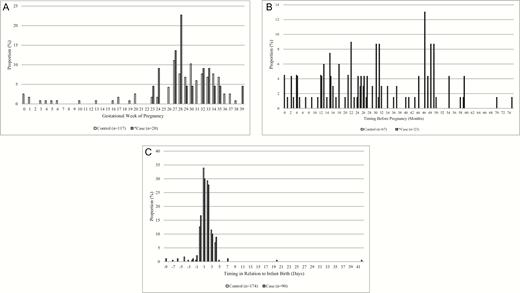
A,破伤风类毒素、减量白喉类毒素和无细胞百日咳联合疫苗(Tdap)的接种时间,按孕期分类。白色条形图代表对照组母亲在孕期接种的 Tdap 疫苗剂量,灰色条形图代表病例组母亲在孕期接种的 Tdap 疫苗剂量。两例病例缺失孕周信息,因此无法计算 Tdap 疫苗接种的确切周数;根据出生日期和 Tdap 疫苗接种日期,这两例病例在分析模型中均被纳入孕中期。B,Tdap 疫苗的接种时间,按孕前分类。白色条形图代表对照组母亲在孕前接种的 Tdap 疫苗剂量,灰色条形图代表病例组母亲在孕前接种的 Tdap 疫苗剂量。一例病例缺失孕周信息,因此无法计算孕前 Tdap 疫苗接种的确切月份;根据出生日期和 Tdap 疫苗接种日期,该病例在分析模型中被纳入≤2 岁组。 C,Tdap 疫苗接种时间(归类为产后)。白色条形图代表对照组母亲在产后接种的 Tdap 疫苗剂量,灰色条形图代表病例组母亲在产后接种的 Tdap 疫苗剂量。
在妊娠晚期任何时间接种疫苗的总体有效率是 77.7%(95%置信区间[CI],48.3%–90.4%; 表 3 );在妊娠早期或中期接种 Tdap 疫苗的有效率为 64.3%(95% CI,-13.8%至 88.8%),但其置信区间与妊娠晚期的置信区间存在重叠。当将妊娠晚期的接种剂量限制在推荐的 27-36 周窗口期时,疫苗有效率(VE)为 78.4%(95% CI,49.8%–90.7%)。在产后给母亲接种 Tdap 疫苗则无有效性(4.9%;95% CI,-49.3%至 39.5%; 表 3 )。
| 疫苗接种情况 | 病例数(%) | 对照组,数量(%) | 多变量 VE a ,%(95% CI) | ||
|---|---|---|---|---|---|
| 全部的 | 240 | (%) | 535 | (%) | |
| 未接种疫苗 | 104 | (43.3) | 177 | (33.1) | 参考 |
| 怀孕前 | 24 | (10.0) | 67 | (12.5) | 50.8 (2.1–75.2) |
| 妊娠早期或中期 | 5 | (2.1) | 27 | (5.1) | 64.3(-13.8 至 88.8) |
| 妊娠晚期 | 17 | (7.1) | 90 | (16.8) | 77.7 (48.3–90.4) |
| 怀孕后 | 90 | (37.5) | 174 | (32.5) | 4.9(-49.3 至 39.5) |
缩写:CI,置信区间;VE,疫苗有效性。
最终模型中包含以下变量:家庭规模(3E2 人)、母亲教育程度、家庭成员百日咳诊断情况和婴儿年龄(周)。
孕前任何时间接种的 Tdap 疫苗预防婴儿百日咳的有效率为 50.8%(95% CI,2.1%–75.2%)( 表 3 )。我们进一步按孕前≤2 年和孕前 3%至 2 年接种 Tdap 疫苗的剂量进行分层分析;孕前 3%至 2 年接种 Tdap 疫苗的有效率为-25.6%(95% CI,-207.4%至 48.7%),孕前≤2 年接种 Tdap 疫苗的有效率为 83.0%(95% CI,49.6%–94.3%)。孕前≤2 年接种 Tdap 疫苗的有效率点估计值与孕晚期接种 Tdap 疫苗的有效率点估计值无显著差异( P = 0.6034)。
约 65.4%(157/240)的病例婴儿在百日咳感染期间住院治疗。当我们评估 Tdap 疫苗预防婴儿百日咳住院的有效性时,发现妊娠晚期接种疫苗的疫苗有效率点估计值提高至 90.5%(95% CI,65.2%–97.4%)。在孕前、孕早期或孕中期以及产后接种疫苗的疫苗有效率点估计值也有所提高;然而,产后接种疫苗的疫苗有效率点估计值仍无统计学意义( 表 4 )
表4。母体接种 Tdap 疫苗预防婴儿百日咳住院的有效性,按接种时间划分
| 疫苗接种情况 | 病例数(%) | 对照组,数量(%) | 多变量 VE a ,%(95% CI) | ||
|---|---|---|---|---|---|
| 全部的 | 157 | (%) | 336 | (%) | |
| 未接种疫苗 | 76 | (48.4) | 109 | (32.4) | 参考 |
| 怀孕前 | 16 | (10.2) | 46 | (13.7) | 76.2 (37.2–91.0) |
| 妊娠早期或中期 | 2 | (1.3) | 20 | (6.0) | 91.4 (24.8–99.0) |
| 妊娠晚期 | 6 | (3.8) | 47 | (14.0) | 90.5 (65.2–97.4) |
| 怀孕后 | 57 | (36.3) | 114 | (33.9) | 32.5(-23.5 至 63.1) |
缩写:CI,置信区间;VE,疫苗有效性。
最终模型中包含以下变量:家庭规模(3E2 人)、母亲教育程度、家庭成员百日咳诊断情况和婴儿年龄(周)。
在 136 例接种疫苗的病例组母亲中,共有 43 例(31.6%)接种了 Boostrix 疫苗;在 358 例接种疫苗的对照组母亲中,共有 102 例(28.5%)接种了 Boostrix 疫苗;在 136 例接种疫苗的病例组母亲中,共有 76 例(55.9%)接种了 Adacel 疫苗;在 358 例接种疫苗的对照组母亲中,共有 207 例(57.8%)接种了 Adacel 疫苗;其余 17 例(12.5%)接种了 Tdap 疫苗的病例组母亲和 49 例(13.7%)接种了 Tdap 疫苗的对照组母亲的疫苗品牌信息缺失。当我们计算两种疫苗在妊娠晚期预防婴儿疾病的有效性时,点估计值之间无统计学差异( P = 0.85)。
讨论
我们利用来自美国多个州的数据进行的研究结果,进一步证实了孕期接种疫苗的有效性,凸显了其作为预防婴幼儿百日咳的关键策略的重要性。英国率先评估了孕期接种 Tdap 疫苗的效果,结果表明该疫苗在预防婴儿出生后头两个月的百日咳方面具有很高的有效性[ 11 , 12 ]。由于婴儿百日咳发病率和死亡率的突然上升,英国于 2012 年底建议孕妇接种疫苗,并迅速实现了孕妇中较高的 Tdap 疫苗接种率(60%)[ 11 ]。三年后,该疫苗的有效性仍然很高[ 13 ]。与英国的经验相反,美国对该建议的采纳速度要慢得多。近期一项调查报告显示,2015-2016 年流感季期间,美国 48.8%的孕妇接种了百白破疫苗,较 2013-2014 年流感季提高了 21.8%[ 14 ]。尽管疫苗接种率持续上升,但美国各地以及为孕妇提供医疗服务的医护人员之间的疫苗接种率可能存在显著差异。应重点提高孕期百白破疫苗的接种率,以充分发挥该策略的益处。
尽管我们的结果与一项美国队列分析的结果一致,但我们发现孕期疫苗接种的有效性略低于英国(英国采用类似的病例对照方法得出估计值);另一项更新的美国队列研究也发现了更高的疫苗有效性点估计值,但其置信区间较宽,包含了我们估计的有效性[ 11 , 15 , 16 ]。2002 年至 2009 年间,英国报告的百日咳患儿中,90%(3-1 岁)需要住院治疗[ 17 ]。相比之下,美国数据显示,百日咳患儿的住院率为 34%至 69%[ 3 , 6 , 18 , 19 ],且近年来住院率有所下降[ 2 ]。尽管重症疾病的流行病学特征或疑似婴儿病例的住院阈值可能存在实际差异,但这种差异更可能反映了病例确诊实践的差异以及美国监测系统能够捕捉到更多门诊病例的能力[ 10 ]。有趣的是,当我们的模型仅限于住院病例时,观察到了更高的疫苗有效率,与英国的估计值非常接近。在英国的研究中,所有病例均经实验室确诊,这也可能导致更高的疫苗有效率估计值;然而,我们的大多数病例也经实验室确诊(94%),这表明这并不能解释我们较低的估计值。
我们病例中 68%来自加利福尼亚州( 表 1 ),该州近年来百日咳疫情严重,其中西班牙裔婴儿病例比例高于加州出生队列中西班牙裔人口的比例[ 20 ]。因此,我们纳入的病例中有 62%为西班牙裔( 表 1 ),高于美国全国估计值(美国国家传染病监测系统 2011-2014 年未发表数据,已知种族的 3-2 个月龄百日咳病例中西班牙裔占 49%)。虽然已有报道称西班牙裔婴儿百日咳风险增加,但仍需进一步研究以充分了解西班牙裔婴儿风险增加的原因[ 21 ]。令人欣慰的是,在西班牙裔病例比例较高的群体中,孕期接种疫苗非常有效,这进一步凸显了该策略的重要性。
自美国引入 Tdap 疫苗以来,就一直建议采取“茧式隔离”策略;然而,该策略的实施面临着巨大的后勤挑战,导致 Tdap 疫苗接种率低,且婴儿密切接触者的接种覆盖率不足[ 22 , 23 ]。与已发表的对“茧式隔离”策略的评估结果一致,我们的分析结果虽然未达到统计学意义,但点估计值显示,产后给母亲接种一剂 Tdap 疫苗并无益处[ 16 , 24 , 25 ]。近期来自非人灵长类动物的数据表明,与全细胞百日咳疫苗不同,无细胞疫苗可能无法阻止百日咳杆菌的定植和进一步传播[ 26 ]。在美国完全使用无细胞疫苗的时代,接种过疫苗的个体仍可能成为婴儿百日咳的重要传染源,这凸显了“茧式隔离”策略的其他缺陷,并进一步强调了孕期接种疫苗等有效策略的关键作用。
近期研究对孕期接种百白破疫苗的最佳时机提出了质疑,有证据表明,在孕中期或孕晚期早期接种疫苗可能最大程度地提高母体百日咳抗体经胎盘传递给婴儿的效率[ 27-29 ]。虽然人们认为孕 30 周前母体抗体的主动转运量极低,但孕晚期接种疫苗可能会降低对婴儿的保护作用[ 30 ]。由于我们评估中的大多数接种百白破疫苗的母亲都是在推荐的孕晚期接种的,因此我们的样本量不足以检测孕晚期接种剂量与孕早期接种剂量在疫苗有效率方面的显著差异,而且样本量较小也使我们无法评估更短时间段的疫苗效果。我们的分析确实发现,在孕前两年接种一剂百白破疫苗是有益的,其疫苗有效率的点估计值与孕晚期接种剂量的疫苗有效率没有显著差异。虽然我们的样本量不足以检测出点估计值之间的显著差异,但这一发现与其他疫苗有效性研究的结果一致,这些研究表明孕前接种百白破疫苗有益[ 16 , 31 ]。未来的研究不仅应继续评估妊娠晚期前接种百白破疫苗对婴儿免疫反应的影响,还应评估转移抗体与预防临床疾病之间的相关性。
尽管孕期接种 Tdap 疫苗能有效预防婴儿百日咳,但仍存在一些重要问题。有研究记录显示,与接种全细胞百日咳疫苗的人群相比,接种过无细胞百日咳疫苗的青少年群体中,Tdap 疫苗的有效性有所降低[ 32-34 ]。随着接种过无细胞百日咳疫苗的孕妇人数增加,孕期或孕前两年内接种疫苗的有效性是否会降低尚待确定;如果这些女性体内的抗体下降速度更快,那么对于接种过无细胞百日咳疫苗的母亲而言,Tdap 疫苗的接种时间可能就显得更为关键。孕期母体免疫接种也可能减弱婴儿对儿童期 DTaP 系列疫苗的免疫反应。虽然母体循环抗体下降迅速,且这种潜在的干扰预计持续时间较短,但关于这种减弱作用的研究结果尚不一致,其临床意义也尚不明确[ 35-40 ]。持续监测百日咳的流行病学对于发现儿童疾病年龄分布的潜在变化至关重要。
最大限度地保护婴幼儿仍然是重中之重,尤其是在百日咳活动日益频繁的情况下。应重点通过医护人员和患者教育来推广孕妇免疫接种,以提高孕妇接种 Tdap 疫苗的比例( www.cdc.gov/pertussis/pregnant )。虽然我们需要免疫持续时间更长的百日咳疫苗,但新疫苗的问世仍遥遥无期。尽管孕期接种疫苗有助于弥补下一代百日咳疫苗获批上市前的这段空白期,但即使在新疫苗问世后,这种高效的策略仍可能是百日咳预防和控制的重要组成部分。
Hits: 6
- 孕期接种 Tdap 疫苗终止了百日咳发病率二十年的上升趋势
- 母亲接种百日咳疫苗、婴儿免疫接种和百日咳风险
- 孕妇接种百日咳疫苗预防婴儿感染和疾病的有效性:新南威尔士州公共卫生网络病例对照研究
- 美国孕妇破伤风、白喉和无细胞百日咳疫苗接种计划对预防2个月以下婴儿百日咳的影响:一项病例对照评估
- Boostrix 疫苗
- Adacel 疫苗:用途、剂量、副作用
- Adacel TDAP:药品说明书/处方信息/作用机制
- Boostrix:药品说明书/处方信息/作用机制
