Contents
海伦娜·N·艾德,医学博士,公共卫生硕士Corresponding Author;
探讨孕期接种 COVID-19 疫苗与幼儿期各种感染风险之间的关联。
我们开展了一项基于挪威全国登记数据的队列研究,纳入了 2021 年 3 月至 2023 年 12 月期间挪威所有活产婴儿,并随访至 2023 年。我们采用 Cox 回归模型估算了在初级或专科医疗机构确诊的感染的风险比。此外,我们还针对特定感染(包括 COVID-19)进行了单独分析。
在研究期间挪威出生的 146,031 名婴儿中,37,013 名(25%)在孕期接种了新冠疫苗。在孕期接种过疫苗的婴儿中,专科医疗机构登记的任何感染总体风险并无差异(调整后风险比[HR]为 0.99;95%置信区间[CI]为 0.95-1.03)。在接种过疫苗的婴儿中,初级医疗机构登记的任何感染风险略有增加(调整后 HR 为 1.05;95% CI 为 1.03-1.07),但在排除随访结束时仍未接种疫苗的母亲所生的婴儿后,这种风险完全消失。随着时间的推移,后代对 COVID-19 的保护作用逐渐减弱。调整后的住院风险比 (HR) 在前 2 个月为 0.48(95% CI,0.40–0.56),3 至 5 个月为 0.76(95% CI,0.60–0.98),6 至 11 个月为 1.13(95% CI,0.82–1.56),12 个月后为 1.14(95% CI,0.72–1.79)。未观察到除 COVID-19 以外的其他感染住院风险存在显著差异。
孕期接种新冠疫苗可保护婴儿在出生后前6个月免受新冠病毒感染。对其他感染未观察到明显效果。
关于此主题的已知信息:
母亲在怀孕期间接种新冠疫苗的婴儿,在出生后的头几个月内可免受新冠肺炎住院治疗的影响。
这项研究的新发现:
孕期接种新冠疫苗可在婴儿出生后的前 6 个月内预防新冠病毒感染,且对其他感染没有明显影响。
介绍
感染是导致幼儿期发病率和死亡率的重要因素。 17 急性呼吸道感染是就医的主要原因,通常由病毒和细菌混合感染引起。有趣的是,对病毒性疾病的免疫力可能对其他感染也有一定的保护作用。 18 然而,孕期母体高水平的 IgG 可能会饱和抗体的胎盘传递,从而增加对其他传染病的易感性,正如某些慢性感染母亲所生的婴儿所表现出的那样。 6,19 鉴于目前关于孕期接种 COVID-19 疫苗后幼儿健康状况的证据有限,且其对非 COVID-19 感染的影响尚不明确,我们旨在研究孕期接种 COVID-19 疫苗是否与后代幼儿期感染风险相关。次要目标是确定对 COVID-19 的保护持续时间。
方法
该项目已获得挪威区域医学和健康伦理委员会的批准(编号:141135),该委员会豁免了这项基于登记研究的参与者知情同意的要求。该研究遵循了《加强流行病学观察性研究报告指南》(STROBE)。 20
研究设计、人群和数据来源
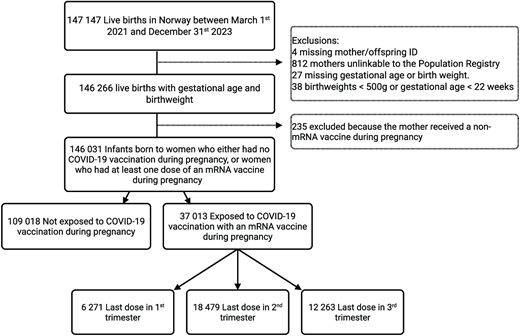
我们开展了一项基于全国登记数据的队列研究,纳入了 2021 年 3 月 1 日(首批孕期接触过母亲新冠疫苗的婴儿出生之日)至 2023 年 12 月 31 日期间挪威所有活产婴儿。我们使用挪威医疗出生登记处(MBRN)确定了研究人群,该登记处包含挪威所有分娩的信息。若婴儿和母亲没有国民身份证号码,则将其排除在外。此外,我们还排除了出生体重缺失、胎龄缺失、出生体重低于 500 克、出生胎龄小于 22 周的婴儿,以及母亲在孕期接种过非 mRNA 新冠疫苗的婴儿,因为挪威的疫苗接种计划已于 2021 年暂停使用病毒载体疫苗( 图 1 )。 21
我们将来自母婴登记网络(MBRN)的信息与以下信息关联起来:挪威免疫登记处的孕妇疫苗接种信息、挪威传染病监测系统中孕期新冠病毒检测阳性记录、孕妇教育程度(义务教育或以下、中学、高等教育不足 4 年、高等教育超过 4 年或缺失)、家庭收入(最低三分之一、中间三分之一、最高三分之一或缺失)、移民和死亡日期(来自挪威统计局)、挪威患者登记处(NPR)的专科医疗服务接触数据以及挪威基层医疗登记处(NRPHC)的基层医疗服务接触数据。 22-25
新冠疫苗接种
我们利用挪威免疫登记处提供的疫苗接种日期和类型信息,来确定婴儿在孕期是否接触过母体接种的 mRNA 新冠病毒疫苗(以下简称“新冠疫苗接种”)。妊娠起始日定义为末次月经(LMP)的第一天,并根据出生日期和孕周(以天为单位)从挪威母婴登记处(MBRN)计算得出。MBRN 中的孕周估计值是根据孕 18 周左右的常规超声检查结果估算的,如果没有超声检查结果,则使用末次月经日期。孕期疫苗接种定义为母亲在末次月经至分娩前一天(末次月经至分娩日-1)期间至少接种过 1 剂新冠疫苗。分娩前 14 天内接种疫苗的妇女所生的婴儿获得的抗体数量较少,但由于母体抗体滴度在先前接种疫苗或感染后可能迅速升高,因此仍将其归类为暴露人群。 26 27 妊娠时期按妊娠期分为:妊娠早期(妊娠第 0 至 97 天)、妊娠中期(妊娠第 98 至 202 天)和妊娠晚期(妊娠第 203 天及以后)。
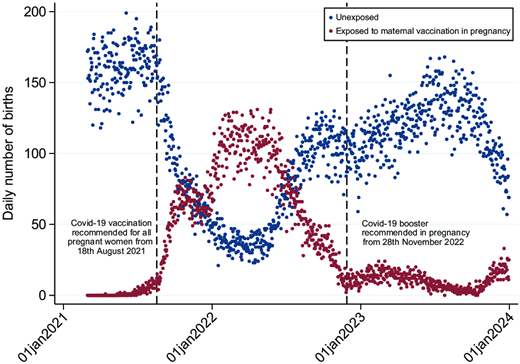
在挪威,存在风险因素的孕妇可在疫苗上市后考虑接种新冠疫苗,而自 2021 年 8 月 18 日起,所有孕妇均被建议接种疫苗。仅推荐孕妇接种 Moderna 和辉瑞-BioNTech 的 mRNA 疫苗。自 2022 年 11 月 28 日起,在整个研究期间,如果孕妇距离上次接种新冠疫苗已超过 20 周,则建议接种加强针。
感染
所有结局均定义为首次因感染诊断代码而与初级或专科医疗保健服务机构接触。在挪威,儿童医生问诊免费,使用私人医疗服务的情况很少见。 28 大多数儿童仅在初级保健机构接受治疗,包括全科医生和与当地急诊科相对应的非工作时间医疗服务。 28-30 挪威公共卫生局 (NRPHC) 提供有关与初级保健机构接触的信息,诊断代码基于国际初级保健分类第二版 (ICPC-2) 编码系统。 25
在挪威,获得专科医疗服务受到严格控制,即使是急性病症也需要医生转诊。 28-32 医院就诊被定义为以医院为基础的门诊或住院专科医疗服务,因为在儿科入院评估后,患者可能被收治入院或出院,并登记为门诊患者。 28,29 挪威患者登记系统(NPR)包含与公共资助的专科医疗服务机构接触的信息,出院诊断代码根据《 国际疾病与相关健康问题统计分类》(第十版) 进行分类。 25
感染可登记为主要诊断或次要诊断。传染病编码被归类为“任何感染”的综合结局,并分别细分为特定感染,包括 COVID-19、上呼吸道或下呼吸道感染、胃肠道感染、泌尿道感染、重症感染(脓毒症、脑膜炎、脑炎或骨髓炎)、围产期感染和病毒感染。有关用于定义结局的诊断编码的完整列表,请参见补充表 1 。
统计分析
我们分别分析了初级和专科医疗机构登记的感染风险,采用 Cox 比例风险回归模型,比较了孕期接种 SARS-CoV-2 疫苗的母亲所生的子女与未接种疫苗的母亲所生的子女,以出生后的天数作为时间尺度。我们还对感染亚组进行了单独分析。所有儿童均从出生开始随访,直至首次接触医疗服务机构(观察预设结局)、死亡、移居或随访结束(2023 年 12 月 31 日)。
为了解释季节性因素导致的人群感染率变化,我们基于出生周进行了分层 Cox 模型分析,从而比较了同一周出生的暴露组和未暴露组后代。在调整后的分析中,母亲年龄、出生国家、胎次、本次妊娠期间是否感染 COVID-19、居住地区、教育程度和家庭收入均作为分类协变量纳入模型。缺失值被视为一个单独的类别。由于兄弟姐妹之间缺乏独立性,共享的家庭层面因素可能造成混淆,因此我们在模型中将母亲 ID 作为聚类变量纳入模型。
鉴于孕期接种疫苗的母亲所生的婴儿出生后对新冠病毒的免疫力预计会逐渐减弱,我们估算了婴儿在出生后 0 至 2 个月(0-90 天)、3 至 5 个月(91-181 天)、6 至 12 个月(182-364 天)以及 12 个月后(365 天及以上)因新冠病毒感染住院的粗略和调整后风险比(HR)。我们计算了每个时间段的 HR,以显示不同时间段的保护差异。我们使用 Wald 检验来检验不同时间段协变量的系数是否存在差异。我们使用 Schoenfeld 残差检验和图形分析来检验比例风险假设。在主要分析中,我们仅在专科医疗机构感染新冠病毒的病例中观察到违反比例风险假设的情况,这反映了母体抗体在出生后预期会减弱;但在按年龄段进行的分析中,未观察到违反比例风险假设的情况。
我们进行了多项分析以评估研究结果的稳健性。由于产次表明是否存在年长的兄弟姐妹,从而可能反映不同的感染风险,而出生年份则可能反映流行毒株、检测方法和疫苗接种率的差异,因此我们将结果按母亲的产次和出生年份进行分层。在敏感性分析中,我们排除了早产儿,因为早产是已知的传染病风险因素。 33 我们还通过排除截至 2023 年底仍未接种 COVID-19 疫苗的母亲所生的婴儿,来研究与就医行为差异相关的潜在偏倚。我们进行了一项敏感性分析,排除了分娩前 14 天内暴露于病毒的婴儿。对于 COVID-19 感染,我们还按暴露的孕期进行了分析。
所有分析均使用 Stata 17 进行。
结果
2020 年 3 月 1 日至 2023 年 12 月 31 日期间,共有 147,147 名婴儿出生,其中 146,031 名儿童纳入分析( 图 1 )。在这些儿童中,37,013 名(25%)在孕期接种过新冠疫苗,其中 6,271 名在孕早期接种了最后一剂疫苗,18,479 名在孕中期接种,12,263 名在孕晚期接种( 图 1 )。研究人群中母亲的基线特征见表 1。 接种过疫苗的儿童更可能出生于年龄超过 30 岁、来自挪威/斯堪的纳维亚半岛、初产且受过高等教育的母亲。他们也更可能出生于 2021 年 9 月至 2022 年 12 月之间,而这一时期主要流行 Omicron 变异株( 图 2 )。未接触儿童的中位随访时间为 464 天(四分位距,219-865),接触儿童的中位随访时间为 627 天(四分位距,530-713)。
| 特征 | 未暴露组(N = 109 918)n (%) | 暴露组(N = 37013)n(%) |
|---|---|---|
| 怀孕开始时母亲的年龄 | ||
| 20岁以下 | 972 (0.9) | 165 (0.4) |
| 20-24岁 | 10 754 (9.9) | 2550 (6.9) |
| 25-29岁 | 36 391 (33.4) | 11 430 (30.9) |
| 30-34岁 | 40 811 (37.4) | 15 448 (41.7) |
| 35-39岁 | 16 801 (15.4) | 6391 (17.3) |
| 40岁以上 | 3289 (3.0) | 1029 (2.8) |
| 母亲出生国 | ||
| 斯堪的纳维亚 | 77 908 (71.5) | 31 490 (85.1) |
| 其他欧洲国家 | 12 685 (11.6) | 2061 (5.6) |
| 非洲/中东 | 10 247 (9.4) | 1208 (3.3) |
| 其他/缺失 | 8178 (7.5) | 2254 (6.1) |
| 居住地区 | ||
| 东南 | 63 253 (58.0) | 21 278 (57.5) |
| 西方 | 24 340 (22.3) | 8076 (21.8) |
| 中间 | 11 602 (10.6) | 4879 (13.2) |
| 北 | 9527 (8.7) | 2734 (7.4) |
| 丢失的 | 296 (0.3) | 46 (0.1) |
| 未生育 | 46 013 (42.2) | 16 755 (45.3) |
| 教育 | ||
| 义务教育或更少 | 16 950 (15.5) | 3253 (8.8) |
| 中等教育 | 21 161 (19.4) | 5639 (15.2) |
| 短期高等教育(≤4年) | 42 179 (38.7) | 16 155 (43.6) |
| 长期高等教育(>4 年) | 20 329 (18.6) | 10 739 (29.0) |
| 丢失的 | 8399 (7.7) | 1227 (3.3) |
| 家庭收入 | ||
| 最低三分之一 | 32 617 (29.9) | 8327 (22.5) |
| 中间三分之一 | 46 531 (42.7) | 16 704 (45.1) |
| 最高三分之一 | 25 047 (23.0) | 11 419 (30.9) |
| 丢失的 | 4823 (4.4) | 563 (1.5) |
| 妊娠期新冠病毒感染 | 10 647 (9.8) | 5364 (14.5) |
| 出生时的胎龄 | ||
| 足月(37周后) | 102 413 (93.9) | 34 810 (94.0) |
| 早产儿(32-37周) | 5669 (5.2) | 1966 (5.3) |
| 极早产儿(孕32周前) | 936 (0.9) | 237 (0.6) |
| 出生体重 | ||
| 极低出生体重(<1500克) | 795 (0.7) | 212 (0.6) |
| 低出生体重(1500-2499克) | 3941 (3.6) | 1271 (3.4) |
| 正常出生体重(2500–4499克) | 101 108 (92.7) | 34 489 (93.2) |
| 高出生体重(≥4500克) | 3174 (2.9) | 1041 (2.8) |
缩写:N,总人口规模;n,总人口的子群体。
医院感染接触者
在孕期接种过新冠疫苗的后代中,因任何感染而住院的风险为每 10000 个随访日 2.9 例;而在未接种疫苗的后代中,该风险为每 10000 个随访日 3.1 例。传染病住院情况的时间趋势见补充图 1。 我们观察到,孕期接种过新冠疫苗的儿童与未接种过疫苗的儿童之间,因任何感染而住院的风险无差异(调整后 HR,0.99;95% CI,0.95–1.03)( 表 2 )。正如预期,我们观察到,孕期接种过新冠疫苗的后代,因新冠感染而住院的风险降低(调整后 HR,0.64;95% CI,0.56–0.73)。至于其他类别的感染,我们观察到,根据孕期接种 COVID-19 疫苗的情况,上呼吸道或下呼吸道、胃肠道、泌尿道、严重感染、病毒感染或围产期感染的风险没有差异(调整后的 HR 范围在 0.93 到 1.11 之间)( 表 2 )。我们观察到,母亲接种 COVID-19 疫苗对子女 COVID-19 住院接触的保护作用逐渐减弱,调整后的风险比 (HR) 在 0 至 2 个月龄时为 0.48(95% CI,0.40–0.56),在 3 至 5 个月龄时为 0.76(95% CI,0.60 和 0.98),在 6 至 11 个月龄时为 1.13(95% CI,0.82–1.56),在 12 个月龄后为 1.14(95% CI,0.72–1.79)( 表 3 )。
| 护理级别 | 结果 | 接触 | 受试者人数 | 后续随访时间(天) | 病例数 | 未调整的风险比(95% 置信区间) | 调整后的风险比(95% 置信区间) |
|---|---|---|---|---|---|---|---|
| 与专科医疗保健机构联系 | 任何感染 | 不 | 107 925 | 49 541 016 | 15 232 | 参考 | 参考 |
| 是的 | 36 647 | 19 482 932 | 5743 | 0.97 (0.93–1.01) | 0.99 (0.95–1.03) | ||
| 2019冠状病毒病感染 | 不 | 108 904 | 55 968 428 | 1546 | 参考 | 参考 | |
| 是的 | 36 966 | 21 787 010 | 555 | 0.66 (0.59–0.75) | 0.64 (0.56–0.73) | ||
| 上呼吸道感染 | 不 | 108 903 | 53 582 968 | 7730 | 参考 | 参考 | |
| 是的 | 36 964 | 20 935 786 | 3033 | 1.01 (0.95–1.06) | 1.01 (0.95–1.07) | ||
| 下呼吸道感染 | 不 | 108 906 | 53 922 640 | 5454 | 参考 | 参考 | |
| 是的 | 36 970 | 21 162 150 | 2040 | 1.01 (0.95–1.07) | 1.03 (0.97–1.10) | ||
| 胃肠道感染 | 不 | 108 912 | 56 043 880 | 1285 | 参考 | 参考 | |
| 是的 | 36 974 | 21 870 984 | 547 | 0.97 (0.85–1.11) | 1.11 (0.97–1.28) | ||
| 尿路感染 | 不 | 108 914 | 56 050 912 | 1128 | 参考 | 参考 | |
| 是的 | 36 972 | 21 900 348 | 385 | 0.91 (0.79–1.05) | 0.93 (0.80–1.09) | ||
| 严重感染 | 不 | 108 895 | 56 473 884 | 227 | 参考 | 参考 | |
| 是的 | 36 969 | 22 051 286 | 70 | 1.03 (0.74–1.45) | 0.98 (0.69–1.40) | ||
| 病毒感染(不包括新冠病毒) | 不 | 108 897 | 55 698 168 | 2325 | 参考 | 参考 | |
| 是的 | 36 972 | 21 757 392 | 908 | 0.98 (0.89–1.08) | 0.99 (0.89–1.10) | ||
| 围产期感染 | 不 | 108 048 | 55 941 496 | 337 | 参考 | 参考 | |
| 是的 | 36 684 | 21 843 240 | 104 | 1.00 (0.75–1.33) | 1.04 (0.77–1.39) | ||
| 与基层医疗保健机构的联系 | 任何感染 | 不 | 108 921 | 28 805 816 | 62 900 | 参考 | 参考 |
| 是的 | 36 976 | 11 697 271 | 25 332 | 1.00 (0.98–1.02) | 1.05(1.03–1.07) | ||
| 2019冠状病毒病感染 | 不 | 108 917 | 50 825 936 | 9703 | 参考 | 参考 | |
| 是的 | 36 975 | 20 308 008 | 3183 | 0.99 (0.94–1.05) | 0.96 (0.91–1.01) | ||
| 上呼吸道感染 | 不 | 108 921 | 34 155 672 | 52 882 | 参考 | 参考 | |
| 是的 | 36 976 | 13 959 548 | 21 108 | 0.97 (0.95–0.99) | 1.03 (1.01–1.05) | ||
| 下呼吸道感染 | 不 | 108 917 | 49 890 712 | 16 010 | 参考 | 参考 | |
| 是的 | 36 975 | 19 789 892 | 6553 | 1.04(1.01–1.08) | 1.06 (1.02–1.10) | ||
| 胃肠道感染 | 不 | 108 917 | 52 651 432 | 9893 | 参考 | 参考 | |
| 是的 | 36 975 | 20 757 842 | 3861 | 0.95 (0.91–1.00) | 1.10 (1.05–1.16) | ||
| 尿路感染 | 不 | 108 921 | 56 008 756 | 1559 | 参考 | 参考 | |
| 是的 | 36 976 | 21 909 720 | 533 | 0.95 (0.83–1.08) | 0.98 (0.86–1.13) | ||
| 病毒感染(不包括新冠病毒) | 不 | 108 917 | 52 540 563 | 11 939 | 参考 | 参考 | |
| 是的 | 36 975 | 20 693 414 | 5149 | 1.01 (0.96–1.05) | 1.05 (1.01–1.10) | ||
缩写:HR,风险比。
已根据母亲年龄、教育程度、胎次、出生国家、居住地区、本次妊娠期间登记的 COVID-19 感染情况以及家庭收入进行调整。为考虑疫情感染随时间推移的差异,未调整和调整后的分析均按出生周进行分层。
| 暴露状态 | 婴儿期 | 受试者人数 | 后续随访时间(天) | 病例数 | 未调整的风险比(95% 置信区间) | 调整后的风险比(95% 置信区间) |
|---|---|---|---|---|---|---|
| 未曝光 | 108 904 | 55 968 427 | 1546 | 参考 | 参考 | |
| 孕期接触过母体疫苗 | 0-2个月 | 36 966 | 3 286 997 | 282 | 0.51 (0.43–0.59) | 0.48 (0.40–0.56) |
| 3-5个月 | 35 587 | 3 215 372 | 123 | 0.79 (0.62–1.00) | 0.76 (0.60–0.98) | |
| 6-11个月 | 35 032 | 6 199 640 | 92 | 1.10 (0.81–1.50) | 1.13 (0.82–1.56) | |
| 12个月后 | 32 546 | 9 085 001 | 58 | 1.10 (0.72–1.67) | 1.14 (0.72–1.79) |
缩写:HR,风险比。
已根据母亲年龄、教育程度、胎次、出生国家、居住地区、本次妊娠期间登记的 COVID-19 感染情况以及家庭收入进行调整。为考虑疫情感染随时间推移的差异,未调整和调整后的分析均按出生周进行分层。
初级保健中诊断出的感染
敏感性分析
按胎次和出生年份分层后,总体关联性相似( 补充图 2 和图 3 )。排除早产儿后,也观察到与主要分析相似的结果( 补充表 2 )。在排除截至 2023 年底仍未接种 COVID-19 疫苗的母亲所生子女的分析中,我们观察到专科医疗机构登记的感染与主要分析结果相似,而暴露于 COVID-19 的后代在基层医疗机构登记的感染风险有所降低(任何感染的调整后 HR 为 1.01;95% CI,0.99–1.03),唯一仍然显著的关联是基层医疗机构诊断的胃肠道感染风险略有增加(调整后 HR 为 1.08;95% CI,1.02–1.14)( 补充表 3 )。
各个孕期阶段的结果相似,尽管在孕中期接触 COVID-19 的婴儿在出生后的前 6 个月内受到的保护略好一些( 补充表 6 )。
讨论
在这项基于登记数据的全国性队列研究中,我们观察到,除孕期接种新冠疫苗的儿童感染新冠病毒的风险降低外,其他感染的医院就诊风险并无差异。这种对新冠病毒的保护作用在6个月龄后逐渐减弱。对于在基层医疗机构登记的感染病例,我们观察到孕期接种新冠疫苗的母亲所生子女的感染风险略高。排除随访结束时仍未接种疫苗的母亲后,这种关联性减弱,提示就医行为差异等未测量的混杂因素可能导致了这种关联性的偏差。
目前尚缺乏关于孕期接种新冠疫苗后,除新冠病毒感染外,其他感染风险的研究。孕期接种流感疫苗旨在保护母亲和婴儿,但关于孕妇接种流感疫苗与婴儿全因感染风险的观察性研究结果存在争议。 34 Hviid 等人发现,孕期接种流感疫苗的儿童因上呼吸道感染和胃肠道感染住院的风险较低,而 Maas 等人则发现,因感染相关症状就诊的婴儿比例并无差异。 34-36 我们观察到,接种疫苗的儿童在医院感染非新冠病毒感染的风险方面没有显著差异,但其感染新冠病毒的风险正如预期般降低。我们还发现,在婴儿出生后的前 6 个月内,孕妇接种疫苗对降低婴儿因新冠病毒感染住院风险的保护作用逐渐减弱,这与之前的研究结果一致。 14,37
母体抗体的胎盘转移取决于母体总 IgG 水平、孕周以及胎盘病变的发生情况。 19 IgG 转移始于妊娠中期,并在整个孕期逐渐增加,大部分转移发生在足月前。 19 因此,早产是儿童感染的重要危险因素。 33 在敏感性分析中,当我们将研究人群限定为足月儿时,结果保持不变,这表明两组间孕周的差异并不能解释观察到的结果。
观察性疫苗接种研究容易出现某些偏倚。 38 如果患有基础慢性疾病的女性更可能接种疫苗,而她们的孩子更容易感染,则可能出现适应症混杂;如果更健康的女性(以及她们的家庭,因此生活方式更健康)更可能遵循疫苗接种建议,则可能存在健康接种者偏倚。 38 在我们的研究中,接种疫苗的母亲通常受教育程度和收入更高,这表明存在健康接种者偏倚;她们也更可能患有妊娠期糖尿病,这表明存在适应症混杂。然而,健康接种者偏倚是一种健康使用者偏倚,选择一个积极的、因此更具可比性的对照组可以最大限度地减少这种偏倚。 39 由于到 2023 年,挪威的大多数成年人至少接种过 1 剂 COVID-19 疫苗,因此我们进行了一项分析,排除了在整个研究期间(直至 2023 年底)均未接种 COVID-19 疫苗的女性所生的婴儿( 补充表 3 )。截至 2023 年底,仍有 40 人未接种疫苗,其中大多数人并非出生于挪威,且教育程度和收入数据往往缺失。因此,我们有理由推断,该群体与其他人群的就医行为存在差异。排除该群体后,专科医疗机构的检测结果依然一致,而初级医疗机构登记的感染病例数略有增加,但增幅有所减弱。这可能表明,初级医疗机构感染病例分析中存在因就医行为差异而导致的混淆因素。 初级保健中胃肠道感染的剩余略微增加的估计值可能反映了社会经济因素造成的残余混杂,这些因素既影响孕产妇的就医行为,也影响儿童患胃肠道感染的风险。41 42
这项研究的主要优势在于,它纳入了挪威孕妇接种新冠疫苗期间的所有新生儿,并对其子女的医疗保健使用情况进行了完整的随访,从而最大限度地减少了选择性偏倚。在挪威,儿童新冠疫苗和医疗保健咨询均免费,且所使用的行政健康登记系统均为强制性且数据几乎完整;因此,我们相信研究结果可以推广到其他拥有类似医疗保健系统的群体。我们还进行了敏感性分析,以评估一些潜在的偏倚。尽管如此,虽然专科医疗保健的数据质量普遍较高,且在我们的研究期间,大多数疑似呼吸道感染的儿童都在医院接受了病毒病原学检测,但我们预计初级保健机构进行的病毒感染实验室检测数量较少。 25 43 此外,初级保健机构更频繁地使用非特异性症状代码,这可能会增加对这些结果进行错误分类的风险。 31 44 虽然对密切接触者和轻症或无症状者的常规检测在 2022 年初停止,但基于临床指征的检测仍在继续,医院接触者可能未受到 COVID-19 检测策略变化的影响 。45 我们没有关于影响妊娠期间胎盘转运效率的因素(例如母体 IgG 水平或胎盘病理)的数据,也没有关于母乳喂养或婴儿出生后常规疫苗接种的数据。19 23 46 在挪威,从未建议 12 岁以下的儿童接种 COVID-19 疫苗,而在我们的研究人群中,只有 20 名儿童接种了 COVID-19 疫苗,而且没有一个儿童在 6 个月大之前接种。47
结论
孕期接种新冠疫苗可为新生儿提供保护,使其在出生后的前6个月内免受因新冠病毒感染而住院的侵害,但保护作用会逐渐减弱。对其他感染未观察到明显效果。
Eide 博士构思并设计了本研究,进行了数据分析,解释了数据,撰写了初稿,并对稿件进行了审阅和修改。Magnus 博士构思并设计了本研究,解释了数据,并对稿件进行了审阅和修改。Håberg 博士、Næss 博士和 Stephansson 博士解释了数据,并对稿件进行了审阅和修改。所有作者均已审阅并同意最终提交的稿件,并对本研究的各个方面负责。
Hits: 0
相关文章:
- 根据对“来源不明”的小瓶的研究,声称 COVID-19 mRNA 疫苗含有 DNA 污染物;没有证据表明 COVID-19 mRNA 疫苗可以改变人体的 DNA
- SARS-CoV-2 mRNA 疫苗使肿瘤对免疫检查点阻断敏感
- MNEXSPIKE(新冠疫苗,mRNA)注射混悬液,用于肌肉注射 2025-2026年配方
- 斯派克瓦克斯(新冠疫苗,mRNA)注射混悬液,用于肌肉注射 2025-2026年配方
- COVID-19 mRNA 疫苗与降低全因死亡风险相关
- 一项历时四年的大型研究发现,新冠病毒 mRNA 疫苗接种并未导致死亡人数增加
- COVID-19 mRNA 疫苗训练免疫细胞提供持久保护
- 辉瑞首席执行官:HHS 声称 mRNA 疫苗“隐瞒的安全问题”是“完全不准确的”
- JN.1 更新的 mRNA COVID-19 疫苗的安全性
- 俄罗斯研究人员声称 COVID mRNA 疫苗与癌症有关
- RFK Jr. 正在散布有关 mRNA 疫苗的虚假声明。这就是他错的地方。
- mRNA covid 疫苗:危害的理由是缺失数据
- 2025-2026 年 mRNA 新冠疫苗(6 月龄至 11 岁儿童适用剂型)接种常规医嘱
- 试验:mRNA 流感疫苗比四价疫苗更有效
- 美国疾控中心疫苗委员会暂时放弃停止推荐 mRNA 新冠疫苗的提议
Powered by YARPP.