Contents
- 1 序言
- 2 本 NACI 声明中包含的信息摘要
- 3 介绍
- 4 方法
- 5 流行病学
- 6 产品
- 7 经济学
- 8 道德、一般、可行性和可接受性 (EEFA) 注意事项
- 9 建议
- 10 研究重点
- 11 监控问题
- 12 缩写列表
- 13 致谢
- 14 附录 A:加拿大各省和地区以及国际上接受帕利珠单抗的当前标准
- 15 附录 B:帕利珠单抗的安全性
- 16 附录 C:帕利珠单抗有效性:附加数据表
- 17 脚注
- 18 页面详细信息
Recommended use of palivizumab to reduce complications of respiratory syncytial virus infection in infants
发布时间:2022 年 6 月 1 日
序言
国家免疫咨询委员会 (NACI) 为加拿大公共卫生署 (PHAC) 提供与免疫接种相关的持续和及时的医疗、科学和公共卫生建议。
除了疾病负担和疫苗特性外,PHAC 还扩大了 NACI 的任务范围,包括在制定循证建议时系统考虑计划因素,以促进省级和地区级公共资助疫苗计划的及时决策。
NACI 要系统考虑的其他因素包括:经济、道德、一般、可行性和可接受性。并非所有 NACI 声明都需要对所有程序因素进行深入分析。虽然将使用循证工具对规划因素进行系统考虑,以确定可能影响建议制定决策的不同问题,但仅包括确定为特定于疫苗或疫苗可预防疾病的不同问题。
PHAC 承认本声明中提出的意见和建议基于当前可用的最佳科学知识,并正在分发本文件以供参考。接种疫苗的人也应了解相关产品专论的内容。此处列出的使用建议和其他信息可能与加拿大疫苗制造商的产品专论中列出的内容不同。制造商已寻求疫苗的批准,并仅在按照产品专论使用疫苗时提供其安全性和有效性的证据。NACI 成员和联络成员在 PHAC 的利益冲突政策范围内行事,包括每年申报潜在利益冲突。
本 NACI 声明中包含的信息摘要
下面重点介绍了免疫接种提供者的关键信息。详情请参阅声明的其余部分。
1. 什么
- 呼吸道合胞病毒病
呼吸道合胞病毒 (RSV) 每年在加拿大从深秋到早春暴发呼吸道疾病。它是全世界幼儿下呼吸道疾病的最常见原因。虽然许多感染是简单的感冒,但 2 岁以下的儿童有患毛细支气管炎或肺炎等严重疾病的风险,可能会住院治疗。潜在的健康状况,尤其是早产、慢性肺病和先天性心脏病 (CHD) 会再次导致严重的 RSV 疾病。再感染发生在一生中,因为感染仅产生部分和暂时的免疫力,尽管再感染通常比最初的免疫力轻。
- 帕利珠单抗
目前没有预防 RSV 的疫苗。预防 RSV 疾病的唯一方法是使用单克隆抗体制剂帕利珠单抗 (SynagisTM) 进行临时被动保护。帕利珠单抗 (PVZ) 仅在 2 岁以下有潜在健康状况的儿童中进行了研究。早期研究在不同患者群体中的疗效为 38-78%,进一步的研究(主要是观察性研究)显示效果差异很大,一些研究显示没有益处。PVZ 已在许多国家使用了 2 多年,具有良好的安全记录,非常罕见的过敏反应病例是主要的严重不良事件 (SAE) 它是一种昂贵的产品,对成本效益(或物有所值)的估计范围很广。在各种情况下,估计的增量效率比 (ICER) 从每个质量调整生命年 (ALY) 不到 1,000 美元到每个 QALY 超过 200 万美元不等。在各种高风险群体中,64% 到 100% 的估计值为每个 QALY < 50,000 美元。在极少数情况下,它可能是占主导地位的(即成本更低且更有效)。RSV 疫苗目前正在研究中。
2. 对象
NACI 为公共卫生计划层面的决策提出以下建议:
- PVZ 应提供给胎龄 < 30 周 (wGA) 和 < 6 个月龄的早产儿在 RSV 季节开始时或期间;< 24 个月大的患有慢性早产儿肺病的儿童,在 RSV 季节之前或期间需要持续氧疗;< 12 个月且血流动力学显著的 CHD 婴儿,以及 < wGA 出生时 < 6 个月大的婴儿,生活在偏远的北部因纽特人社区,需要航空运输住院治疗。对于同时患有 CHD 和慢性肺病的儿童,应遵循慢性肺病的建议。
- 对于 30-32 wGA 和 <3 个月大的 RSV 暴露风险高的早产儿,可以考虑使用 PVZ;选定的 <24 个月大,因囊性纤维化或其他病因患有严重慢性肺病,在 RSV 季节之前或期间需要持续氧疗或辅助通气的儿童;<12 个月大的婴儿患有血流动力学显着的慢性心脏病,而不是先天性;等待心脏移植或在 RSV 季节开始后 6 个月内接受过心脏移植的 12-24 个月大的儿童;以及 <24 个月大的严重免疫缺陷儿童。对于生活在偏远因纽特人社区的 <6 个月足月婴儿,足月婴儿 RSV 住院率非常高,以及胎龄< 36 周和 <6 个月大的婴儿,生活在 RSV 住院率高且需要航空运输住院的偏远社区。当控制 NICU 中 RSV 爆发的所有其他措施都失败时,可以考虑 PVZ。
- PVZ 不应提供给 33 wGA 或之后出生的其他方面健康的婴儿;或不符合预防条件的多胞胎兄弟姐妹。不应常规提供给 <24 个月大的囊性纤维化儿童;对于没有其他 PVZ 标准的 <24 个月大的唐氏综合征儿童;或生活在偏远北部因纽特人社区的健康足月婴儿,除非 RSV 的住院率非常高。在没有其他适应症的情况下,它不应用于预防复发性喘息或哮喘。
- 不应给予 PVZ 来预防留在医院的符合条件的儿童发生医院相关的 RSV 感染。当所有其他措施都无法控制新生儿重症监护病房中的 RSV 暴发时,可以考虑该检查。
由于在加拿大,PVZ 不容易购买,因此没有为个人层面的决策提出具体建议。
3. 如何
- PVZ 的剂量为 15 mg/kg,从当地 RSV 季节开始肌内注射。符合条件的住院儿童应在出院时(或在出院前 48-72 小时内接受第一剂,以方便共用小瓶)。第一剂和第二剂之间的间隔应为 21-28 天,后续剂量之间的间隔应为 28-35 天,最多 4 剂。
- 心脏旁路或体外膜肺氧合后应给予额外剂量。在偏远的北部地区,可以考虑额外剂量,那里的 RSV 爆发可能比其他地方的正常情况持续更长时间。
- 如果儿童因 RSV 感染住院,则应在本季节停止 PVZ。
- 如果可行,应安排诊所或预约,以促进小瓶共享,以降低成本。
- PVZ 禁用于已知对 PVZ 或产品的任何成分(人源化单克隆抗体、甘氨酸、组氨酸)有明显超敏反应的个体。中度至重度疾病,伴或不伴发热,是考虑推迟 PVZ 的一个原因,以避免 PVZ 的不利影响叠加在基础疾病上,或错误地将基础疾病的表现识别为 PVZ 的并发症。延迟 PVZ 的决定取决于基础疾病的严重程度和病因。轻微疾病,如普通感冒,伴或不伴发热,都不是使用 PVZ 的禁忌症。
- PVZ 仅包含针对 RSV 的抗体,可以与任何其他活疫苗或灭活疫苗共同给药。
4. 为什么
PVZ 推荐给健康状况使他们更容易患上严重 RSV 疾病的婴幼儿,需要住院治疗,并可能入住重症监护病房和机械通气。
尽管降低了患严重 RSV 疾病的风险,但 PVZ 并不能阻止所有因 RSV 住院。它被认为可以防止 40% 到 80% 的住院治疗,具体取决于年龄和潜在的健康状况。因此,其他预防 RSV 的方法(限制高危儿童与咳嗽和感冒患者接触、适当的手部卫生、防止接触香烟烟雾)很重要。
尽管任何幼儿都可能因 RSV 住院,但大多数不会患上严重疾病。不建议重症风险较低的儿童使用 PVZ,在某些情况下是因为成本,在其他情况下是因为缺乏关于它是否有效的信息。
介绍
呼吸道合胞病毒 (RSV) 是全世界幼儿下呼吸道疾病的最常见原因脚注1 脚注2.
目前,唯一可用于预防严重 RSV 疾病的免疫剂是 PVZ,一种单克隆抗 RSV 抗体。几种活性候选疫苗目前正在婴儿、孕妇和成人中进行临床试验脚注3.本声明不会涉及 RSV 疫苗。
2002 年 6 月,加拿大卫生部批准 PVZ (SynagisTM) 用于预防严重 RSV 疾病高危婴儿由 RSV 引起的严重下呼吸道疾病。2003 年,国家免疫咨询委员会 (NACI) 发布了关于使用 PVZ 或预防 RSV 疾病的建议脚注4.当时,NACI 建议在 RSV 季节对早产儿(小于或等于 32 周胎龄 (wGA),在 RSV 季节开始时实际年龄小于 6 个月、小于 24 个月大患有慢性早产儿肺病 (CLD) 的儿童在过去六个月内需要氧气和/或药物治疗或其他需要氧疗的肺部疾病, 以及 24 个月以下患有血流动力学显着的先天性心脏病 (hsCHD) 的儿童。对于出生时体重低于 35 wGA、在 RSV 季节开始时年龄小于 6 个月且居住在偏远北部社区的儿童,也可以考虑进行 PVZ 预防脚注4.自 2003 年声明以来,加拿大免疫指南 (CIG) 中修改了 NACI 建议,但没有发布新的声明。从 2013 年开始,除了上述建议外,CIG 还指出,PVZ 预防可能有益于 33 至 35 wGA 之间的选定婴儿,这些婴儿在 RSV 季节开始时年龄小于 6 个月,并且可以考虑用于居住在农村或偏远社区的胎龄儿,根据对获得医疗保健的评估(例如, 需要空运到医院设施)和其他已知会增加风险的因素。此外,对于北部偏远社区的所有因纽特儿童,在 RSV 季节开始时年龄小于 6 个月,无论 wGA 如何,都应考虑 PVZ 预防。
自 2003 年 NACI 声明发布以来,包括美国儿科学会 (AAP) 在内的专家委员会在 2009 年和 2014 年发布了一系列更新的 PVZ 指导文件脚注5 脚注6 脚注7和 2015 年的加拿大儿科学会 (CPS)脚注8其中提出的 PVZ 预防建议与 2003 年 NACI 指南明显不同,并强调需要重新评估 NACI 的建议。附录 A 总结了加拿大各省和地区以及其他 10 个北半球国家目前的 PVZ 资格标准,“在加拿大和国际上使用帕利珠单抗的建议”。
本文件的目的是更新之前关于 PVZ 使用的 NACI 建议,同时考虑到有关 RSV 疾病导致的疾病负担的最新数据、PVZ 对有更严重 RSV 疾病风险的婴儿的疗效和有效性以及 PVZ 使用的经济影响。
指导目标:
本咨询委员会声明的目的是审查证据并制定策略指南,以通过施用单克隆抗体来预防严重 RSV 疾病高危儿童感染 RSV 感染的严重后果。
方法
NACI 的推荐开发过程在别处有详细描述脚注9.
简而言之,准备这份 NACI 咨询委员会声明的主要阶段包括:
- 知识综合
- 综合益处和危害的证据体,考虑到综合证据的质量以及在研究中观察到的效果的大小和确定性
- 将证据转化为建议。
有关 NACI 循证方法的更多信息,请参阅:基于证据的免疫建议:NACI 的方法,2009 年 1 月,CCDR。
为了实现本声明的目标,使用标准 NACI 方法进行了三项系统文献综述:
- 高收入国家幼儿的 RSV 疾病负担与加拿大相当
对 2000 年至 2017 年 2 月的文献进行初步检索,检索到 2389 条记录。由于记录数量众多,进一步评估仅限于系统评价,其中 6 篇,评分为 6 至 7 篇(平均),使用评估系统评价的测量工具 (AMSTAR)脚注10,被保留;没有一个评分更高。这些综述包括 1995 年至 2015 年的文献。
对 2014 年至 2018 年 9 月的文献进行第二次检索,共获得 1022 条记录,其中 29 条被保留用于最终质量评估和数据提取。选择开始日期是为了提供从 2014 年 AAP 更改 PVZ 使用建议时开始的数据。两名评价员使用基于观察队列和横断面研究质量评估工具(Quality Assessment Tool for Observational Cohort and Cross-sectional Studies)和预后研究质量(Quality in Prognosis Studies, QUIPS)的修改工具,独立评估了每项研究的偏倚风险(risk of bias, ROB)。对于研究内比较,两位评价员使用推荐评分评估、开发和评价 (GRADE) 的原则独立评估了每个结局(高、中等、低或极低)的证据质量。分歧通过共识解决。Wingert 等人 2021 年的手稿中介绍了该搜索的方法和结果的详细信息脚注11并在本声明的第 III.1 节和第 III.2 节中进行了总结。
使用相同的策略对 2018 年 9 月 1 日至 2020 年 7 月 29 日的文献进行III次检索,确定了另外 699 条记录,其中 14 条保留用于质量评估和数据提取。
由于检索较新的文献没有提供关于需要建议的某些问题的数据,因此对系统评价或 2014-2018 年检索中接受的论文中确定的相关早期参考文献进行了评估。保留 15 项研究进行质量评估。来自这些研究和 2018-2020 年检索的信息在本文件的第 III.1 节和第 III.2 节中提供。
- PVZ 预防对减少婴儿 RSV 相关并发症的有效性
有关方法和结果的详细信息,请参阅即将发布的文件“关于 PVZ 预防对减少婴儿呼吸道合胞病毒相关并发症影响的 NACI 文献综述”。本声明第 IV.2 节总结了数据脚注12.
- PVZ 预防 RSV 的成本效益
有关方法和结果的详细信息,请参阅“呼吸道合胞病毒 (RSV) PVZ 预防的成本效益:系统评价”。本声明的第 V.1 节总结了数据。
除了这些系统综述外,其他文献检索包括:
- 对加拿大各省和地区以及其他北半球国家使用 PVZ 的建议进行环境扫描
- 关于 PVZ 安全性的快速文献综述
- 当需要信息来解决特定问题时,进行非正式文献综述。
(4) 和 (5) 的结果作为附录 A 和 B 添加到本文件中。非正式评价 (6) 的信息和数据在本文件的文本中介绍。
为了制定全面、适当的免疫计划建议,NACI 考虑了许多因素。除了批判性地评估有关疾病负担和疫苗特性(如安全性、有效性、免疫原性和有效性)的证据外,NACI 还使用已发布的同行评审框架和循证工具来确保与道德、一般、可行性和可接受性 (EEFA) 相关的问题得到系统评估并整合到其指南中脚注13.NACI 秘书处应用该框架以及随附的循证工具(道德综合过滤器、一般矩阵、可行性矩阵、可接受性矩阵),以系统地考虑这些规划因素,以便为及时、透明的决策制定清晰、全面、适当的建议。有关 NACI 的 EEFA 框架和循证工具(包括道德综合过滤器、一般矩阵、可行性矩阵和可接受性矩阵)的开发和应用的详细信息,请参阅 https://doi.org/10.1016/j.vaccine.2020.05.051。
对于本声明,NACI 回顾了 RSV 工作组提出的系统文献综述的关键问题。在文献检索和对个别研究的批判性评价之后,提出了 PVZ 使用的建议。RSV 工作组主席和 PHAC 医学专家于 2020 年 2 月 5 日向 NACI 提交了证据并提出了建议。在 2020 年 2 月 5 日、2020 年 9 月 24 日和 2021 年 10 月 22 日的 NACI 会议上对证据进行全面审查和咨询后,委员会对具体建议进行了投票。文中描述了相关考虑因素、具体决策的理由和知识差距。
流行病学
RSV 是一种包膜 RNA 病毒,属于副粘病毒科。根据 G 表面蛋白的差异,有 2 个亚组,这些亚组内有许多基因型。人类是唯一的感染源,传播是通过直接或间接接触含有病毒的呼吸道分泌物而发生的脚注14.
RSV 几乎感染了所有 2 岁以下的婴儿脚注1 脚注2.在需要住院治疗的幼儿中,RSV 最常见的临床表现是毛细支气管炎(一种与呼吸急促、咳嗽和喘息相关的急性下呼吸道感染)和肺炎脚注14 脚注15.原发性感染并不赋予完全的保护性免疫。再感染会终生发生,但通常不太严重,主要表现为年龄较大的儿童和成人的上呼吸道疾病脚注14.
1 < 岁儿童的住院率最高,尤其是在出生后的前 2 个月脚注16.据报道,高收入国家每年每 1000 名儿童的住院率分别为 26.3 (95% CI 22.8, 30.2)、11.3 (95% CI 6.1, 20.9) 和 1.4 (95% CI 0.9, 2.0) 年龄组 0-5 个月、6-11 个月和 12-59 个月脚注2.在加拿大,据报道,6 个月大的儿童每年每 1000 人中有 20 例、10.2 例和 4.8 例< 例脚注15、<1 岁和 1-3 岁脚注17.在安大略省,每年 9% 的 <1 岁儿童住院归因于 RSV脚注17.高收入国家的病死率通常为 <0.5%,患有合并症的婴儿的病死率更高脚注1 脚注18.在一项加拿大研究中,82% 的死亡发生在具有严重 RSV 疾病潜在危险因素的儿童中脚注19.
大多数因 RSV 感染住院的 2 岁以下儿童没有合并症脚注1 脚注17,但早产儿和 CLD 或 CHD 患者的住院率和住院时间更高,重症监护病房收治率更高。脚注1 脚注8 脚注17.患有其他与早产无关的肺部疾病(如囊性纤维化)的儿童脚注20或患有其他慢性病,包括免疫缺陷脚注21 脚注22以及生活在遥远北方土著社区的儿童脚注23患严重 RSV 疾病的风险也可能增加。RSV 越来越被认为是老年人发病和死亡的重要原因脚注24.
在温带气候中,RSV 每年冬天都会引起流行病。在加拿大,RSV 季节通常从 10 月或 11 月开始,一直持续到 4 月或 5 月,大多数病例发生在 12 月至 3 月脚注25.对 RSV 住院率时间趋势的研究显示了相互矛盾的结果,这可能是由于检测政策、所用诊断测试的敏感性和住院标准的差异脚注1.最近的一项美国研究报告称,从 1997 年到 2012 年,所有婴儿以及 CLD 和高危 CHD 婴儿的 RSV 住院率都有所下降,但其他高危婴儿的 RSV 住院率没有降低脚注26.
III.1 特定高危人群的疾病负担
为制定本声明而进行的 RSV 疾病负担系统评价的数据总结并整合到下面的相关部分中。鉴于确定的文章数量少,以及使用的方法和研究结果的异质性,必须谨慎看待对研究结果的解释。此处还介绍了来自早期研究和 2018-2020 年文献综述的信息。
III.1.1 无冠心病或慢性肺病的早产儿
IIII.1.1.1 住院治疗
因 RSV 感染住院的风险随着胎龄的降低而增加。在 2000-2005 年一项针对实验室确诊 RSV 下呼吸道疾病住院的幼儿的前瞻性人群研究中,Hall 等人报告了胎龄为 <<29、29-31、32-34、≥ 35 周和足月婴儿的每 1000 名 24 个月婴儿的 RSV 住院率 (RSVH) 分别为 19.3、18.7、6.3、6.9 和 5.3。在他们的研究中,38% 的婴儿患有其他高危疾病,20% 的婴儿接受了 PVZ脚注16.
关于幼儿 RSV 疾病负担的系统文献综述 (BODsr),仅限于 2014年至 2018年9月的出版物,以及 2020 年更新的综述,没有对 <29 wGA 早产儿 RSV 疾病负担的研究。此处总结了早产儿的研究数据。
在研究水平的比较中,一项中等至低质量证据 (COE) 的研究发现,29-32 wGA 和 33-36 wGA 的婴儿在第一个 RSV 季节的 RSVH 率相似(RR 1.20,95% CI 0.92,1.56)脚注27.另一项同样被评为中度至低 COE 的研究发现,33-36 wGA 的婴儿和 <24 个月的足月婴儿的 RSVH 相对风险为 2.05 (95% CI 1.89, 2.22)脚注28.在一项针对婴儿的研究中,发现 RSVH 的 COE 非常低 <与第一个 RSV 季节的足月婴儿相比为 33 wGA (RR 3.88,95% CI 1.13,13.30)脚注29.
对于 29 至 <33 wGA 的婴儿,RSVH 的单臂合并比例(表 1)分别为 5.1%、2.8%、3.3% 和 4.1脚注27 脚注2932-34 瓦加脚注30、32/33 至 35 wGA脚注27 脚注28 脚注30 脚注31 脚注32 脚注33 脚注34 脚注35和 35 wGA脚注30分别。健康足月婴儿的 RSVH 率为 1.2%。该组的 4 项研究中有 3 项报告了出生后第一年的 RSVH (0.8%-1.5%)脚注29 脚注36 脚注37,一项研究报告了 24 个月大的 RSVH (1.3%)脚注28.
| wGA | % RSVH | 95% CI | 数量研究 | 偏倚风险 |
|---|---|---|---|---|
| 29 – <33脚注27 脚注29 | 5.1 | 4.0, 6.3 | 2 | 低 |
| 32 – 34脚注30 | 2.8 | 1.6, 4.0 | 1 | 高 |
| 32/33 – 35脚注27 脚注28 脚注30 脚注31 脚注32 脚注33 脚注34 脚注35 | 3.3 | 2.7, 4.1 | 8 | 中等 (5), 高 (3) |
| 35脚注30 | 4.1 | 2.8, 5.4 | 1 | 高 |
| 健康术语脚注28 脚注29 脚注36 脚注37 | 1.2 | 1.1, 1.2 | 4 | 低 |
使用合并数据的研究间比较(由于证据的间接性质,均由 GRADE 以极低的 COE 进行评估)显示,早产儿 RSVH 的 RR 与 29-32 至 <33 wGA 婴儿的足月婴儿的 RR 为 4.3(95% CI 3.7,4.8,p=0.000),32-35 wGA 婴儿为 2.8(95% CI 2.5,3.1,p=0.000)。实际风险差异分别为 3.9% (95% CI 2.7, 5.1) 和 2.1% (95% CI 1.4, 2.8)。
2020 年的文献更新确定了两项研究,这些研究报告了其他方面健康的早产儿的 RSVH。在一项评估 nirsevimab(一种抗 RSV 活性的新型单克隆抗体)疗效的多国随机对照试验中,≥29 至 ≤32 wGA 和 > 32 wGA 婴儿在安慰剂给药后 150 天内的 RSVH 发生率分别为 4.3% 和 4.0%(ROB 低)脚注38.在 Papenburg 等人于 2015-2017 年在魁北克进行的一项回顾性队列研究中,33-35 wGA 婴儿在 RSV 季节的 RSVH 率为 3.4%(ROB 中度)脚注39.此外,一项被 AMSTAR 评为平均水平的系统评价报告了 2000 年至 2008 年间进行的 7 项观察性前瞻性研究。其他方面健康的 33-<35 wGA 婴儿的合并 RSVH 率为 3.4% 或 5.5/100 个患者季节脚注40.
对早期文献进行了综述,以获取有关更严重早产儿的数据。在 1996-1997 年 PVZ 随机对照试验的安慰剂组中,婴儿在第一个 RSV 季节的 RSVH 发生率分别为 (% 和 95% CI) 10.0 (2.8, 23.7)、7.7 (3.6, 14.1)、10.1 (5.1, 17.3) 和 8.2 (3.1, 17),胎龄分别为 <29、29-32、32-35 和 33-35 周(ROB 低)脚注41.在 PVZ 之前时代的历史队列研究中,Stevens 等人报告了 26 周、 27-28 岁、≤>28 周和 >30-32 周胎龄 (wGA) 的无 CLD 早产儿 1 岁校正年龄的 RSVH 率分别为 10.2%、8.6%、6.8% 和 4.3%。对于所有 ≤ wGA 为 30 的婴儿,RSVH 率为 8.1%(ROB 中度)脚注42Boyce 等人使用 1989-93 年的田纳西州医疗补助数据,估计 28 岁、29 至 ≤<33 岁和 33 至 <36 wGA 的婴儿在出生后前 6 个月的 RSVH 发生率分别为每 1000 名儿童 93.8、81.8 和 79.8 例,低风险婴儿(没有 CLD 或 CHD 或其他慢性疾病的足月婴儿)每 1000 名儿童 44.1 例。出生后 6 个月的住院率分别为每 1000 名 46.1、50 和 34.5 ≤例,其中 28 岁、29 至 <33 岁和 33 至 36 岁儿童,低风险婴儿(ROB 中度)为 15脚注43.其他观察性研究,ROB 低脚注44或中等脚注45 脚注46 脚注47,报告了 <29、<28、<29 或 ≤30 wGA 出生且无其他合并症的婴儿在出生后第一年的 RSVH 发生率为 10.4%、7.7%、13% 和 13.5%。这些早期早产儿很少或没有接受母体抗体,他们较窄的气道通道增加了他们对 RSV 感染影响的脆弱性。
与健康的足月婴儿相比,29-32 wGA 的婴儿患 RSVH 的风险也增加,但 RSVH 率低于更多早产儿,在第一个 RSV 季节为 5.7% 至 9.9%(ROB 中度)脚注45 脚注46.32 或 33 至 35 wGA 的婴儿报告在其出生后第一年或第一个 RSV 季节的 RSVH 发生率为 2.8% 至 6.5%(ROB 中度)脚注45 脚注48.在 Boyce 等人的研究中,早产儿在出生后 6 个月的 RSVH 发生率与出生后 6 个月的低风险足月儿相似(ROB 中等)脚注43.在另一项研究中,32-34 岁 wGA 早产儿(其中 20% 接受 PVZ)的 RSVH 发生率与 4.2 – 4.5 个月大的 1 个月足月儿相似(ROB 中等)脚注49.
实际年龄是 RSVH 的重要危险因素(ROB 中度)脚注16 脚注43 脚注49总体 RSVH 率在 <3 个月大时最高脚注16.
III.1.1.2 RSVH 的住院时间
根据 BODsr,两项研究提供了住院时间 (LOS) 的研究水平比较。在一项中度至低 COE 中,33-36 wGA 的 <24 个月婴儿与足月婴儿之间的 LOS 平均差异为 1.0 天 (95% CI 0.88, 1.12)脚注28而在另一个 COE 非常低的研究中,29-32 wGA 和 33-35 wGA 的 <12 个月婴儿之间的 LOS 平均差异为 4.0 天 (95% CI 1.54, 6.46)脚注50.
来自合并单臂研究的平均 LOS 为 10 天、 7.7 天、 5.5 天、 4.5 天和 7 天,共 29 至 32 wGA脚注50、29 至 34/35 wGA脚注50 脚注51,33-34 wGA脚注28 脚注50、32/33 至 35 wGA脚注28 脚注30 脚注33和 35 wGA脚注50分别。健康足月婴儿的 LOS 为 3.5 天脚注28 脚注37 脚注52 脚注53.(表 2)
| wGA | 平均 LOS(天) | 95% CI | 数量研究 | 偏倚风险 |
|---|---|---|---|---|
| 29 – 32脚注50 | 10.0 | 7.7,12.3 | 1 | 低 |
| 29-34/35脚注50 脚注51 | 7.7 | 6.1,9.2 | 2 | 低 |
| 33 – 34脚注28 脚注50 | 5.5 | 0.6-10.4 | 2 | 中等、低 |
| 32/33 – 35脚注28 脚注30 脚注33 | 4.5 | 2.3-6.8 | 3 | 中等 (1), 低 (2) |
| 35脚注50 | 7.0 | 4.9-9.1 | 1 | 低 |
| 健康术语脚注28 脚注37 脚注52 脚注53 | 3.5 | 2.3,4.7 | 4 | 高 (1), 中等 (2), 低 (1) |
使用合并数据进行的研究间比较(均以极低的COE)显示,29-32 wGA、32/33-35 wGA和29-35 wGA的早产儿与足月儿之间的LOS平均差异分别为6.5天(95% CI 3.9、9.1、p<0.000)、1.0 天(95% CI -8.6、10.6)和4.2天(95% CI -5.3,13.7)。
2020 年的文献更新确定了 3 项报告了这一结局的研究。29-<36 wGA 婴儿 (ROB 低) 的中位 LOS 为 7.0 天 (范围 2-20)脚注38和 29-34 wGA 婴儿 (ROB 中度) 7.0 天 (IQR 3-12)脚注54.Anderson 等人报道,29-32 wGA、33-34 wGA 和 35 wGA 婴儿的中位 LOS 分别为 6 (IQR 3-11)、5 (IQR 3-10) 和 5 (IQR 3-8) 天 (ROB 低)脚注55.此外,为了进行比较,四项研究报告了健康足月儿的 LOS。中位 LOS 为 4 天 (范围 1-23) (ROB 中度)脚注56和 1.9 天 (IQR 1.1-2.9) (ROB 低)脚注57.平均 (SD) LOS 为 5 (2.2) 天 (ROB 中度)脚注58在 Midulla 等人的一项研究中,不同 RSV 基因型的 5.9 (2.99)、5.4 (2.89) 和 5.84 (3.13) 天(ROB 低)脚注59.
在早期文献中,早产儿的中位住院时间也比足月儿长脚注60.在 2008-9 年的一项前瞻性队列研究中,确诊 RSVH 的 28 至 < 33 wGA 婴儿的平均 LOS 为 7.2 ± 3.3 天(ROB 低)脚注61.
III.1.1.3. 入住 ICU 和机械通气
在 BODsr 中,一项研究着眼于 29-32 岁婴儿与 33-35 wGA 婴儿的 ICU 收治、ICU LOS、机械通气 (MV) 和 MV 持续时间。这些参数中的任何一个都没有显著差异 (低到极低的 COE)脚注50.
对于 29-32 wGA 的婴儿,因 RSV 住院而入住 ICU 的患者的单臂合并比例分别为 51.7 、 19.1 、 31.5 和 13.9脚注50、32-34 wGA脚注30、32-35 wGA脚注30 脚注35 脚注50和 35 wGA脚注30分别。住院健康足月婴儿的 ICU 收治率为 15.8%脚注37 脚注52 脚注53.(表 3)
| wGA | % ICU | 95% CI | 数量研究 | 偏倚风险 |
|---|---|---|---|---|
| 29 – 32脚注50 | 51.7 | 41.3, 62.1 | 1 | 低 |
| 33 – 34脚注30 | 19.1 | 2.3, 35.8 | 1 | 低 |
| 32 – 35脚注30 脚注35 脚注50 | 31.5 | 13.1, 53.6 | 3 | 中等 (2) 低 (1) |
| 35脚注30 | 13.9 | 2.6, 25.2 | 1 | 低 |
| 健康术语脚注37 脚注52 脚注53 | 15.8 | 5.4, 30.0 | 3 | 中等 (2), 高 (1) |
使用汇总数据进行的研究间比较(均处于极低 COE)显示,住院早产儿与足月儿入住 ICU 的 RR 分别为 3.3 (95% CI 1.9, 5.7, p=0.000)、2.0 (95% CI 1.0, 4.0, p=0.000) 和 3.3 (95% CI 1.9, 5.6, p=0.000) 对于 29-32 wGA、32-35 wGA、29-35 wGA 的婴儿。实际风险差异分别为 35.9% (95% CI 19.8, 52.0, p=0.000)、15.7% (95% CI -8.0, 39.4, p=0.194) 和 36.2% (95% CI 22.5, 49.9, p=0.000)。
对于 ICU LOS,单臂汇总数据显示 29-32 wGA 婴儿的 ICU LOS 为 9.0、7.0 和 6.7脚注50、29-34/35 wGA脚注50 脚注51和 33-35 wGA脚注35 脚注50分别。没有研究表明健康足月儿需要 ICU LOS 住院。(表 4)
| wGA | 平均 LOS(天) | 95% CI | 数量研究 | 偏倚风险 |
|---|---|---|---|---|
| 29 – 32脚注50 | 9.0 | 7.0, 11.0 | 1 | 低 |
| 29 – 34/35脚注50 脚注51 | 7.0 | 4.7, 9.2 | 2 | 低 |
| 33 – 35脚注35 脚注50 | 6.7 | 5.5, 8.0 | 2 | 中等、低 |
对于 29-32 wGA 的婴儿,接受 MV 的住院患者的单臂合并比例分别为 27.0% 、 22% 和 14.0脚注50、29-34/35 wGA脚注50 脚注51、32/33-35 wGA脚注30 脚注35 脚注50分别。健康足月儿的 MV 率为 14.0%脚注52 脚注53.(表 5)
| wGA | % MV | 95% CI | 数量研究 | 偏倚风险 |
|---|---|---|---|---|
| 29 – 32脚注50 | 27.0 | 17.8, 36.2 | 1 | 低 |
| 29-34/35脚注50 脚注51 | 22.0 | 18.0, 26.0 | 2 | 低 |
| 32/33 – 35脚注30 脚注35 脚注50 | 14.0 | 10.0, 18.0 | -3 | 中等 (2)、低 |
| 健康术语脚注52 脚注53 | 14.0 | 9.0-21.0 | 2 | 中等、高 |
使用合并数据进行的研究间比较(均处于极低的COE)显示,住院早产儿与足月儿的MVRR分别为1.9(95%CI 1.4,2.6,p<0.000)、2.3(95%CI 1.8,2.9,p<0.000)和1.0(95%CI 0.76,1.32,p<-.000),29-32 wGA、29-35 wGA和33-35 wGA的婴儿。实际风险差异分别为 13.0% (2.0, 24.0, p=0.020) 、 18.0% (9.9, 26.1, p=0.000) 和 0.00% (-7.2, 7.2, p=1.000)。
对于29-32 wGA的婴儿,来自合并单臂研究的MV平均持续时间为10天(95%CI 7.6,12.4)、8.6天(95%CI 7.3,9.8)和6.5天(95%CI 3.5,9.4)(一项研究,ROB中等)脚注50,29-35 wGA (两项研究,中等 ROB)脚注50 脚注51和 33-35 wGA (两项研究,ROB 中等,低)脚注35,脚注50分别。没有研究报告健康足月儿的 MV 持续时间。
2020 年文献检索更新确定了 3 项报告了 ICU 收治情况的研究。RSVH 婴儿的 ICU 护理为 29-<35 wGA 婴儿的 25% (ROB 低)脚注38,64.2% 的 29-34 wGA 婴儿(ROB 中度)脚注54以及 48%、46% 和 49% 的 28-32 岁、33-34 和 35 wGA 婴儿 (ROB 低)。脚注556项研究报告了健康足月儿的ICU护理。百分比为 29%脚注57, 43.3%脚注62, 20%脚注63和 9%脚注59在 ROB 低和 3.4% 的研究中脚注56和 2%脚注58在中度 ROB 的研究中。
29-34 wGA 婴儿的中位 (IQR) ICU LOS 为 6 天 (ROB 中度)脚注5429-32 岁、33-34 岁和 35 wGA 的婴儿分别为 6 (3-11)、5 (3-10) 和 5 (3-6) 天(ROB 低)脚注55.对于健康足月婴儿,中位 ICU LOS 报告为 4 天 (IQR 3, 7.6) (ROB 低)脚注57和 0 天(范围 0-15)(中等 ROB)脚注56.
29-<35 wGA 婴儿的 RSVH 婴儿的 MV 为 5% (ROB 低)脚注38,29-34 wGA 婴儿为 31.8%(中度 ROB)脚注54,28-32 岁、33-34 和 35 wGA 的婴儿分别为 22%、20% 和 15%(ROB 低)脚注55.
在早期文献中,据报道,与足月儿相比,早产儿入住 ICU 的风险更高脚注60.在 2008-9 年的一项前瞻性队列研究中,5.9% 的 28 至 < 33 wGA 的婴儿需要入住 ICU(ROB 低)脚注61.后来对 2000-2014 年对 33-35 wGA 无合并症婴儿的研究进行的系统评价(AMSTAR 评为平均水平)报告称,22.2% 的婴儿需要入住 ICU 的中位时间为 8.3 天,12.7% 的婴儿需要 MV 的中位时间为 4.8 天脚注40.年龄越年轻,ICU 入住率越高。在一份 32-35 wGA 婴儿的报告中,没有 >6 个月大的婴儿需要重症监护,但 14% 的 3 至 < 6 个月大的婴儿和 27% 的 < 3 个月大的婴儿被收治在 ICU(实际年龄)脚注64.
III.1.1.4. 死亡率
在对 1990-2007 年研究的荟萃分析中,≤32 wGA 和 32-35 wGA 婴儿在第一个 RSV 季节的全因死亡率分别为 0.99% 和 0.13%。两组合并 RSV 归因死亡率为 0.03%(AMSTAR 评分平均值)脚注65.在 1975 年至 2011 年的另一项文献系统评价中,≤ 24 个月大的 RSV 住院儿童的加权平均病死率为早产儿 <37 wGA) 为 1.2%(范围,0-8.3%;中位数,0%;n = 10),而无严重 RSV 危险因素的儿童(AMSTAR 评级差)的加权平均值为 0.2%(范围 0-1.5%;中位数,0.0%;n = 6)脚注66.在 BODsr 中,一项极低 COE 的研究报告了 29-32 wGA 婴儿中有 1 例归因于 RSV 的死亡,而 33-35 wGA 组没有死亡,差异无统计学意义脚注50.
III.1.1.5. 风险评分
虽然任何程度的早产儿都可能在一定程度上增加 RSV 住院的风险,但为所有人提供预防是不可行的。在加拿大,每年 7.7-8.0% 的出生体重为 < 37 wGA脚注67据估计,5% 的出生队列可能在 32-35 wGA 时出生脚注34.已经开发了风险评分,试图识别 > 29-30 wGA 或 > 32 wGA 的健康早产儿,这些早产儿患严重 RSV 疾病的风险显着增加,目前在加拿大的几个省和地区以及国际上使用(见下面的附录 A)。被确定为显著的危险因素和用于这些风险评分的风险因素差异很大。此类分数的有效性,尤其是那些用几年前的数据或来自不同地理环境的数据验证的分数,一直受到质疑脚注7 脚注34 脚注68 脚注69 脚注70 脚注71.
RSV 季节的实际年龄年轻是确定的最一致的危险因素。其他因素包括增加暴露于 RSV 或更严重 RSV 疾病风险的环境和宿主因素。由于不同研究的结果不一致,因此很难确定与这些个体因素相关的 RSV 住院风险。大多数环境和宿主因素仅略微增加 RSVH 的风险,它们对 RSV 疾病负担的个体贡献有限脚注7 脚注70.在对风险因素(包括男性、儿童保育出勤率、烟雾暴露、缺乏母乳喂养和家中的其他儿童)进行多元 logistic-回归分析中,在调整其他协变量后,只有早产和年龄小与更严重的 RSV 疾病独立相关脚注69.
III.1.2 早产儿慢性肺病和其他慢性肺病
AAP 将 CLD 定义为“胎龄 <32 周出生,需要补充 O2至少在出生后的前 28 天内”脚注6.一些研究将 CLD 定义为需要 O2在概念年龄后 36 周。BODsr 和 2020 年更新的文献检索未发现该风险组的任何研究。
在对截至 2015 年 12 月的数据的系统评价中,由 AMSTAR 评为平均值,CLD 儿童在生命的前 2 年没有预防的 RSVH 发生率为 12-21%,加权平均值为 16.8%。CLD 与其他高危人群 RSVH 发生率较高,是 RSVH 的重要独立危险因素,比值比为 2.2 至 7.2脚注72.加拿大儿科学会的声明报告称,在 1995 年至 2009 年间进行的研究中,RSVH 为 6.0% 至 22.6%脚注8.
1992-6 年的一项回顾性队列研究报告了出生后第一年的 RSVH 率为 16.8%(ROB 中度)脚注42.PVZ RCT 对照组 CLD 的 24 个月大≤儿童 RSVH 率为 12.8%(ROB 中度)脚注48PVZ 观察性研究的对照组初次出院后 12 个月内的儿童为 15.7%(ROB 中度)脚注44.1989-93 年的一项研究报告称,出生后第一年的发病率高于第二年(38.8% 对 7.3%)(ROB 中度)脚注43.Winterstein 等人比较了 CLD 婴儿和有兄弟姐妹的健康足月婴儿的 RSVH 发生率。CLD 患者在 9 个月大时 RSVH 峰值率为 15.3/1000 个患者季节。18.5 个月龄 CLD 婴儿的 RSVH 率与 1 个月大的健康足月婴儿相似 (9/1000 个患者季节)脚注73.在该研究中,42.7% 的 CLD 婴儿接受了 PVZ。
关于住院以外的结局的数据有限。在 AMSTAR 评为平均水平的 Paes 系统评价中,RSV 的平均住院时间为 4-11 天,一项研究报告称,29% 的住院患者入住 ICU,24% 接受机械通气脚注72.在 Stevens 等人的回顾性队列研究中 (ROB 低),平均 LOS 为 9.4 天,9.1% 入住 ICU脚注42.一项被 AMSTAR 评为平均水平的荟萃分析报告称,第一个 RSV 季节的全因死亡率为 0.34%脚注74.在对 1975 年至 2011 年文献的系统评价中,因 RSV 住院的 ≤ 24 个月婴儿的加权平均病死率为 CLD 儿童的 4.1%(范围,0-10.5%;中位数,7.0%;n = 6)脚注66.
关于早产儿以外的病因的慢性肺病患儿的 RSV 风险数据有限。BODsr 确定了两项研究。据报道,患有先天性囊性肺病 (CCLD) < 24 个月大的婴儿 RSVH 发生率增加 (8.3%,95% CI 0.5,16.2)脚注75(ROB 中度)和接受皮质类固醇治疗的慢性间质性肺病 (chILD) 儿童 (30%,95% CI 9.9,50.1)脚注76(ROB 高)。在研究间比较中(均处于极低 COE),与足月儿相比,RSVH 的 RR脚注28 脚注29 脚注36 脚注37(所有 ROB 中等)CCLD 为 6.9 (95% CI 5.3, 8.9, p=0.000),chILD 为 25.0 (95% CI 14.3,43.6 p=0.000)。CCLD 的实际风险差异为 7.1% (95% CI 1.5, 12.7 p=0.013) 和 chILD 为 28.8 (95% CI 8.7, 48.9, p=0.005)。CCLD (ROB 低) 的平均 LOS 为 11.25 天 (95% CI 9.29, 13.21),chILD (ROB 中度) 为 6 天 (95% CI -0.6, 12.6)。在研究间比较中(极低 COE),LOS 与足月婴儿的平均差异为 CCLD 为 7.8 天 (95% CI -1.8, 17.3, p<0.112) 和 chILD 为 2.5 天 (95% CI -4.2, 9.2 p=0.465)。这两项研究中的患者均未因 RSV 入住 ICU。
在较早的一份报告中,Kristensen 等人报告了 < 24 个月大患有 chILD (27.3%)、先天性肺畸形 (13.7%)、其他先天性气道异常 (8.3%、9.3%) 和一些影响气道分泌物清除能力的神经肌肉疾病 (9.9%-15.9%) 的 RSVH 率,而该年龄段人群的总体发生率为 2.8%(ROB 中度)脚注21.
III.1.3 囊性纤维化
BODsr 确定了两项关于婴儿囊性纤维化 (CF) 的研究。RSVH 的合并比例为 12.3% (95% CI 1.3, 30.8) (ROB 高)脚注77 脚注78.在研究间比较中,与足月婴儿相比,RSVH 的 RR 为 10.3 (95% CI 3.3, 31.6, p<0.000),实际风险差异为 11.1% (95% CI -3.7, 25.9, p=0.140)。一项入院人数较少的研究报告的平均 LOS 为 47.00 (12.53, 81.47)(ROB 中等),远高于以前发表的研究,但作者没有评论脚注77.另一项研究 (中度 ROB) 报告的平均 LOS 为 10 天脚注78.由于缺乏数据(Groves 等人未报告标准差),因此没有对这些研究进行合并。在 Bjornson 的研究中,因 RSV 而入住 ICU 的高危人群比例为 2.4% (95% CI -0.9, 5.6) (ROB 中度)脚注77.在入院的 5 人中,2 人被送入 ICU (40%),1 人需要机械通气。平均入住 ICU 的时间为 5.00 天 (95% CI -2.84, 12.84) (ROB 中度)脚注77.另一项研究没有报告 ICU 收治情况脚注78.
早期报告还表明,RSVH 在囊性纤维化儿童中的发生率高于健康儿童。在 AMSTAR 评为平均水平的系统评价中,RSVH 的发生率为 6.4-18.1%,比健康儿童高 2.5-4.3 倍。平均 LOS 为 2-11 天,据报道 12.5% 的 ICU 收治率(8 名住院患者中有 1 名)脚注22.另一项被 AMSTAR 评为良好的囊性纤维化 PVZ 预防的系统评价报告称,未接受 PVZ 的患者的 RSVH 发生率为 7.5-11.7%脚注20.
III.1.4 先天性心脏病
在矫正手术通常延迟的时代,患有 hsCHD 的儿童发生 RSV 发病率和死亡率的风险很高。随着婴儿早期修复成为常态,预计患严重 RSV 疾病的风险会降低,尽管支持这一点的数据很少。美国的一项研究表明,在建议对这组患者进行 PVZ 预防之前,RSVH 发生率降低脚注79.
BODsr 确定了一项针对 hsCHD 儿童的研究。使用 1997 年和 2000 年的综合数据,每 1000 名 hsCHD 婴儿新生儿的 RSVH 发生率为 23 (95% CI 20, 26) (ROB 中度)脚注79.无法与健康足月儿的 RSVH 发生率进行研究间比较。对于其他报告的住院相关结局,仅提供了包括 PVZ 可用后几年的综合数据,因此这些结局被排除在分析之外。
在早期研究中,对 1995 年至 2015 年数据的系统评价(AMSTAR 评为平均水平)报告称,2 < 岁 hsCHD 儿童的 RSVH 发生率为 3.8% 至 10.2%脚注65.加拿大儿科学会的声明报告称,在 1992 年至 2008 年期间进行的研究中,RSVH 发生率为 1.3% 至 15%脚注8.
RSVH 率随年龄增长而降低。1998-2002 年一项 RCT 的安慰剂组发生率为所有婴儿(< 24 个月大)为 9.7%,6 个月<婴儿为 12.2%,6 至 12 个月为 7.3%,1-2 岁为 4.3%(ROB 低)脚注80.在观察性研究中,<12 个月大的 hsCHD 婴儿的 RSV 住院率也明显高于 12-24 个月大的婴儿。在 BODsr 中确定的研究中,报告了 1997 年至 2012 年美国的 RSVH,跨越 PVZ 前后时代,85% 的住院发生在出生后的第一年脚注79.Chiu 等人在 2005-10 年在台湾报告了出生后第一年紫绀型和无紫绀型 hsCHD 的 RSVH 发生率分别为 4.8% 和 2.1%,第二年分别为 0.9% 和 0.56%(ROB 中度)脚注81.Resch 在 2004-08 年的研究中报告了 9.6% 的住院率,其中包括患有 hsCHD 和无血流动力学意义的 CHD 的儿童,其中一些人接受了 PVZ,其中 56 例感染中有 58 例发生在出生后的第一年脚注82.在使用 1989-93 年的 Medicaid 数据对 CHD 儿童(不一定血流动力学显着)进行的研究中,估计第 1 年的 RSVH 率为 9.2%,第 2 年为 1.8%(ROB 中度)脚注43.
在 Checchia 的系统评价中,hsCHD 儿童 RSVH 的中位 LOS 为 7 至 9.7 天。入住 ICU 的住院患者比例为 30.4 – 46%,中位 ICU LOS 为 10 天,接受机械通气的比例为 30%脚注65.在 1998-2002 年 RCT 的安慰剂组中,平均 LOS 为 13.3 天,38.1% 的住院患者平均入住 ICU 19.2 天,22.2% 的患者需要 MV 平均 25.3 天(ROB 低)脚注80.在 Chu 的研究中,与没有 hsCHD 的儿童相比,因 RSV 住院的 hsCHD(联合或不联合 PVZ 预防)患儿的平均住院 LOS 更长(12.1 天 vs 3.4 天,p<0.001),MV 率更高(21.9% vs 2.3%,p<0.001)和更高的呼吸道合胞病毒相关死亡率(2.8 vs 0.1%,p<0.001)脚注79.
Feltes 等人报道了 hsCHD 为 0.6% (ROB 低) 的住院婴儿的 RSV 相关死亡脚注80.在对 1990 年至 2007 年研究的荟萃分析中,第一个 RSV 季节的全因死亡率为 4.17%,RSV 归因死亡率为 0.62%(AMSTAR 评级平均值)脚注74.在 1975 年至 2011 年的文献系统评价中,因 RSV 住院的 ≤ 24 个月婴儿的加权平均病死率为 CHD 儿童的 5.2%(范围,2.0-37.0%;中位数,5.9%;n = 7)脚注66.
III.1.5 唐氏综合症
有证据表明,患有唐氏综合症的儿童比健康儿童患 RSVH 的风险更高。这种增加部分是由 CHD、CLD 或早产等合并症解释的。排除患有这些合并症的儿童,风险仍然增加。可能的解释包括上呼吸道的解剖异常、气道软化、吞咽功能障碍、肌张力减退和免疫功能障碍脚注83.
BODsr 没有发现任何仅限于 2 < 岁儿童的唐氏综合症儿童研究。确定了一项中度 COE 观察性研究,比较了唐氏综合征儿童和 3 <健康儿童的 RSV 结局。对于患有唐氏综合征且没有其他严重 RSV 危险因素的儿童,据报道 RSVH 率为 2%,而健康对照为 1.1%,但 RSVH 数据存在一些不一致,无法进一步评估。中位 LOS 为 5 天,健康对照组为 2 天(平均差 3.00 天,95% CI 1.95,4.05)(低 COE)脚注84.
2018 年发表的一项荟萃分析对截至 2017 年 5 月的研究进行了评价,AMSTAR 将其评为平均水平,报告称,与健康对照组相比,所有唐氏综合征病例的 RSVH 合并比值比 (OR) 为 8.69 (95% CI 7.33, 10.30),合并 OR 为 16.66 (95% CI 7.22, 38.46),当仅纳入排除具有其他已知严重 RSV 危险因素的儿童的研究时(2 项研究)。该亚组的实际 RSVH 率分别为 7.6% 和 9.7%。唐氏综合征患儿,包括那些已知有严重 RSV 危险因素的儿童,LOS 增加(合并平均差 4.73 天;95% CI 2.12,7.33),氧气需求(合并 OR 6.53;95% CI 2.22,19.19);入住 ICU (汇总 OR: 2.56 95% CI 1.17, 5.59) 和机械通气需求 (汇总 OR 4.56;95% CI 2.17, 9.58) 和 RSV 相关死亡率 (汇总 OR 9.4;95% CI 2.26, 39.15) 与无唐氏综合征对照婴儿脚注83.作者报告说,在仅纳入没有其他危险因素的婴儿的单一研究中,没有死亡率,LOS、氧气需求、入住 ICU 和机械通气与整个组报告的没有差异。早期的系统评价(1995-2015 年)被 AMSTAR 评为平均水平,报告称患有唐氏综合症且没有其他已知严重 RSV 危险因素的婴儿的 RSVH 发生率为 3.6 – 13.5%。与健康婴儿的风险比为 3.5-10.5,平均 LOS 为 4-5 天脚注22.
III.1.6. 免疫功能低下的儿童
RSV 可导致免疫功能低下儿童的严重并发症和死亡率。血清和分泌抗体对于预防 RSV 感染很重要,需要 T 细胞来有效清除病毒。关于该群体 RSV 疾病负担的基于人群的数据很少。虽然大多数感染发生在幼儿中,但免疫功能低下的大龄儿童和成人也有患严重 RSV 疾病和死亡的风险。并发症发生率因免疫功能低下的严重程度而异脚注22.
BODsr 确定了两项针对免疫功能低下儿童的研究。2004-2012 年的一项美国多中心研究报告了 18 岁肝移植受者 <RSV 住院情况脚注85.多变量分析确定移植年龄 <2 岁是 RSVH 的预测因子 (p<0.001)。移植后前 2 年 (所有 <18 岁) 的 RSVH 率为 5.3% (95% CI 4.4, 6.2) (ROB 中度)。研究间比较(均在极低 COE)显示与健康足月儿相比,RSVH 的 RR 为 4.4 (95% CI 4.0, 4.9, p<0.000)。实际风险差为 4.1% (95% CI 3.2, 5.04, p=0.000)。入住 ICU 的住院患者比例为 22.2% (95% CI 15.2, 29.2) (ROB 低)。与健康足月婴儿相比,因 RSV 住院的患者入住 ICU 的 RR 为 1.4 (95% CI 0.8, 2.5,p=0.242,极低 COE)。实际风险差为 6.4% (95% CI -7.8, 20.6, p=0.375;极低 COE)。在入院患者中,10.4% (95% CI 5.2, 15.5) 接受了 MV (ROB 低)。与健康足月婴儿相比,入院婴儿 MV 的 RR 为 0.7 (95% CI 0.5, 1.1, p=0.156),实际风险差为 -3.6% (95% CI -11.5, 4.3, p=0.372,均处于极低 COE)脚注85.
第二项研究是 18 岁以下镰状细胞病儿童的 RSV 感染。这项单中心回顾性研究报告称,2 岁儿童 (ROB 中度) 的 RSVH 率为 63/1000 人年 (95% CI 44, 87) <。其他结局 (LOS、入住 ICU、机械通气) 仅报告了所有 18 岁以下儿童,与 2 < 岁健康足月儿的结局无显著差异脚注86.
一项早期的系统评价(被 AMSTAR 评为平均水平)报告称,造血干细胞和实体器官移植受者的大多数 RSV 感染发生在移植后的前 2 年。患有 RSVH 的 2 <免疫功能低下儿童的中位 LOS 分别为 7 天和 10 天,入住 ICU 的比例分别为 13% 和 19.1%,插管和/或机械通气的发生率分别为 3% 和 14.3%。总体病死率分别为 0% 和 4.8%脚注22.在 2-1997 年对 2 岁以下儿童进行的一项丹麦研究中,先天性免疫缺陷儿童的 RSV 首次住院率为 21.3%,癌症儿童的首次住院率为 8.4%,而这个年龄段人群的总体住院率为 2.8%。住院时间未增加 (ROB 中度)脚注21.
El Saleeby 等人报道了 1997 年至 2005 年间田纳西州 58 名 21 < 岁癌症患者的 RSV 感染情况。在多变量分析中,发现 ≤ 2 岁和 RSV 感染时淋巴细胞绝对计数 < 100/mm3 是 LRTI 发展的独立预测因子,OR 分别为 9.84 (95% CI 1.95, 49.8) 和 7.17 (95% CI 1.17, 44.03)。这些因素也与死亡显著相关脚注87.在西雅图对 HSCT 接受者(其中大多数是成年人)的研究中,症状出现时绝对淋巴细胞计数为 ≤100 / mm3 是 RSV 疾病进展的危险因素脚注88.
III.1.7 居住在偏远社区的儿童
BODsr 确定了两项针对偏远社区婴儿的研究。由于研究设计和患者群体的差异,这两项研究的数据没有合并。
2009 年对生活在加拿大北部因纽特人社区的婴儿(约占出生队列的 20%,有或没有早产或合并症)进行的一项研究报告称,<1 岁儿童的总体 RSVH 入院率为每年每 1000 名活产婴儿 66.9 例(ROB 高),西北地区的区域 RSVH 率为 2.0%, 努纳武特地区为 7.5%,努纳维克为 17.6%。在努纳武特的不同地区,比率分别为 19.5%、9.1% 和 3.7%脚注23.
第二项是对生活在美国西南部保留地的健康足月美洲原住民婴儿的研究脚注89.RSVH 率为 12.8% (95% CI 10.1, 15.5) (ROB 高)。在研究间比较中(极低的 COE),RSVH 的 RR 为 10.7 (95% CI 9.4, 12.1, p<0.000)。实际风险差异为 11.6% (95% CI 8.9, 14.3, p=0.000)。平均 LOS 为 4.7 天 (95% CI 4.2, 5.2) (ROB 中等)。LOS 与健康足月婴儿的平均差异为 1.2 天 (95% CI -0.10, 2.5),p<0.802,极低 COE)。入住 ICU 的住院患者比例 (ROB 中度) 为 6.3% (95% CI 1.0, 11.6)。入住 ICU 的 RR 为 0.4 (95% CI 0.04, 1.2, p=0.091)。实际风险差为 -9.5% (95% CI -22.9, 3.9, p=0.164)。平均 ICU LOS 为 5.2 天 (95% CI 2.1, 8.3) (ROB 中度)。2.5% 的住院患者 (95% CI 0.9, 5.9) (ROB 中度) 需要机械通气,平均持续时间为 6.5 天 (95% CI 3.6, 9.4) (ROB 中度)。
2020 年的文献检索更新没有发现任何关于生活在偏远社区的人群的研究。在那次搜索之后,魁北克省努纳维克最近的一项观察性研究的结果变得可用(ROB 高)脚注90.2013-2019 年所有 1 <婴儿的 RSVH 率为 5.0%(与 PCR 相比,调整快速抗原检测可能检测到后的 7.3%),远低于 2009 年报告的比率脚注91.
先前的研究表明,生活在偏远的北部因纽特人社区的儿童感染 RSV 的几率很高。2002 年,16.6% 的巴芬岛 1 岁以下婴儿因 RSV(ROB 中度)被巴芬地区医院收治。发病率从伊卡卢伊特婴儿的 6.3% 到来自高风险农村社区的婴儿的 34.9% 不等。对于 6 个月以下的婴儿,总体 RSVH 率为 25%,在高风险社区为 51%脚注91.Singleton 等人报告说,阿拉斯加的 YK 区是世界上 RSVH 发生率最高的地区,在 PVZ 之前时代,每年有 43.9% 的早产儿和 14.8% 的 1 <足月儿住院(ROB 高)脚注92.这些比率比发达国家报告的足月婴儿 1-2% 的总体比率高出许多倍,并且受感染的婴儿经常需要空运到社区医院或三级护理机构。
关于生活在北美其他原住民社区的儿童 RSV 疾病负担的数据非常有限脚注93也没有其他偏远社区的信息。
III.1.8 其他高危婴儿
BODsr 和 2020 年文献检索更新未发现任何其他有严重 RSV 疾病风险的群体。
III.2 RSV 感染和长期后遗症:反复喘息、哮喘和肺功能
几项研究表明,早期的 RSV LRTI 与儿童期的反复喘息有关。一些研究表明,RSV 后复发性喘息是短暂的,在第一个十年中,喘息会下降到背景水平脚注94.婴儿期 RSV 是否易患哮喘,或者遗传易患哮喘的婴儿是否在婴儿期患严重 RSV 疾病的风险增加,尚不清楚脚注95但后者有一些间接证据。在健康足月新生儿的前瞻性队列中,后来发生严重 RSV 感染和 RSV 后喘息的婴儿在新生儿期的肺功能检查结果低于未发生肺功能检查的婴儿脚注36,另一项研究表明,其他方面健康的足月新生儿后来发展为严重毛细支气管炎,支气管反应性过高脚注96.已经描述了易患严重 RSV 的遗传因素脚注94 脚注95.据报道,早期鼻病毒感染与哮喘之间存在关联脚注95,以及哮喘与早期呼吸道病毒感染频率之间的关联,而不是任何特定病因脚注97.世界卫生组织最近的一项审查确定,在确定 RSV 下呼吸道感染与儿童复发性喘息或哮喘之间的因果关系方面,证据尚无定论,并且证据并未确定 RSV 单克隆抗体会对这些结局产生实质性影响脚注98.
BODsr 确定了 6 项研究,这些研究评估了婴儿期 RSV 感染的长期呼吸道后遗症。
一项对 32-35 wGA 出生时 12 个月大时伴有或不伴有 RSV<H 的儿童的研究发现,父母或医生报告单纯性喘息(< 12 个月内发作 3 次)(RR 1.4,95% CI 1.15,1.60,绝对增加 18%),父母或医生报告复发性喘息(12 个月内 ≥3 次发作)(RR 1.70, 95% CI 1.27、2.29,绝对增加 19%),或医生报告从 2 岁到 6 岁出现严重喘息(≥ 1 次住院或 ≥3 次就医发作或连续 3 个月或累积 5 个月服用喘息药物)(RR 1.59,95% CI 1.13,2.24,绝对增加 14%)。第 6 年喘息几乎没有差异,单纯性、复发性和重度喘息的 RR 分别为 1.16 (95% CI 0.70, 1.93)、RR 1.28 (95% CI 0.71, 2.32) 和 RR 0.91 (95% CI 0.44, 1.88)。支气管扩张剂的使用(RR 1.48,95% CI 1.23,1.77,绝对增加 8%)、吸入皮质类固醇的使用(RR 1.65,95% CI 1.13,2.40,绝对增加 10%)和口服皮质类固醇的使用(RR 1.71,95% CI 1.06.,2.74,绝对增加 8%,白三烯拮抗剂的使用增加幅度更大(RR 2.52,95% CI 1.43, 4.42,2 至 6 岁绝对增加 10%(所有结局的 COE 均较低)脚注32.
一项研究比较了 < wGA 出生的婴儿与足月婴儿在 RSVH 后一年的喘息情况。两组在单纯、复发或重度哮鸣音方面无显著差异(RR 0.54,95% CI 0.18-1.55;RR 0.80,95% CI 0.04,16.14;分别为 RR 0.00,95% CI -0.34,0.34,但 RSV 的人数很小)(极低的 COE)脚注29.
一项对需要或不需要住院治疗的 RSV 感染健康足月婴儿出生后第一年喘息的研究发现,两组之间父母报告的每月喘息天数几乎没有差异(平均差 0.70;95% CI -0.94,2.34)(极低 COE)脚注36.
与出生后第一年患有 RSV 的哮喘母亲所生的健康足月婴儿相比,医生诊断为 7 岁哮喘的相对风险为 RR 2.33(95% CI 1.35,4.05,绝对增加 15%,OR 2.82,95% CI 1.38,5.77,p=0.005)。调整呼吸道感染总数后,OR 为 1.26,(95% CI 0.54,2.91,p=0.59 (COE 极低)脚注97.
足月出生且在 24 个月大时有或没有 RSVH 的个体在 28-31 岁时医生诊断为哮喘<没有差异 (RR 1.82, 95% CI 0.84, 3.94) (COE 极低)。自我报告的支气管扩张剂使用量增加 (RR 2.17, 95% CI 1.08, 4.34),自我报告的吸入性皮质类固醇使用量没有差异 (RR 1.56, 95% CI 0.62, 3.89) (COE 极低)脚注99.
一些研究还涉及肺功能。在 32-35 wGA 出生时一分钟用力呼气容积 (FEV1) Z 评分排名为 -2 或 -1 的儿童比例在 <12 个月大时患有或未患有 RSVH 的儿童中几乎没有差异 (RR 0.83, 95% CI 0.45, 1.53) (COE low)。脚注32
在 24 月龄时有或没有 RSVH 的婴儿在 17-20 岁或 28-31 岁时< 24 个月时进行评估。使用支气管扩张剂前,预测 FEV1 的平均百分比(平均差 -7.63,95% CI -11.35,-3.91)和预测用力肺活量 (FVC) 的平均百分比(平均差 -4.74,95% CI -7.80,-1.67)(COE 低)。预测 FEV1/FVC 的平均百分比(平均差 -3.20,95% CI -9.07,2.67)或 50% 过期 FVC (MEF50) 后预测最大呼气流量的平均百分比几乎没有差异(平均差 -4.00,95% CI -14.95,6.95)(COE 极低)脚注99 脚注100.支气管扩张剂给药后预测 FEV1 的平均百分比变化 (平均差 0.81,95% CI -0.67, 2.30) (COE 低) 几乎没有差异。关于支气管扩张剂给药后预测 FVC 平均百分比的变化(平均差 0.60,95% CI -0.67,1.87)(COE 极低)、FEV1/FVC(平均差 -0.20,95% CI -2.71,2.31)和预测 MEF50 平均百分比的变化(平均差 3.70,95% CI -5.42,12.82),证据非常不确定(COE 非常低)。在 24 月龄时,有或没有 RSVH 的患者<呼出气一氧化二氮分数差异很小或没有差异(平均差 -1.00,95% CI -14.49,12.49)(COE 低)脚注99 脚注100.
单臂数据显示婴儿 RSVH 后复发性喘息的发生率为 12.4% (95% CI 6.3, 18.5;ROB 中度),对于父母报告或医生诊断的复发性喘息,对于 8.0% (95% CI 3.0, 13.0),对于医生诊断的 6 岁严重喘息脚注32.在其他研究中,出生后第一年 RSVH 后医生诊断为哮喘的发生率为 26.9% (95% CI 14.9, 39.0;ROB 低)时 7 岁脚注97和 23.3% (95% CI 10.6, 35.9;ROB 中度)在 28-31 岁时脚注99.
2020 年文献综述更新确定了两项针对长期复发性喘息或哮喘的研究。在一项前瞻性出生队列研究中,对 32-25 wGA 的早产儿在 6 岁时随访父母报告的过去 12 个月内的喘息情况。据报道,婴儿期 RSVH 患儿中有 27.7% 出现喘息,而无 RSVH 的儿童为 17.6% (OR 1.80, 95% CI 1.11, 2.85)。调整混杂因素后,OR 为 1.89 (95% CI 1.06, 3.32)。当按特应性易感性(定义为至少一个父母的特应性疾病)分层时,差异仅对没有特应性易感性的组(ROB 高)有意义脚注101.
一项回顾性匹配队列研究,对在出生后第一年没有 RSV 感染或没有 RSV 感染的无 hsCHD、先天性肺病或呼吸道异常的足月婴儿进行了评估,评估了从行政索赔数据库中确定的出生后前 5 年的哮喘或反应性气道障碍。有或没有 RSV 感染史的儿童哮喘或反应性气道疾病的累积发生率为 25.2% vs 11.4%,aOR (95% CI) 2.6 (2.5, 2.9),p<0.0001;35.4% 对 16.7%,aOR 2.8 (2.6, 2.9),p<0.0001;和 24.4% vs 12.7%,aOR 2.2 (2.0, 2.4),p<0.0001 在三个管理数据库中(ROB 高)脚注102.
III.3 RSV 再感染
RSV 的再感染发生在一生中。自然获得的免疫力并不能防止后续感染,尽管它可能会改变疾病的严重程度,初始感染通常是儿童期最严重的感染脚注103 脚注104 脚注105.此外,两个抗原不同的 RSV 亚群 A 和 B 可能在同一季节传播脚注105 脚注106.在一项针对 30 名 2 岁以下患有支气管肺发育不良 (BPD) 的婴儿的研究中,一名儿童在同一季节有两次 RSVH (3.3%)脚注107.来自西班牙的两项针对妊娠 32 周出生儿童≤前瞻性研究报告了 6/584 (1.0%) 和 9/999 (0.9%) 的患者在同一季节复发 RSVH脚注108 脚注109.出于这些原因,NACI 之前的声明脚注4和 AAP脚注5如果婴儿在接受预防治疗时出现突破性 RSV 感染,建议继续使用 PVZ。
然而,最近的数据表明,在同一季节重复 RSV 感染的情况很少见。丹麦一项针对 240 名 <28 wGA 或出生体重 <1000 g 的早产儿的研究发现,只有 1 名儿童在同一季节患有 2 例 RSVH (0.4%)脚注110.在一项针对 CHD 儿童的 PVZ 安慰剂对照试验中,只有 0.39% 的儿童(安慰剂组 648 名中的 3 名和接受 PVZ 的 639 名中的 2 名)在同一季节的 RSVH 超过 1 次脚注80.在另一项对 429 名早产儿进行了 1 年随访的研究中,没有 RSV 再感染脚注111.一项门诊研究发现,在连续 726 个 RSV 季节中,5 岁以下儿童中有 8 例 RSV 下呼吸道感染。有 56 例再次感染,但只有 1 例发生在同一季节脚注112.在另一项针对 5 岁以下儿童的门诊研究中,在 2 个季节的 1802 名 RSV 呼吸道感染儿童中,只有 1 名在同一季节发生两次感染,一次是 RSV-A,一次是 RSV-B脚注113.由于同一季节重复感染的罕见性,AAP (2014)脚注6和 CPS (2015)脚注8现在建议,如果儿童在接受 PVZ 时出现突破性 RSVH,则应停止每月预防。
III.4 RSV 感染风险和多胞胎兄弟姐妹
在一项针对 BPD 早产儿的病例对照研究中,将 14 对双胞胎和 2 对三胞胎与 34 名单胎婴儿的出生日期和胎龄相匹配。多胞胎婴儿患 RSV 疾病的风险显著高于单胎婴儿 (53% vs. 24%;p=0.01),RSVH 发生率 (32% vs 18%;p=0.05) 和 RSV 肺炎发生率 (24% vs. 6%,p=0.05) 也是如此。在匹配的 logistic 多元回归分析中控制混杂因素后,多胞胎仍然仅与肺炎的发展显著相关 (p=0.048)脚注114.在另一项研究中,Resch 及其同事回顾性评估了 435 名妊娠 29-36 周无慢性肺病的早产儿因呼吸系统疾病住院的比率。他们发现多胞胎与 RSVH 相关 (55% vs. 15%,p=0.013)。未进行考虑混杂因素的多变量分析脚注115.
相比之下,两项关于 RSVH 相关危险因素的更大型前瞻性研究,共涉及 2326 名早产儿,发现 RSVH 组和对照组的多胞胎婴儿比例相似脚注71 脚注116.
在一项针对因 RSV 毛细支气管炎住院的婴儿的回顾性研究中,双胞胎占住院人数的 7.6% (66/875)。在 53 对双胞胎中,至少有一对双胞胎患有 RSVH,如果一对双胞胎住院,另一对双胞胎在同一时期也有 34% 的几率也因毛细支气管炎住院(24% 的几率因 RSV 阳性毛细支气管炎住院)。然而,双胎组婴儿比单胎婴儿更年轻,胎龄也更低。在多变量分析中,双胞胎出生并不是 RSV 疾病严重程度的重要危险因素脚注117.
III.5 医疗保健相关的 RSV 感染
RSV 经常在医院传播,包括在新生儿重症监护病房脚注118.现有数据表明,在新生儿病房接受 PVZ 预防的婴儿与出院时开始接受 PVZ 预防的婴儿相比,出生住院期间的 RSV 感染率没有差异脚注119 脚注120 脚注121.这些研究被评为一般(Harris 标准)脚注122.2003 年 NACI 关于 PVZ 的声明没有解决向住院患者管理 PVZ 的问题脚注4.2014 年 AAP 声明指出,符合预防条件的新生儿病房婴儿可以在出院回家前 48-72 小时或出院后立即接受一剂脚注6.CPS 指出,对于在 RSV 季节首次出院回家的符合条件的婴儿,PVZ 应在出院前开始脚注8.英国的绿皮书指出,属于适当风险群体的新生儿病房婴儿应在出院前 24 至 48 小时开始 PVZ。脚注123为避免每天为即将出院的单身婴儿打开小瓶时浪费,建议将给药协调为每周 3 次脚注121.
PVZ 经常用于控制新生儿病房中的 RSV 爆发。在某些情况下,对所有暴露的婴儿进行 PVZ脚注118 脚注124 脚注125 脚注126 脚注127,在其他情况下,只有那些有资格作为门诊患者参加 PVZ 的人脚注118 脚注127 脚注128.PVZ 是在一些疫情中的其他感染控制措施失败后开始的脚注118 脚注124,以及在其他人认识到疫情爆发时脚注118 脚注125 脚注126 脚注127 脚注128.无法确定 PVZ 在控制这些疫情方面发挥的增量作用脚注118.当其他措施未能控制疫情爆发或预计感染控制建议的依从性不佳时,PVZ 可能有用脚注118 脚注126.
虽然 AAP 2014 或 CPS 声明中没有提及,但 2009 年 AAP PVZ 声明表明,在季节早期开始 PVZ 预防并在到期剂量之日住院的婴儿应按计划接受该剂量脚注5.同样,英国绿皮书规定,那些已经开始 PVZ 疗程但随后住院的婴儿应在住院期间继续接受 PVZ 治疗脚注123.
产品
IV.1 授权在加拿大使用的制剂
目前在加拿大唯一获准用于预防严重 RSV 疾病的产品是 PVZ(Synagis,艾伯维阿斯利康,安大略省密西沙加)。PVZ 是一种通过重组 DNA 技术生产的人源化单克隆抗体 (IgG1κ),直接作用于 RSV F 蛋白 A 抗原位点的表位,这是一种在 RSV 分离株中高度保守的表面蛋白。它是 95% 人和 5% 小鼠氨基酸序列的复合体®脚注129.它于 2002 年被授权在加拿大使用。
注射用 PVZ 溶液有 50 mg/0.5 ml 和 100 mg/1 ml 一次性小瓶两种规格。包括的非药用成分是氯化物、甘氨酸、组氨酸和注射用水脚注129.
IV.2 疗效和有效性
PVZ 在预防严重 RSV 疾病高危儿童 RSV 感染严重后果方面的疗效和有效性研究在即将发布的“关于 PVZ 预防对减少婴儿呼吸道合胞病毒相关并发症的影响的文献综述”中进行了报道。结果总结如下。在有严重 RSV 感染风险的婴儿的混合人群中,PVZ 预防与 RSV 相关住院风险降低 38 – 86% 相关,需要治疗人数 (NNT) 以防止 2 至 24 人住院。混合人群健康状况的差异排除了关于不同患者群体的相对益处的明确结论。对混合人群的研究不会在这里进一步讨论,但包含在即将发布的文献综述中。
IV.2.1 无婴儿慢性肺病的早产儿
IV.2.1.1 RSV 相关住院
12 项研究检查了 PVZ 预防对无 CLD 早产儿 RSVH 的影响:平均质量的系统评价和荟萃分析脚注74,4 项 RCT 报告为良好脚注41 脚注48或平均质量脚注111 脚注130,六项观察性队列研究脚注131、一般或一般脚注27 脚注44 脚注49或差脚注47 脚注132质量和 1 项质量一般的案例对照研究脚注133.
对 1990 年至 2007 年研究的系统评价和荟萃分析发现,与不预防相比,使用 PVZ 与 ≤32 wGA 出生的婴儿的 RSVH 减少 72% 和 74-32 wGA 出生的婴儿减少 35% 相关脚注74.1996 年进行的 IMPACT RCT 报告称,接受 PVZ 的 6 个月≤无 CLD 的早产儿因 RSV 住院率降低了 78%,NNT 为 16脚注48.32 wGA ≤婴儿下降 47%,32-35 wGA 婴儿下降 72%脚注48.Notario 等人进一步分析了按胎龄组划分的 IMpact 研究的数据。PVZ 导致 28-31 wGA (73%) 、 29-32 wGA (80%) 、 32-34 wGA (82%) 和 32-35 wGA (82%) 的婴儿住院率显著降低,但 <29 wGA 或 33-35 wGA 的婴儿没有。后两组的人数很少脚注41.NNT 范围为 13 至 21 岁,并随着胎龄的增加而降低。在 2008-10 年招募的 33-35 wGA 婴儿的后期 RCT 中发现了 PVZ 预防的类似显着保护作用 (82%。NNT 24)脚注111以及 2009-11 年入组的 ≤32 wGA 出生婴儿的小型 RCT (OR 0.26, NNT 5)脚注130.
在 2002 年至 2006 年进行的被评为一般质量的前瞻性病例对照研究中,PVZ 预防 RSVH 的有效性为 29-35 名 wGA 婴儿的 74%。在 29 wGA <未观察到有效性,但数量很小脚注133.
关于 PVZ 预防对早产儿 RSVH 的影响,观察性队列研究的结果相互矛盾。一项对 2012-2015 年出生儿童质量一般的回顾性队列研究发现,与未接受预防的婴儿 (NNT 53) 相比,接受 PVZ 的 29-32 wGA 婴儿在第一个 RSV 季节的 RSVH 率降低了 38%,但在接受和未接受 PVZ 预防的 33-36 wGA 婴儿中,RSVH 没有统计学意义差异。然而,后一组接受 PVZ 治疗和坚持 PVZ 预防的儿童人数较少脚注27.
在一项质量一般的观察性研究中,与 2000-2008 年出生的历史对照组相比,2011-2013 年入组的 ≤ wGA 无 CLD 婴儿的 PVZ 预防并未显著降低 RSVH 发生率脚注44.然而,样本量很小。
在一项被评为高质量研究中,PVZ 在 2002-35 wGA 出生的儿童队列中没有显着效果脚注131.另一项针对 1995-2004 年 32-34 wGA 出生婴儿的队列研究,被评为一般质量,发现德克萨斯州的 RSVH 显着降低(OR=0.45,95% CI 0.26,0.78,p=0.005),但在佛罗里达州没有(OR=0.81,95% CI 0.42,1.58,p=.54)脚注49.
在一项被评为低质量的研究中,发现 PVZ 预防可显著降低 1999-2004 年 ≤30 wGA 出生的儿童队列的 RSVH(1.1% 对 13.6%,NNT 9)脚注47.
总之,基于早期 RTC,有充分的证据表明 PVZ 对 28-35 wGA 早产儿的疗效。对 32-36 wGA 婴儿的观察性研究结果相互矛盾的结果很难解释,但部分可能是由于研究设计、依从性、地点和时代的差异。三项研究,一项为良好,两项为一般质量,表明对 < 29 wGA 的婴儿没有影响,但这可能是由于这个非常早产儿中没有 CLD 的婴儿数量少脚注41 脚注44 脚注133.一项质量差的观察性研究支持对 ≤ 30 wGA 的婴儿有保护作用。一般来说,似乎有证据支持 PVZ 在减少早产儿 RSVH 方面的有效性,尽管从数据中尚不清楚 PVZ 最有效的早产儿水平。
IV.2.1.2. 死亡率
唯一一项检查全因死亡率的研究是 Checchia 等人对平均质量的系统评价和荟萃分析。在 ≤32 wGA 出生的婴儿中。与安慰剂或无干预的接受者相比,PVZ 接受者的全因死亡风险显著降低 (OR=0.25, 95% CI 0.13, 0.49, p<0.001),而在 GA 32-35 周出生的婴儿中,差异不显著 (OR=0.22, 95% CI 0.03, 1.89, p=0.085)脚注74.
PVZ 预防对该人群的全因死亡率可能影响不同,对 ≤32 周 GA 出生的婴儿有保护作用,但在较低早产儿水平(32-35 周 GA)中没有。然而,这些发现是基于少数研究,这些研究可能不足以检测早产儿死亡率的差异。
IV.2.1.3 长期后遗症
IV.2.1.3.1 复发性喘息和特应性哮喘
六份报告研究了 PVZ 预防对出生后最初几年喘息风险的影响:来自随机对照试验的两份质量一般或一般的报告脚注111 脚注134以及来自两项 Good 队列研究的 4 份报告脚注135、一般或一般脚注136 脚注137而且很差脚注138质量。一项研究脚注111仅调查父母报告的喘息,而其他 5 项研究调查了医生诊断或父母报告和医生诊断的喘息。三项研究发现,PVZ 预防发生在 33-35 wGA 出生的其他方面健康的早产儿脚注111 脚注138或 ≤35 wGA脚注136,导致儿童在出生后第一年喘息的风险显著降低 (46-66%)脚注111,至 3 岁脚注138,或入组后 ≤36 个月至 2 年脚注136.
在 Simoes 等人的队列研究的另一份报告中,接受 PVZ 预防的儿童在研究入组后 24 个月医生诊断的喘息发生率显著降低,并且与未接受干预的儿童相比,III次医生诊断的喘息发作的时间显着延长,但仅限于没有哮喘或特应性家族史的儿童。在有哮喘或特应性家族史的儿童中,这些结局没有显著差异脚注135.
对 33-35 wGA 出生的儿童队列的随访,最初评估 3 岁时喘息脚注138发现,与未接受预防的儿童相比,接受 PVZ 预防的儿童在出生后的前 6 年内经医生诊断的复发性喘息的发生率降低。然而,这种关联仅在有过敏家族史的儿童亚组中发现。作者将特应性哮喘(反复喘息和 IgE 升高)与复发性喘息区分开来,发现接受 PVZ 的儿童和未接受 PVZ 的儿童的特应性哮喘发生率相似,无论过敏家族史如何脚注137.在 Blanken 等人 RCT 中入组婴儿的 6 岁随访中,PVZ 和安慰剂接受者之间的差异仅对父母报告不频繁喘息(每年 1-3 次发作)的婴儿有意义。在过去 12 个月内,医生诊断的哮喘或使用哮喘药物没有显著差异,6 岁时的肺功能在两组之间没有差异脚注134.
PVZ 似乎在降低幼儿出生后最初几年复发性喘息的发生率方面可能具有持续的影响,但关于 PVZ 与特应性家族史对年龄较大儿童后续复发性喘息的相对影响,研究结果是矛盾的。从这些研究中也不清楚在什么水平的早产儿 PVZ 最能有效地产生长期影响。在 32-35 或 33-35 wGA 的婴儿中预防 1 例复发性喘息的 NNT 为 7-8脚注111 脚注136 脚注137 脚注138, 10 代表 29-32 wGA脚注13615 分,< 29 wGA脚注136.
IV.2.1.3.2 生长参数
一项质量一般的队列研究评估了 33-35 wGA 出生儿童在 6 岁时的生长参数脚注137.研究发现,接受 PVZ 的儿童与接受 PVZ 的儿童在体重、身高或体重指数方面没有显著差异。
IV.2.2 患有婴儿慢性肺病的早产儿
IV.2.2.1 RSV 相关住院
5项研究检查了这一结局。1996 年对 ≤35 wGA 和 ≤24 个月出生的 BPD 儿童进行的一项高质量随机对照试验发现,与接受安慰剂的婴儿相比,PVZ 接受者发生 RSV 相关住院的风险降低(RR=0.61,95% CI 0.40,0.95;NNT 21)脚注48.在一项被评为一般的观察性研究中,与 2000-2008 年出生的历史对照组相比,2011 年至 2013 年入组的 CLD 婴儿在初次出院后的前 6 个月内,PVZ 预防将 RSVH 率降低了 86% (NNT 13)。按胎龄计算,≤28 wGA (89%,NNT 12) 的减少显著,而 29-35 wGA 的减少则不显著,但后一组的人数很少脚注44.1999-2002 年对 ≤32 wGA 出生的婴儿质量差进行的早期前瞻性观察队列研究发现,PVZ 预防与 RSVH 风险降低相关(RR=0.15,95% CI 0.05,0.49,p<0.01;NNT 3) 在第 1 个 RSV 中脚注139.另一项包括 24 个月以下 CLD 儿童的低质量前瞻性观察性研究也报告了 RSVH 的风险降低 (RR=0.28,95% CI 0.14,0.58,p<0.007;NNT 8)脚注46.在 2002 年至 2006 年进行的一项前瞻性病例对照研究中,对 ≤35 wGA 和 <12 个月或 12-24 个月大的婴儿进行了评定为一般质量的研究,住院率没有显著降低脚注133.
结果表明,PVZ 预防可降低该人群中 RSV 相关住院的风险,但胎龄对这一益处的影响尚不清楚。
IV.2.2.2 死亡率
一项对平均质量的荟萃分析显示,PVZ 与无干预/安慰剂相比对早产 CLD 全因死亡率没有观察到的影响(0.22% 对 0.34%;Peto OR,0.83;95% CI 0.13, 5.25),但预防组只有 3 个事件,安慰剂/无干预组只有 2 个事件脚注74.
IV.2.3 囊性纤维化儿童
IV.2.3.1. RSV 相关住院
6项研究检查了这一结局。一项质量被评为良好的系统评价确定了 1998-2001 年进行的一项 RCT。该研究发现,接受 PVZ 预防或安慰剂的囊性纤维化儿童的 RSVH 无显著差异 (RR 1.02 (95% CI 0.06, 16.09)。然而,每组中只有一名儿童因 RSV 住院脚注140 脚注141.一项质量一般的小型观察性研究发现,与 2003-2007 年接受 PVZ 的儿童相比,1997-2002 年未接受 PVZ 的历史对照更有可能患有 RSVH (21.3% 对 4.4%,p=0.027;NNT 6)脚注78.其他三项观察性研究发现 PVZ 受者和对照组之间的 RSVH 没有显着差异。在 Bjornson 等人于 2000 年至 2017 年进行并被评为一般的研究中,PVZ 接受者的住院率为 2.7%,对照组为 6.0% (p=0.20)。在调整混杂因素后,接受 PVZ 的儿童的 RSV 住院率仍然没有显著低于未接受 PVZ 的儿童。然而,PVZ 接受者因呼吸系统疾病住院的比率显著降低,RSV 的总体检测率较低,为 53%脚注77.1999-2006 年的一项质量较差的大型研究脚注142,以及一项对 2001-05 年 PVZ 接受者的小型研究,以及 1997-2000 年的历史控制,质量也很差脚注143未发现 PVZ 预防与不干预相比对后续 RSVH 有显著益处。2001-12 年进行的一项质量一般的病例对照研究发现,PVZ (5%) 和对照组 (2.9%) 之间的 RSVH 没有显着降低脚注144.
从这些研究的结果中,无法得出关于 PVZ 预防在降低囊性纤维化儿童 RSVH 风险方面的有效性的结论。只有 Groves 等人的观察性研究发现 PVZ 预防对 RSVH 有显著的预防作用脚注78.在该研究中,对照组的 RSVH 发生率非常高,参与者人数很少。大多数研究的样本量很小,并且可能不足以检测效果。Winterstein 等人的大型研究是一个例外,该研究使用了医疗保健提供者的管理数据库脚注142.一些患有囊性纤维化的儿童,例如,那些在出生后的前 1 年或 2 年患有严重慢性肺病的儿童,可能会受益。
IV.2.3.2 RSV 引起的其他医院结局
IV.2.3.2.1 RSV 导致的住院时间
一项质量一般的观察性队列研究检查了 PVZ 对囊性纤维化儿童因 RSV 住院时间的影响。PVZ 接受者的平均住院时间 (5.7 ± 2.4 天) 显著短于对照组 (47 ± 39 天),p=0.048脚注77.早期一项质量差的小型历史队列研究发现,与接受安慰剂的儿童 (13,IQR: 2-14) 相比,PVZ 接受者 (11,四分位距: 3-14) 的 RSVH 中位天数没有显著差异 (OR=0.46, 95% CI 0.16, 1.31)脚注143.
目前,由于一项评估质量较差的小型研究的结果可能不足以检测差异,因此无法就 PVZ 预防对囊性纤维化儿童 RSVH 持续时间的影响得出确切结论。
IV.2.3.2.2. 因 RSV 入住重症监护病房
一项研究评估了这一结局。183 名 PVZ 接受者和 2 名对照者中有 84 名因 RSV 入住 ICU。在因 RSV 住院的患者中,对照组 5 名患者中有 2 名需要入住 ICU脚注77.
IV.2.3.2.3 RSV 引起的呼吸支持的使用
Robinson 等人研究了 PVZ 预防对囊性纤维化儿童因 RSV 而使用氧疗的影响。在氧疗需求方面,两组之间没有发现显著差异;然而,结局数量很少 (PVZ 预防组,n=1;安慰剂干预组,n=0)脚注140.在 Bjornson 的研究中,2.2% 的 PVZ 受者和 1.2% 的对照组需要增加呼吸支持,无论是 MV 还是氧疗 (p=0.58)脚注77.在 Buchs 的研究中,没有患者需要补充氧气或 MV脚注144.
IV.2.3.3 全因死亡率
RCT 研究检查了 PVZ 预防在降低囊性纤维化儿童全因死亡率方面的有效性。然而,由于在研究期间的 6 个月随访期间,两组均未发现死亡,因此无法得出关于 PVZ 预防对该结局影响的结论脚注140.Fink 等人的一项更大规模的队列研究也报告了接受或未接受 PVZ 的患者在 2 岁之前的全因死亡率没有差异脚注145.
IV.2.3.4. 长期后遗症
IV.2.3.4.1 肺功能
一项质量一般的小型历史队列研究发现,在 6 岁时的随访评估中,接受和未接受 PVZ 的囊性纤维化患儿的肺功能(通过 FEV1 测量评估)无显著差异脚注78.Fink 等人的队列研究被评为质量差,也发现接受或未接受 PVZ 的人在 7 岁时的 FEV1 没有差异脚注145.
IV.2.3.4.2 生长参数
RCT 发现,在 12 个月的随访中,PVZ 组和安慰剂组在体重增加或体重身高比方面没有显著差异脚注140.一项小型历史队列研究发现,接受和未接受 PVZ 预防的儿童在 6 岁时的生长参数(体重、身高、体重指数)没有显著差异脚注78.Buchs 等人的病例对照研究也发现,PVZ 受体和对照组在生命前 3 年的生长方面没有显着差异脚注144.
IV.2.3.4.3 铜绿假单胞菌和金黄色葡萄球菌定植
RCT 发现,在 12 个月的随访中,与接受安慰剂的儿童相比,接受 PVZ 的儿童铜绿假单胞菌气道定植儿童的数量没有统计学意义差异。脚注140在 Groves 等人的研究中,PVZ 受者首次分离铜绿假单胞菌的中位时间明显短于非受者,并且 PVZ 受者在研究期间首次分离的相对风险也显著增加。然而,在 6 岁随访时,两组慢性铜绿假单胞菌定植率无显著差异脚注78.Buchs 等人报告说,PVZ 预防对铜绿假单胞菌或金黄色葡萄球菌首次定植的年龄或 3 岁时铜绿假单胞菌定植的儿童比例没有显著影响。与对照组 (85%) 相比,PVZ 接受者 (97%) 到 3 岁时被金黄色葡萄球菌定植的婴儿比例显著增加脚注144.Fink 等人还报告了在有或没有 PVZ 预防的患者之间首次铜绿假单胞菌定植的时间没有差异脚注145.
这些研究的结果似乎一致,在接受和未接受 PVZ 预防的囊性纤维化儿童之间检查的长期后遗症没有显着差异。然而,研究的儿童数量很少。
IV.2.4 血流动力学显著的先天性心脏病患儿
IV.2.4.1. RSV 住院 (RSVH)
五项研究检查了 PVZ 预防对 hsCHD 儿童的疗效或有效性。1998-2002 年进行的高质量 RCT脚注80发现与接受安慰剂的儿童相比,在 RSV 季节开始时年龄为 ≤24 个月且接受 PVZ 预防的 hsCHD 儿童的 RSVH 显着相对降低 (RD=45%,p=0.003;NNT 23)。这在无紫绀型 CHD 患儿中具有统计学意义 (RD=58%,p=0.003;NNT 15),但在紫绀型 CHD 儿童中不常见 (RD=29%,p=0.285)。一项对 2013-2015 年 PVZ 接受者进行前瞻性随访的 1 < 岁婴儿质量一般的观察性队列研究,回顾性确定 2010-15 年的对照组发现,所有病例均显著降低 49% (NNT 45),紫绀型 hsCHD 亚组降低 65% (NNT 31),但无紫绀性疾病患者无显著降低 35%脚注146.在一项质量一般的小型观察性研究中,所有 1 岁 hsCH<D 病例的住院相对危险度为 0.28(减少 72%,NNT 7),该研究报告了 2014-16 年间入组的 PVZ 受者和 2007-09 年出生的历史对照脚注147.一项针对 2003-07 年 PVZ 接受者和 1998-03 年出生的历史对照的早期低质量观察队列研究未发现,与不干预相比,PVZ 预防可显著降低 RSVH 对 RSV 季节开始时出生的 ≤36 w 和 ≤24 个月大的 CHD 儿童(RR=0.58, 95% CI 0.21, 1.65),但对照人群的 RSVH 率非常低 (2.9%)脚注148.在 2002-6 年进行的一项质量一般的前瞻性病例对照研究中,在出生后的第一年或第二年都没有观察到显著的 PVZ 有效性脚注133.
这些研究表明,PVZ 对 hsCHD 婴儿 RSVH 的保护作用结果相互矛盾。两项未显示显著效果的研究脚注133 脚注148与两项显示风险降低 45-49% 的大型研究相比,参与者人数较少脚注80 脚注146.其中一项研究表明,对紫绀型心脏病儿童有显著保护作用,但对无紫绀型心脏病儿童没有保护作用脚注146,但另一个显示相反脚注80.这些差异的原因并不明显,但可能是由于样本量不足,无法检测亚组的差异。
IV.2.4.2. RSV 引起的其他医院结局
IV.2.4.2.1. RSV 导致的住院时间
涉及 ≤24 个月大的 hsCHD 儿童的 RCT 发现,与安慰剂接受者相比,PVZ 接受者每 100 名儿童的 RSVH 总天数相对显著减少 (RD=56%,p=0.003)脚注80.对于因 RSV 入院的患者,PVZ 接受者的平均 LOS 为 10.8 天,安慰剂为 13.3 天,差异无统计学意义。在 Chiu 等人的研究中,接受或未接受 PVZ 的患者的 LOS 没有显著差异,无论是对于总组还是对于紫绀型或无紫绀型 hsCHD 患者脚注146.
IV.2.4.2.2 因 RSV 入住重症监护病房和在重症监护病房停留的时间
对 ≤24 个月大的 hsCHD 儿童的 RCT 报告说,与安慰剂接受者相比,PVZ 接受者入住 ICU 的人数相对减少,但减少不显著 (RD=46%,p=0.094)脚注80.在观察性队列研究中,Chiu 等人报告了接受 PVZ 的患者和未接受 PVZ 的患者在 ICU 入院率方面没有显著差异,无论是对于整个组还是对于紫绀性或无紫绀性 hsCHD 患者,Harris 等人也发现 ICU 入院率没有显着差异。在这三项研究中,接受 PVZ 的组和未接受 PVZ 的婴儿因 RSV 住院而需要入住 ICU 的婴儿比例也没有显著差异脚注80 脚注146 脚注148.
在 RCT 中,PVZ 和安慰剂接受者因 RSV 在 ICU 中总天数/100 名儿童没有显著差异脚注80.在 Harris 的队列研究中,平均 ICU LOS 从 14.9 天下降到 10 天,但差异不显著脚注148.
IV.2.4.2.3 RSV 导致的机械通气 (MV)
Feltes 等人的 RCT 发现,与安慰剂接受者相比,接受 PVZ 的 hsCHD 儿童和 RSV 季节开始时 ≤24 个月大的 HSCH 儿童在 MV 的使用方面没有显著差异(RD=41%,p=0.282)脚注80.
IV.2.4.2.4. RSV 引起的氧疗持续时间
RCT 发现,与安慰剂相比,接受 PVZ 预防的儿童/100 名接受氧疗的儿童的总天数显著减少 (RD=73%,p=0.014)脚注80.
这些结果表明,对于因 RSV 感染住院的 hsCHD 患儿,接受 PVZ 不会影响疾病的严重程度,如医院 LOS、ICU 收治、ICU LOS 或需要 MV 所表现,尽管研究数量很少。
IV.2.4.3 全因死亡率
Feltes 等人的 RCT 和 Harris 等人的队列研究都检查了该人群的全因死亡率脚注80 脚注148.在 RCT 中,与安慰剂接受者相比,接受 PVZ 治疗的 hsCHD 儿童和 RSV 季节开始时 ≤24 个月大的全因死亡率没有显著差异。Harris 等人的研究报告了无干预组有 1 例死亡,PVZ 预防组无 1 例死亡。
RCT 报告了 639 名 PVZ 接受者中有 2 名和 648 名对照中有 4 名死于 RSV (p=0.46)脚注80.
IV.2.5 唐氏综合症儿童
IV.2.5.1 RSV 相关住院
三项研究检查了 PVZ 预防对减少唐氏综合征婴儿 RSVH 的影响。2012-14 年进行的一项针对一般质量儿童的小型观察性队列研究发现,没有其他 PVZ 预防标准的唐氏综合症儿童的住院率在接受 PVZ 和未接受 PVZ 的儿童中没有显着差异(3% 对 15%,p=0.075)脚注149.一项较早、质量较差的更大规模队列研究将 2005-2012 年接受 PVZ 的加拿大唐氏综合症儿童与 2003-05 年出生但未接受 PVZ 的荷兰唐氏综合症登记处的儿童进行了比较脚注150.在调整了 hsCHD 、不显著的 CHD、胎龄和出生体重后,分析发现,与无干预相比,接受 PVZ 与 RSVH 降低 72% 具有统计学意义相关 (IRR=3.63 95% CI 1.52,8.67,p=0.002;NNT 12)。当分析仅限于具有至少一项 RSV 预防标准风险标准的儿童 (hsCHD,出生在 ≤35 wGA,CLD) (IRR 3.39 (1.02–11.25)) 时,也发现住院率显着减少。然而,当分析仅限于没有标准 RSV 风险标准的儿童时,接受 PVZ 预防的儿童与未接受干预的儿童之间 RSVH 的差异不显著 (IRR=6.57 95% CI 0.70, 62.16)。III项研究被评为良好,报告称,在日本批准对所有唐氏综合征患儿进行 PVZ 预防后,总体 RSVH 有所降低。对于所有儿童,接受 PVZ 的儿童的校正比值比 (aOR) 为 0.41 (95% CI 0.18, 0.92, p=0.03),但在无 hsCHD 的组中 RSVH 没有差异 (aOR 0.43, 95% CI 0.04, 4.26, p=0.47) 或没有 RSVH 的其他危险因素 (aOR 0.68, 95% CI 0.06–7.73, p=0.75)脚注151.
IV.2.5.2 RSV 引起的其他医院结局
IV.2.5.2.1 RSV 导致的住院时间
Yi 等人研究的观察性研究发现,与未接受干预的儿童相比,PVZ 接受者因 RSV 导致的平均住院天数没有显著差异(6.4 天对 12.4 天,p=0.48)脚注150.
IV.2.5.2.2. 因 RSV 入住重症监护病房和在重症监护病房停留的时间
Yi 等人的观察性研究报告说,接受 PVZ 预防的 532 名儿童中没有一人被收治在 ICU,而在没有 PVZ 的 233 名儿童中,有 4 人被收治到 ICU (p=0.0085)。ICU 的平均 LOS 为 10.3 天脚注150.
IV.2.5.2.3 RSV 引起的机械通气 (MV) 的使用和持续时间
Yi 等人的研究也没有接受需要 MV 的 PVZ 预防的儿童,而在没有 PVZ 的组中,有 4 名儿童需要 MV (p=0.0085)。MV 的平均持续时间为 10.3 天脚注150.
IV.2.5.2.4 RSV 所致氧疗的使用和持续时间
Yi 等人的研究发现,与未接受 PVZ 的儿童相比,接受 PVZ 预防的儿童对辅助氧疗的使用明显较少(2/532,0.004% 对 19/233,0.08%,p<0.001)和氧疗的平均使用天数更少(4 天 vs 13.7 天,p=0.046)脚注150.
这些研究结果的重要性,质量差的研究之一脚注150另一项涉及极少数儿童脚注149尚不清楚,但表明 PVZ 可能对没有其他可能需要 PVZ 给药的疾病的唐氏综合征儿童没有益处。在得出关于 PVZ 对该人群的益处的结论之前,还需要进一步的研究。
IV.2.6 居住在偏远社区的婴儿
IV.2.6.1 RSV 相关住院
有两项质量较差的队列研究检查了这一结局脚注92 脚注152.Banerji 等人的研究包括来自加拿大努纳武特地区的因纽特儿童,他们出生时体重为 <36 wGA 和/或患有严重的心脏或呼吸系统疾病,并且在 2009-10 RSV 季节开始时年龄为 <6 个月。与未接受干预的符合 PVZ 条件的儿童 (5/10, 50%) 相比,接受 PVZ 的儿童的 RSVH (2/91, 2.2%) 显著减少 (OR=0.04,95% CI 0.008, 0.26,p=0.0005)。预防 1 例 RSVH 所需治疗的人数为 2脚注152.由于并非所有符合 PVZ 条件的婴儿都被确定,实际减少率可能低于报告的减少率。在 Singleton 等人的研究中,在 1998 年为高危婴儿引入 PVZ 计划之前和之后,对阿拉斯加土著儿童的 RSVH 进行了评估,在 ≤36 wGA 出生的婴儿中,RSVH 显着降低(相对率 0.34,95% CI 0.17,0.68,p<0.001)。引入 PVZ 计划后,在高危婴儿中,首次 RSVH 发生率为每 1000 个 PVZ 保护日 0.55 例和每 1000 个无保护日 1.07 例(相对率 0.52;95% CI 0.28,0.93)。预防 1 例 RSVH 所需治疗的人数为 4 例脚注92.
尽管已知居住在偏远北部社区的因纽特婴儿患 RSVH 的风险很高脚注23,关于 PVZ 预防该组住院的有效性的数据非常有限。在完成 PVZ 有效性文献综述后,魁北克省努纳维克 (Nunavik) 在 RSV 季节为 3 个月以下的健康足月婴儿提供 PVZ 预防的计划结果现已公布脚注90.研究质量被评为一般。在 2016 年 11 月至 2019 年 6 月期间,646 名符合条件的健康足月婴儿中有 73% 接受了一些 PVZ,但只有 37% 按时接受了所有推荐剂量。通过以下方式评估 PVZ 有效性:1) 比较按时接受所有剂量 PVZ 的婴儿和未接受 PVZ 的婴儿的 RSVH,以及 2) 比较 PVZ 保护和无保护日的 RSVH。RSVH 发生在 10/237 名接受 PVZ 的婴儿 (4.2%) 和未接受 PVZ 的婴儿中 7/177 (4.0%)。PVZ 直接有效性计算为 -6.7%,宽 95% CI 为 -174.8、85.5。RSVH 发生率为 37.6/100,000 个 PVZ 保护天数和 39.1/100,000 个无保护天数,直接保护效果为 3.8%,95% CI -1167.6,64.9。该研究的局限性包括 RSVH 数量少、不同年份 RSVH 差异大以及与其他呼吸道病毒混合感染的发生率高。具体请参见附录 C 中的数据表。
IV.2.7. PVZ 预防建议变化的影响。
在关于 RSV 疾病负担的文献检索中确定了几项研究,这些研究通过分析实施修订建议前后的连续时间段,描述了 2014 年 AAP 修订的 PVZ 使用建议对 RSVH 的影响脚注6.这些研究不符合文献综述的标准,因为未确定接受或未接受 PVZ 的儿童,但在此处总结。
在北达科他州的一项三级中心研究中,每 1,000 名儿童 <24 个月大) 的 RSVH 率在 2014 年指导期之前(2012-13 和 2013-14 赛季)为 5.37,在 2014 年后指导期(2014-2015 赛季)为 5.78(率差为 +0.4,95% CI -1.2,+2,p=0.622)。RSV 入院人数为 194 人。在 2014 年指南期间,每 1000 <名 24 个月大儿童接种的 PVZ 剂量为 21.7 剂,在 2014 年后指南期间为 10.3 剂,减少了 11.4 剂(95% CI 14.3,8.4,p<0.001)脚注153.
来自密尔沃基的另一项单中心研究研究了 ≥29-35 wGA 出生的 1 岁以下婴儿的 RSVH 数量,以及该胎龄组所有 RSV 入院的比例实施 2014 年 AAP 指南实施前 2 个季节和之后两个季节(2012-2017 年)。RSVH 数为 91.新指南实施前后该胎龄组的入院人数或入院比例无显著差异。住院时间从实施前的中位数 5.86 天增加到实施后的中位数 7.86 天 (p=0.02),但对 ICU、补充氧气或 MV 的需求没有差异脚注154.
俄亥俄州的一项单中心研究考察了 2014 年指南实施前后 <12 个月大婴儿的 RSVH。在 1063 名 RSVH 中,29 岁出生的婴儿0/7-346/7wGA 在 2013-4 赛季占 7.1% (34/482),在 2014-5 赛季占 9.8% (57/581)(没有显著差异)。2013-14 年 29-34 岁 wGA 的 <6 个月婴儿占 RSVH 的 3.5% (17/482),而 2014-15 年为 7.1% (41/581) (p=0.01)。其中 290/7-346/72014-15 年 <3 个月大、氧气管理(40.0% vs 78.9%;p=0.05)、儿科 ICU 收治(30.0% vs 68.4%;p=0.04)、MV(10.0% vs 52.6%;0.04)、住院时间(1.8 vs 8.8 天;p=0.04)的 wGA 其他方面健康的婴儿均较高。在 2013-14 年和 2014-15 年期间,在 3 至 <6 或 6 至 <12 个月的早产儿中未观察到发病率差异。PVZ 资格从 2013-14 年的 32.3% 下降到 2014-15 年的 1.8% (p<0.001)脚注51.
一项大型研究使用商业数据库和 Medicaid 数据库来评估 2011 年 7 月 1 日至 2016 年 6 月 30 日之间出生的婴儿。婴儿被归类为早产儿或足月儿,并确定 < 6 个月婴儿因 RSV 住院的情况。计算比较早产儿和足月儿住院率的比率。早产儿与足月儿指导变化前的季节性比率在 1.6 至 3.4 之间。指导值变更后,季节性比率在 2.6 至 5.6 之间。2014 年至 2016 年,与足月分娩相比,29-34 wGA 早产的相关风险显著高于 2012 年至 2014 年(商业保险婴儿为 2.00,p<0.0001,医疗补助婴儿为 1.46,p<0.0001,p<0.0001)。不同 wGA 和年龄组的 PVZ 使用量减少了 74-97%脚注155.
一项使用类似数据库的早期研究评估了 2014-2015 年季节 29-36 wGA 早产儿的 PVZ 使用和 RSVH 率以及 2013-2014 年季节的比率。相对于 2013-2014 赛季,2014-2015 赛季 29-34wGA 婴儿的 PVZ 预防利用下降了 62% 至 95% (p< 0.01)。与 2013-2014 赛季相比,2014-2015 赛季 29 至 34wGA 婴儿的 RSVH 率分别增加了 2.7 倍 (p=0.02) 和 1.4 倍 (p=0.03),年龄为 <3 个月大,有商业和医疗补助保险。3-6 月龄未观察到显著差异脚注156.
另一项研究调查了建议变化对 hsCHD 患儿的影响。2014 年 AAP 指南建议对出生后第一年的人进行 PVZ 预防,而以前的指南建议对 2 <的人进行预防。回顾了美国国家行政医疗保健数据库,以确定在 2012-2014 和 2014-2016 RSV 季节因 RSV 收治的 < 24 个月 CHD 儿童。644-2012 和 2013-2014 赛季有 2014 例 RSV 入院,625-2014-15 和 2015-2016 赛季有 2016 例。建议更改后,13-24 个月大的 CHD 儿童的 LOS、ICU 收治率或院内死亡率没有变化。无论年龄如何,13-24 个月大的儿童均无死亡。研究的人群不仅限于 hsCHD 患者脚注157.
继 2014 年发布 AAP 修订后的建议后,意大利于 2016 年秋季对其他方面健康的早产儿使用 PVZ 实施了类似的限制。在意大利一个地区的 284,902 名 <2 岁儿童中,RSVH 的数量为 1729 人。在政策改变后,观察到 RSVH 数量从 6.3/1000 (95% CI 6.0, 6.7) 减少到 5.5/1000 (95% CI 5.0, 5.9)。在政策变更前后的 2 个季节,因 RSV 入院的儿童入院的 wGA 或年龄无显著差异。政策变更后,PVZ 的处方数量减少了 48%脚注158.
在意大利的单个三级中心对连续三个 RSV 季节 (2014-15、2015-16、2016-2017) ≤ 1 岁儿童的 RSVH 进行了回顾性回顾。3 个赛季的 RSV 总入院人数为 366 人。29 – 36 wGA 组早产比例在 3 个季节中分别从 6.6% 增加到 7.3% 到 9.2%,33 – << 36 wGA 亚组分别从 5.1% 增加到 6.4% 到 8.3%。这些增加在统计学上不显著,但样本量很小脚注159.
在意大利的三个新生儿 ICU 中,在引入更严格的 PVZ 建议之前 (2015-2016) 或之后 (2016-2017) 对 29-35 wGA 出生的婴儿的 RSVH 进行了另一项回顾性队列研究。2015-16 年有 262 名婴儿入组,2016-17 年有 274 名婴儿入组。2015-16 年和 2016-17 年婴儿 RSVH 发生率分别为 1.9% 和 5.1%(比值比 2.77;95% CI 0.98,7.8,p=0.045。未接受 PVZ 的婴儿比例从 2015-16 年的 63.7% 显着增加到 2016-17 年的 80.6% (p< 0.0001)脚注160.
总之,关于 2014 年 AAP 建议变化对 29 至 35/36 wGA 早产儿 RSVH 影响的人群数据很少。一项小型单中心研究报告称,总体 RSVH 发生率没有差异。一项大型管理数据库研究表明,3 个月<早产儿的 RSVH 发生率增加了 1.4 至 2.7 倍。其他研究着眼于年龄为 29-35 wGA 的 RSV 入院儿童的比例。两项单中心研究显示这一比例没有差异。一项研究显示入院患者的发病率没有差异,而另一项研究报告称年龄偏小,3 个月 < 岁入院患者的发病率更高,但年龄较大的婴儿则没有。另一项大型数据库研究比较了 RSV 收治患者的早产儿与足月儿的比率,报告称早产儿与足月儿的比率增加了 1.5 至 2 倍。一项针对 13-24 个月 CHD 儿童的研究显示,因 RSV 住院的儿童的发病率没有增加。意大利也做出了类似的政策变化。两项研究显示没有显著影响,而III项研究报告称 29 至 <36 wGA 婴儿的 RSVH 发生率增加了 2.7 倍。然而,RSVH 率从一个季节到另一个季节存在重要差异,这些研究仅涵盖政策变化前后的 1 或 2 个季节。
IV.3 免疫原性
IV.3.1 PVZ 级别
PVZ 是一种被动免疫剂。≥ 30 ug/mL 的 PVZ 血清浓度显示可将 RSV 在棉鼠肺部的复制减少 99%脚注161.基于这些数据,在婴儿临床试验中,≥40 ug/mL 被任意选择为首选目标谷水平脚注48 脚注80 脚注162.在这些研究中,间隔 30 天给予 5 剂 15 mg/kg。基于 22 项临床试验数据的药代动力学计算机模型表明,该时间表将在 6 个月内提供高于目标谷值的水平脚注163.
PVZ 的半衰期为 19-27 天脚注164.谷 PVZ 水平随着连续剂量的增加而增加。15 mg/kg 剂量 1、2、3 和 4 后 30 天的平均 SD 谷血清浓度分别为 37±21 μg/mL、57±41 μg/mL、68±51 μg/mL 和 72±50 μg/mL±脚注165.在一项对 CHD 儿童 PVZ 的研究中,第 2 剂和第 5 剂前的血清浓度 (平均值 ±SD) 分别为 55.5 ±19 μg/mL 和 90.8 ±35 μg/mL。在 139 例接受心脏搭桥手术的患者中,搭桥前后测得的 PVZ 水平分别为 98.0 ±52 ug/mL 和 41.4 ±33 ug/mL,下降了 58% (p=0.0001)脚注80.以前的 NACI 指南和 AAP 指出,对于将继续需要预防的 CHD 儿童,心脏搭桥后应给予 15 mg/kg 剂量的 PVZ脚注4 脚注6.AAP 还建议,如果仍需要预防,则在体外膜肺氧合结束时考虑额外 15 mg/kg 剂量脚注6.
已经探索了给予少于 5 剂 PVZ 的可能性。最近的一项建模研究预测,如果第 1 剂和第 2 剂间隔 29 天给药,随后的 3 剂间隔 38 天,则 30 至 40 ug/mL 的水平将维持 181 天。只需 4 剂,这些水平就可以维持 143 天脚注166.CPS 建议计划应最多接种 3 至 5 剂,如果仅在社区有 RSV 活动时才开始 PVZ,特别是如果间隔 38 天接种第 2、3 和 4 剂,则所有风险群体的 4 剂可能就足够了脚注8.
然而,每隔 38 天给药实施起来更复杂,并且可能导致更多的浪费;间隔 35 天可能更实用。不列颠哥伦比亚省的一个项目给予了 4 剂 PVZ,前 2 剂之间间隔 21-28 天,后续剂量之间间隔 28-35 天。RSVH 发生在 666 名婴儿中的 10 名 (1.5%)。除一组双胞胎在第 4 剂后 65 天住院外,所有病例均为 PVZ 突破性病例。其他 18 例 (2.7%) 在接受 PVZ 时因毛细支气管炎住院,但未进行 RSV 检测。为 514 名 29 至 <35 wGA 出生且无慢性肺或 CHD 的低风险儿童提供了 3 剂方案。一名儿童在接受 PVZ 时因 RSV 入院,另一名儿童在第 3 剂后 58 天入院脚注167.
对 2012 年至 2016 年接受 4 剂 PVZ 的不列颠哥伦比亚省 391 名患有 CHD 的儿童进行的进一步队列研究表明,已证实或潜在(未测试)RSV 下呼吸道感染的入院率为每 100 个 PVZ 批准 6.2 例脚注168,该比率类似于在 CHD 儿童每月 5.3 剂临床试验中观察到的 5.3%(不包括未进行 RSV 检测的呼吸系统疾病)脚注80.只有一名儿童在最后一次 PVZ 给药后 30 天以上出现 RSVH。在另一项研究中,保护性中和抗体水平(定义为中和滴度 (NT95) 为 ≥ 1/12 稀释度)在最后一次 PVZ 给药后平均 55 天 (范围 28-105 天) 存在。在未接受 PVZ 的 4-11 个月对照婴儿中,也有 54% 的患者发现了保护性中和抗体水平,这表明对亚临床 RSV 感染的体液反应可能有助于中和 PVZ 给药后持续存在的滴度脚注169.
人们对 PVZ 水平的巨大个个体内差异表示担忧脚注163 脚注165以及如果使用较少的 PVZ 剂量或更长的剂量间隔对保护的影响。第一剂后的低谷水平导致建议缩短第一剂和第二剂之间的间隔脚注170.据报道,33% 的受者在第一次给药后出现 <40 ug/ml 的谷值脚注164.在一份报告中,46% 的突破性 RSV 感染发生在第一次给药后的间隔内脚注171但这种高比率尚未在其他研究中复制。对 42 名尽管有 PVZ 但仍因 RSV 住院的患者进行的回顾性回顾显示,较低的 PVZ 水平与入住 ICU 之间存在相关性。需要 ICU 护理的患者的平均水平为 47.2 ug/mL,不需要 ICU 护理的患者的平均水平为 98.7 ug/mL (p< 0.0001)。在上述研究的多变量分析中,包括潜在的混杂因素,与入住 ICU 相关的唯一参数是 PVZ 水平脚注172.
IV.3.2. 剂量方案和 RSV 季节性
一年一度的“RSV 季节”是感染 RSV 的风险足够高以保证对高危婴儿进行预防的时期。在加拿大,这个季节通常从 10 月或 11 月开始,到 4 月或 5 月结束,大多数病例发生在 12 月至 3 月。每年 RSV 季节的持续时间因年份和地点而异,据报道,在美国不同地点从 13 周到 23 周不等脚注7在安大略省汉密尔顿市 90 至 181 天脚注173.由于 5 个月一剂应提供 > 6 个月的保护水平,因此 AAP 建议最多接种 5 剂脚注6.如果使用当地病毒学实验室数据来确定何时开始预防,则可以优化 PVZ 的使用脚注173.如果无法获得此类数据,则开始日期可能由儿科 RSVH 数据或前几个季节确定。在某些地区,每月 4 剂可能就足够了脚注174.在加拿大,一些计划通常在 11 月或 12 月开始,而另一些计划则使用当地的实验室和住院数据来确定 RSV 季节(见附录 A)。后者可能比使用固定日期更复杂,但可能更有效地使用产品。
在某些地区,在主要季节之前或之后可能偶尔出现 RSVH,但在季节高峰期将从预防中获得最大益处。
IV.4 安全性
PVZ 通常被认为是安全的商品。由于 NACI 2003 PVZ 声明中对不良事件 (AE) 的描述脚注4没有安全警报,但暴露于 PVZ 的婴儿数量已大幅增加。NACI 确定这需要对 PVZ 安全数据进行新的评估。对 2003 年以后的出版物进行了快速文献检索,并对加拿大警戒计划的数据进行了回顾。有关 PVZ 安全的完整报告作为附录 B 附于本文档中,如下所示。
IV.4.1 快速文献综述
确定了 9 项 RCT、2 项基于人群的队列研究、来自登记处或队列的 26 份描述性报告以及 2 份病例报告。被认为与 PVZ 相关的最常见报告的 AE 是注射部位反应、发烧、紧张或易怒、咳嗽、鼻炎和腹泻。PVZ 相关的严重不良事件 (SAE) 非常罕见,报告了 1% 或更少的接受者,大多数研究没有报告。大多数是超敏反应。确定了 3 例过敏反应报告。因 AE 而停用 PVZ 的受者发生在 0-2.3% 的受者中。没有可归因于 PVZ 的死亡。重复注射人源化单克隆抗体引起了人们对免疫介导疾病发展的关注。研究表明,暴露于 PVZ 的儿童患自身免疫性疾病或特应性疾病的风险没有增加。
IV.4.2 来自加拿大警戒计划的数据
对向加拿大卫生部加拿大警戒计划报告的 AE 的审查确定了 259 例 PVZ 后 AE 病例报告,其中 237 例被归类为严重病例。最常见的事件是呼吸道事件,有 137 例 (53%),其中 113 例是感染,主要是由于 PVZ 产品失败,其次是超敏反应,有 23 例 (9%)。报告的其他事件是推荐使用 PVZ 的潜在疾病的预期并发症,并且与产品专论中报告的事件一致。PVZ 在这些 AE 中的作用尚不清楚,因为未评估因果关系。
IV.5 疫苗管理
PVZ 以 15 mg/kg 体重的剂量通过肌肉注射给药。
有关剂量间隔和剂量数,请参阅上文免疫原性,第 IV.3 节。
IV.6 储存要求
PVZ 应储存在 +2 至 +8°C 之间的原始容器中。它不应该被冷冻。样品瓶为一次性使用,不含防腐剂。
如果患者每月注射不需要整瓶(50 毫克或 100 毫克),医生应在 6 小时内安排多名患者接受 PVZ脚注4或在同一诊所当天脚注175为了最大限度地减少产品浪费。如果样品瓶中含有 6 小时内未使用的产品,则应丢弃且不要储存。每周为特定地区的符合条件的婴儿提供诊所,有助于以最少的浪费实现高效使用。
IV.7 与其他疫苗同时接种
PVZ 是一种专门针对 RSV 的抗体,不含其他抗体或人血清。预计它不会干扰对活疫苗或灭活疫苗的免疫反应脚注7 脚注129.接受 PVZ 的儿童应按照推荐的时间表接种所有常规儿童疫苗和可能因潜在健康状况而需要接种的任何其他疫苗。
IV.8 禁忌症和注意事项
禁忌症
对 PVZ 的任何成分显着超敏反应是使用本品的禁忌症。
注意事项
轻微疾病,如普通感冒,伴或不伴发烧,都不是使用 PVZ 的禁忌症。中度至重度疾病,伴或不伴发热,是考虑推迟 PVZ 的一个原因,以避免 PVZ 的不利影响叠加在基础疾病上,或错误地将基础疾病的表现识别为 PVZ 的并发症。延迟 PVZ 的决定取决于基础疾病的严重程度和病因。
经济学
V.1 系统评价
对 RSV PVZ 预防的成本效益进行了系统评价。回顾了 2000 年至 2018 年在经合组织国家进行并发表的研究。原始综述已发表脚注176.出于 NACI 的决策目的,对原始审查的报告和讨论进行了更改,可以作为 NACI 增刊找到,题为“PVZ 对呼吸道合胞病毒 (RSV) 的成本效益:系统评价”,该补充即将发布。变化包括以加元报告的货币、加拿大研究部分、报告的替代子组和其他评论。补充剂的结果总结如下。在最终分析纳入的 28 项研究中,20 项是成本效用分析,8 项是成本效益分析。两项经济评价是基于试验的脚注177 脚注178,其余的都被视为基于模型的。研究在美国 (n=6)、加拿大 (n=5)、荷兰 (n=3)、英国 (n=3)、西班牙 (n=3)、奥地利 (n=2)、德国 (n=2) 以及意大利、墨西哥、新西兰和瑞典 (各 1 项) 进行。从卫生系统支付者角度 (n=15) 或社会角度 (n=13) 进行基本案例分析。其中 8 项付款人视角研究从社会角度进行了额外的分析。大多数研究是由行业赞助的 (n=17, 61%)。成本效益结局以 ICER 报告,主要表示为每增加 QALY 的增量成本 (n=20) 和每次避免的住院成本 (n=6)。ICER 调整为 2017 年加元 (CAD)。
PVZ 预防的范围从作为主要策略(即成本更低、更有效)到拥有 2,975,489 美元/QALY 的 ICER。ICER 的巨大差异取决于观点、研究环境、人群、当地 RSV 流行病学、医疗保健系统和关键模型输入参数,例如 RSVH 的减少率 (39%-96%)、估计的 RSV 相关死亡率 (1%-8.1%)、PVZ 成本(每 1,099 毫克小瓶 2,198 美元-100 美元)、剂量方案和小瓶使用情况。
V.1.1 以每 QALY 成本表示的结局的经济评价
表 1 和表 2 总结了数据。对于从卫生系统支付者的角度报告每个 QALY 成本的成本效益的研究,有 22 个早产儿的成本效益估计值,范围从每个 QALY 6,216 美元到每个 QALY 的 938,623 美元不等脚注82 脚注179 脚注180 脚注181 脚注182 脚注183 脚注184 脚注185 脚注186 脚注187 脚注188.估计数次高的亚组是 (i) 按风险因素评分分层的早产儿脚注185 脚注186 脚注187,(ii) 患有 CHD 的婴儿脚注82 脚注179 脚注181 脚注182 脚注190 脚注191 脚注192,以及 (iii) 患有 CLD 的婴儿脚注82 脚注181 脚注182 脚注187 脚注191.表 1 显示了报告的低于不同阈值的成本效益估计数的比例。低于 50,000 美元/QALY 的常用阈值的报告估计值中一致性最大的是 CLD 婴儿(6 项研究中的 n =6)、早产儿 (n=18/22) 和 CHD 婴儿 (n=8/10)。对于早产儿,未检测到 wGA 和 ICER 之间的特定趋势。从社会角度来看,PVZ预防被认为是某些情况下早产儿的主要策略(即成本更低、效果更广)。脚注183 脚注193 脚注194 脚注195、加拿大北极地区的足月婴儿脚注196和患有 CHD 的婴儿脚注182.然而,在综述研究(包括那些报告 PVZ 预防是主要策略的研究)中,研究设计和模型参数存在高度异质性。PVZ 预防占主导地位的共同驱动因素似乎不存在。在其他情况下,观察到 ICER < 200,000 美元/QALY。一般来说,人们会预期从社会角度来看的 ICER 低于从支付方的角度来看的 ICER,但这一趋势并未观察到。支付者和社会视角估计通常来自不同的研究,模型设计存在异质性,特定环境成本与 RSV 流行病学之间存在差异,这可能解释了在社会角度下更大的 ICER。
其中 12 项研究由行业赞助。值得注意的是,200,000 <美元/QALY 的所有估计中,50% 和 19% 的 200,000 美元/QALY 的所有估计中>来自由行业资助的研究(S. Mac 个人通信,2019 年 3 月)。
| 健康状况 | ||||||||
|---|---|---|---|---|---|---|---|---|
| CLD 系列 | CHD | 早产儿 | 早产儿伴 CLD | 有危险因素的早产儿脚注* | CF 系列 | 加拿大北极脚注** | ||
| 所有婴儿 | 高风险区域 | |||||||
| 付款人视角 | ||||||||
| 估计数 | 6 | 10 | 22 | 4 | 14 | 2 | 6 | 2 |
| ICER (最低) | 4,786 | 11,668 | 6,216 | 15,202 | 215 | 167,107 | 主导 | 主导 |
| ICER (最大值) | 46,821 | 164,946 | 938,623 | 131,874 | 205,563 | 693,105 | 178,057 | 391 |
| 占主导地位的估计值的比例 | 0.0 | 0.0 | 0.0 | 0.0 | 0.0 | 0.0 | 0.17 | 0.50 |
| CE 低于 50,000 美元/QALY 的估计比例 | 1.00 | 0.80 | 0.82 | 0.75 | 0.64 | 0.0 | 0.67 | 1.00 |
| CE 低于 100,000 美元/QALY 的估计比例 | 1.00 | 0.90 | 0.86 | 0.75 | 0.86 | 0.0 | 0.67 | 1.00 |
| CE 低于 200,000 美元/QALY 的估计比例 | 1.00 | 1.00 | 0.91 | 1.00 | 0.92 | 0.50 | 1.00 | 1.00 |
| 社会视角 | ||||||||
| 估计数 | 1 | 8 | 23 | 3 | 6 | 0 | 6 | 2 |
| ICER (最低) | 28,529 | 主导 | 主导 | 18,717 | 21,931 | N/A | 主导 | 主导 |
| ICER (最大值) | 28,529 | 209,666 | 2,975,489 | 138,282 | 635,172 | N/A | 175,291 | 主导 |
| 占主导地位的估计值的比例 | 0.0 | 0.13 | 0.13 | 0.0 | 0.0 | N/A | 0.17 | 1.00 |
| CE 低于 50,000 美元/QALY 的估计比例 | 1.00 | 0.63 | 0.39 | 0.67 | 0.17 | N/A | 0.67 | 1.00 |
| CE 低于 100,000 美元/QALY 的估计比例 | 1.00 | 0.63 | 0.48 | 0.67 | 0.50 | N/A | 0.67 | 1.00 |
| CE 低于 200,000 美元/QALY 的估计比例 | 1.00 | 0.88 | 0.52 | 1.00 | 0.67 | N/A | 1.00 | 1.00 |
所有 ICER 均以 2017 年加元 (CAD) / QALY 报告。主导 = 成本更低,效率更高 CLD,慢性肺病;CHD,CHD;CF 囊性纤维化 N/A:不可用 | ||||||||
| ICERS:胎龄(周)早产儿 (wGA) | |||||||
|---|---|---|---|---|---|---|---|
| 26-28 | < 29 | 29-30 | 29-32 | < 32 | < 33 | 32-35 | |
| 付款人视角 | |||||||
| 估计数 | N/A | 3 | N/A | 3 | 2 | 3 | 6 |
| ICER (最低) | N/A | 6,216 | N/A | 9,989 | 12,710 | 16,434 | 26,170 |
| ICER (最大值) | N/A | 24,009 | N/A | 58,872 | 25,065 | 42,730 | 919,073 |
| 占主导地位的估计值的比例 | N/A | 0.00 | N/A | 0.00 | 0.00 | 0.00 | 0.00 |
| CE 低于 50,000 美元/QALY 的估计比例 | N/A | 1.00 | N/A | 0.67 | 1.00 | 1.00 | 0.67 |
| CE 低于 100,000 美元/QALY 的估计比例 | N/A | 1.00 | N/A | 1.00 | 1.00 | 1.00 | 0.67 |
| CE 低于 200,000 美元/QALY 的估计比例 | N/A | 1.00 | N/A | 1.00 | 1.00 | 1.00 | 0.83 |
| 社会视角 | |||||||
| 估计数 | 4 | 5 | 2 | N/A | 3 | N/A | 4 |
| ICER (最低) | 165,301 | 22,765 | 449,264 | N/A | 主导 | N/A | 32,390 |
| ICER (最大值) | 2,406,619 | 1,359,641 | 1,083,976 | N/A | 主导 | N/A | 338,823 |
| 占主导地位的估计值的比例 | 0.00 | 0.00 | 0.00 | N/A | 1.00 | N/A | 0.00 |
| CE 低于 50,000 美元/QALY 的估计比例 | 0.00 | 0.40 | 0.00 | N/A | 1.00 | N/A | 0.75 |
| CE 低于 100,000 美元/QALY 的估计比例 | 0.00 | 0.80 | 0.00 | N/A | 1.00 | N/A | 0.75 |
| CE 低于 200,000 美元/QALY 的估计比例 | 0.25 | 0.80 | 0.00 | N/A | 1.00 | N/A | 0.75 |
所有 ICER 均以 2017 年加元 (CAD) / QALY 报告。主导 = 成本更低,效率更高 N/A:不可用 | |||||||
V.1.2 以避免的每次住院费用表示结果的经济评价
6 项研究报告了每次避免住院成本 (cost per hospitalizations avoided, HA) 方面的成本效益脚注179 脚注197 脚注198 脚注199 脚注200 脚注201.一项针对加拿大北极不同地区健康足月婴儿的研究从付款人的角度比较了 6 个月以下婴儿的两种 PVZ 预防情况。ICER 的范围从特定北极地区的主导地位(即成本更低、更有效)到西北地区的 593,250 美元/公顷脚注197.同样从支付方的角度来看,佛罗里达州一项针对早产儿 (<32 wGA)、患有 CHD、CLD 的足月儿、所有三组的组合以及无 PVZ 指征的婴儿的研究报告称,ICER 在 413,127 美元/HA(早产儿)和 2,924,911 美元/HA(无适应症的婴儿)之间脚注201.
从社会角度来看,荷兰一项针对具有额外风险因素(BPD、男性、出生体重< 2,500 克)的早产儿 (< wGA) 的研究发现,ICER 在 24,875 美元/公顷和 1,572,268 美元/公顷之间,具体取决于预防月份脚注198.在一项来自德国的针对具有额外危险因素的早产儿 (<35 wGA) 的研究中,从社会角度来看,患有 CLD 和危险因素的早产儿和没有 CLD 且没有兄弟姐妹的早产儿的 ICER 范围在 11,821 美元/HA 和 364,462 美元/HA 之间脚注199.新西兰的一项研究从社会角度分析了早产儿 (<28, 29-31 wGA) 伴或不伴 CLD 的预防成本效益。ICER 范围从吸氧回家的早产儿 33,376 美元/公顷,到≤ 28 wGA 无 CLD 的婴儿的 37,213 美元/公顷,再到患有 CLD 的早产儿 (29-31 wGA) 的 193,859 美元/公顷脚注200.
V.1.3 以其他比率表示结果的经济评价
对加拿大西部患有 CHD 的足月儿的经济评估发现,从社会角度来看,基本情况 ICER 为每避免住院一天 18,155 美元脚注148.一项针对法国早产儿 (< 32 wGA) 或患有 CLD 或显著 CHD 的研究发现,从社会角度来看,CLD 早产儿和患有 CHD 的早产儿的基本 ICER 分别为增加 43,856 美元/生命年 (LY) 和 33,450 美元/LY。从付款人的角度来看,患有 CLD 的婴儿的 ICER 为 16,368 美元/LY脚注202.在一项针对美国患有 CLD 的早产儿的研究中,该模型使用了 RSV 感染发生率的降低,从付款人的角度来看,从减少 50%(每次避免 RSV 感染事件 66,494 美元)到 83%(PVZ 预防是一种主要策略,即成本更低且更有效)脚注178.
V.1.4 加拿大环境中的经济评估
在加拿大进行了五次经济评估脚注148 脚注186 脚注189 脚注196 脚注197.研究的人群是来自加拿大北极的足月婴儿脚注196 脚注197、 早产儿脚注186、 CF 婴儿脚注189和患有 CHD 的婴儿脚注148.这些研究假设每个 RSV 季节服用 4.5 至 6 剂 PVZ,每 100 毫克 PVZ 的成本为 1,599 至 1,718 美元(2017 加元)。在上述研究中,PVZ 的有效性是通过降低 RSVH 来衡量的,RSVH 在 42% 到 96% 之间。死亡率被纳入两个模型,分别为 1% 和 8.1%脚注186 脚注196.后遗症被纳入两个模型 (一个 RSV 感染后遗症,另一个与 CF 相关的后遗症)脚注186 脚注189.在五项加拿大研究中,对成本效益结局影响最大的参数是: RSVH 率脚注196 脚注197、PVZ 的成本脚注148 脚注189和住院费用脚注196 脚注197,其中包括住院医疗费用和前往医疗中心的交通费用。
在加拿大北极地区,PVZ 预防被认为对某些婴儿亚组具有成本效益,因为 PVZ 可以防止与运输费用相关的高住院费用。对于基线 RSVH 率高的地区尤其如此。从付款人的角度来看,对于<所有 1 岁 (46,151 美元/QALY) 或 <6 个月大 (11,925 美元/QALY)、农村地区所有 1 <足月婴儿 (28,965 美元/QALY)、高风险农村地区 < 1 岁婴儿 (391 美元/QALY) 的常用阈值下,PVZ 可以被认为是具有成本效益的, 以及农村地区或高危农村地区 < 6 个月大的婴儿(占主导地位)。然而,对于居住在伊卡卢伊特的 1 < 岁(178,057 美元/QALY)或 <6 个月大(120,817 美元/QALY)的婴儿来说,这并不划算脚注196.ICER 在该市并不具有成本效益,因为 PVZ 无法防止与 RSVH 相关的运输成本。从社会角度来看,ICER 略低,但遵循类似的趋势。Banerji 等人包括来自八个北极地区的足月婴儿:西北地区、努纳武特地区、没有伊卡卢伊特的努纳武特地区、努纳武特地区的三个子区域(Kitikmeot、Kivalliq 和 Qikiqtaaluk)、没有伊卡卢伊特的 Qikiqtaaluk 地区和努纳维克(魁北克北部);以及在两个不同情况下每个 HA 报告的成本:预防至 RSV 季节结束(情景 A)和预防至 5 个月大(情景 B)。PVZ 预防是 Kitikmeot(情景 A 和 B)和 Kivalliq(情景 B)的主要策略(即成本更低且更有效);Kivalliq 为 24,981 美元/公顷(情景 A);努纳武特地区 5,042 美元/公顷(情景 B)和 31,104 美元/公顷(情景 A),没有伊卡卢伊特;努纳武特地区 15,829 美元/公顷(情景 B)和 45,060 美元/公顷(情景 A);16,979 美元/公顷(情景 B) 努纳维克为 32,899 美元/公顷(情景 A)。在所有其他地区,ICER 都超过 100,000 美元/HA脚注197.不同地区的 ICER 差异很大。在 RSVH 率较高的地区(范围:努纳维克、Kivalliq 地区、Kitikmeot 地区和努纳武特地区每 1,000 人中有 97.8 至 296.1 名 RSV 入院),PVZ 在 RSVH 率较低的地区(范围:西北地区和 Qikiqtaaluk 地区每 1,000 人中有 1,000 名 RSV 入院人数为 16.6 至 49.4 人),PVZ 往往不具有成本效益,阈值为 100,000 美元/QALY)脚注197.
从付款人的角度来看,在 32-35 周 GA 早产儿的常用阈值下,PVZ 被认为具有成本效益(20,814 美元/QALY,包括 RSV 感染导致的哮喘和 35,119 美元/QALY,不包括哮喘)。使用两组风险因素评分,得分高(高风险)的婴儿的 ICER 为 251 美元/QALY 和 5,906 美元/QALY,中等得分的婴儿为 29,901 美元/QALY 和 38,566 美元/QALY>,得分较低或无风险因素的 ICER 为 50,000 美元/QALY(92,649 美元 – 919,073 美元)脚注186.对于年龄小于 24 个月的 CF 婴儿,从付款人的角度来看,PVZ 被确定不太可能具有成本效益(所有婴儿为 693,105 美元/QALY,高危婴儿为 167,107 美元/QALY)脚注189.在对 24 个月大的 CHD 儿童< PVZ 成本效益的研究中,从社会角度来看,ICER 避免了 18,155 美元/天的住院治疗,并且被认为不太可能具有成本效益脚注148.
后三项研究可能适用于加拿大大多数省份,因为它们使用的 PVZ 成本(每 100 毫克小瓶 1,468 美元 – 1,505 美元,原始成本)与加拿大其他省份相似,给药方案接近每季 5 次注射(每季 4.5 至 5.39 瓶),不列颠哥伦比亚省和安大略省的医疗保健成本,并包括与加拿大医疗保健系统相关的模型参数。缺乏对加拿大较小省份(如滨海省份)婴儿 PVZ 预防的成本效益的研究。
| 作者, 年份 | 人口 | 剂量 (每季) | 单件商品成本(未盘点) | 住院 | 死亡率 | 包括 RSV 后遗症? | ||
|---|---|---|---|---|---|---|---|---|
| PVZ | 无 PVZ | 减少 (%) | ||||||
| Tamet al., 2009 年脚注196 | 巴芬岛足月婴儿 | 5 剂 | 样品瓶单位成本:NR; 每公斤婴儿 220 美元 | 1.4 – 11.4% | 6.3 – 51.2% | 78%表 8 脚注一个 | 1% (两组) | 否 |
| Banerji et al., 2016脚注23 | 加拿大北极 足月婴儿 | 6 剂(最大剂量) | 样品瓶单位成本:NR;婴儿 $226/公斤 | NR | NR | 96% | NR | 否 |
| Smartet al., 2010 年脚注186 | 早产儿 32-35 wGA | 5.39 样品瓶 | 50毫克: $752100 毫克: $1,505 | 1.8% | 10.0% | NR (82% 回溯计算) | 3.9% (两组)表 8 脚注b | 是 / 否 (哮喘) |
| McGirr et al., 2017脚注189 | 囊性纤维化年龄 <24 个月 | 5 剂 | 100 毫克: $1,505 | 1.7%(假设减少 55%)表 8 脚注c | 3.8% | 55% | NR (使用 CF 相关死亡) | 是(囊性纤维化进展) |
| Harris et al., 2011脚注148 | CHD 年龄 <24 个月 | 4.5 剂 | 100 毫克: $1,468 | 1.7% | 2.9% | NR (42% 回溯计算) | NR 0.2%(1/41,无 PVZ); 0%(0/292,PVZ) | 不 |
NR:未报告 | ||||||||
V.1.5 结果的异质性:关键参数
影响 ICER 的最常见报告的影响参数是 RSVH 率和所用 PVZ 的成本。RSVH 的减少在 39% 到 96% 之间差异很大,具体取决于感兴趣的人群和数据来源。一瓶 100 毫克 PVZ 的成本也在 1,099 美元到 2,198 美元(2017 加元)之间。然而,西林瓶的使用和剂量方案仅影响了 4 个脚注181 脚注183 脚注195 脚注200和 3 项研究脚注185 脚注187 脚注200分别。在解决药物浪费的研究中,ICER 波动高达 50%,具体取决于假设的样品瓶使用情况。在新西兰的一项研究中,假设不共享样品瓶(每次注射使用整个 100 mg 样品瓶),每箱成本最多可增加 50%(即性价比更差)脚注200,而西班牙的另一项研究得出结论,当使用 50 毫克小瓶而不是 100 毫克小瓶时,ICER 较低(即物有所值)脚注183.文献中表明,PVZ 可以实现样品瓶使用效率脚注203.贴现也经常被报道为对 ICER 有影响。折扣率因研究而异 (3-5%)。目前,加拿大指南建议成本和结果的贴现率为 1.5%脚注204.
V.1.6 纳入研究对加拿大背景的普遍性
大多数研究结果可能可以广泛推广到加拿大医疗保健系统,因为这些是在医疗保健成分与加拿大相似的经合组织国家进行的经济评估脚注205.唯一的例外是来自美国的 6 项研究。支付方或社会观点的选择可能会影响分析中包含的成本和收益。在使用社会视角的研究中,考虑了医疗保健系统之外的以下成本:哮喘导致的工作时间损失;院内感染的间接成本;差旅费用(即酒店、交通);生产力损失(即照顾、闲暇、儿童的未来生产力);和旷课。
根据加拿大的三项研究,模型中使用的每 100 毫克小瓶 PVZ 的成本在 1,599 美元至 1,718 美元(2017 加元)之间。来自英国的型号使用的 PVZ 成本较低,每 100 毫克小瓶为 1,099 至 1,240 美元,其余研究(来自美国的研究除外)的成本在 1,386 美元至 2,035 美元(2017 加元)之间。每个季节的剂量在 3.88 到 6 剂之间。在与加拿大医疗保健结构相似的国家子集中,几乎所有模型都假设每个季节接种五剂 PVZ,但 Resch 等人(奥地利)除外脚注82、Nuijten 等人、Sanchez-Luna 等人和 Schmidt 等人(均来自西班牙),其中平均剂量为每季 4 剂脚注183 脚注185 脚注195.
尽管 PVZ 预防成本和剂量方案相似,但估计 RSVH 的降低率从 39% 到 96% 不等,具体取决于婴儿人群和参考文献。68% 的研究(S. Mac 个人通信,2019 年 6 月)将 IMPACT-RSV 试验用于他们的一些模型参数,该试验包括加拿大儿童,并得出结论,早产儿的 RSVH 降低 78%,CLD 儿童降低 39%,总体降低 55%。虽然该研究中加拿大受试者亚组显示 RSVH 总体降低 40%,但这一趋势与美国 (56%) 和英国受试者 (64%) 相似脚注48.值得注意的是,IMPACT-RSV 试验于 1996 年进行,随着早产儿、CLD 和 CHD 以及 RSV 感染管理的变化,基于该研究的模型参数在今天可能不合适。
V.2 魁北克省努纳维克的成本效益研究
除了系统评价中的研究外,2019 年 3 月 13 日向 NACI 报告了魁北克北部努纳维克地区成本效益研究的初步结果(R. Gilca,魁北克国家公共卫生研究所,个人通信,2020 年 11 月 18 日)脚注206.从 2016-17 赛季开始,在 RSV 季节开始时 <3 个月大或在 RSV 季节出生的健康足月婴儿有资格接种最多 3 剂 PVZ。在 2017-18 赛季,符合这些标准的婴儿有资格接种最多 5 剂疫苗。目标是估计目标人群中 RSVH 的医疗保健成本和 PVZ 计划的成本,并估计避免的每次住院成本。
以下分析基于该计划的前 2 年。它正在更新以包括 4 年的数据,并将发布。结论保持不变。
| 日期 | 每 100 000 个患者天的 RSVH 发生率 | 有效性表 9 脚注* | |
|---|---|---|---|
| 保护 | PVZ – 受保护 | ||
| 2017 | |||
| 1 月 1 日至 4 月 30 日 | 58.1 | 37.5 | 35.5% |
| 1 月 1 日至 5 月 31 日 | 45.5 | 33.8 | 25.7% |
| 2018 | |||
| 1 月 1 日至 5 月 31 日 | 22.5 | 14.5 | 35.6% |
| 1 月 1 日至 6 月 30 日 | 17.8 | 13.0 | 27.3% |
| |||
| 情景/假设 | 避免的成本: (2014-2016 年无项目 的平均成本 = 156,914 美元) | 2017 | 2018 | ||||
|---|---|---|---|---|---|---|---|
| 项目总费用 | 支出/避免的比率 | 投资回报率 | 项目总费用 | 花费 / 避免的比率 | 投资回报率 | ||
| 1. PVZ 有效性 = 36%脚注*;成本降低与效果成正比 | 55,861 美元 | 291,533 美元 | 5 | 0.19 | 369,641 元 | 7 | 0.15 |
| 2. 2017 年观察到的所有减少都是由于 PVZ (减少 = 89%)脚注** | 139,395 元 | 291,533 美元 | 2 | 0.48 | 369,641 元 | 3 | 0.38 |
| 3. 2018 年观察到的所有减少都是由于 PVZ (减少 = 71%)脚注** | 112,040 元 | 291,533 美元 | 3 | 0.38 | 369,641 元 | 3 | 0.30 |
ROI:投资回报率 | |||||||
该计划的费用远远超过住院和交通费用。为了实现成本中立,该计划每年需要防止 9 到 11 次住院治疗(计划总成本 / 2014-2016 年每次住院的平均费用 = 33,600 美元)。在该人群中尚未观察到如此高的住院人数(2014-2016 年的平均住院人数 = 7 次住院)
这项研究有几个局限性,包括人口规模小,每年大约 220 名健康足月婴儿在 10 月 1 日至 6 月 30 日之间出生,并且分散在许多非常小的社区。来自 Nunavik 的健康足月 0-2 个月大婴儿的住院人数较低(低于先前的预期),并且每年变化很大。因此,住院和运输的总费用也变化很大。该计划的费用每年都相似。PVZ 的成本是主要组成部分,但管理成本也不容忽视(>135 美元/剂)。PVZ 预防 RSVH 的有效性较低。许多住院婴儿与其他病毒合并感染。还存在社会接受度和对 PVZ 计划的合规性问题。
道德、一般、可行性和可接受性 (EEFA) 注意事项
同行评审的 EEFA 框架脚注13应用于本指南,以确保系统考虑对全面免疫规划决策和成功实施建议至关重要的因素。使用该 EEFA 框架使委员会能够审查和平衡所有可用证据,并透明地总结其理由,以便提出适当、及时的建议。与该框架相关的循证工具(道德综合过滤器、一般矩阵、可行性矩阵、可接受性矩阵)确保与专家委员会指导的 EEFA 相关的问题得到系统和充分的整合。
道德注意事项
为了支持道德审议和决策,NACI 针对核心道德维度(尊重个人和社区、仁慈和非恶意、正义、信任)和程序道德维度(问责制、包容性、责任感、响应性、透明度)应用了道德综合过滤器。NACI 遵循其既定的方法、标准作程序 (SOP) 和利益冲突指南,以确保对证据进行稳健分析,对已知和未知因素保持透明,并维护利益相关者的信任。为了尊重行使知情选择权,NACI 审查了针对有 RSV 风险的婴儿和儿童群体的最佳、当前证据,并在本指南文件中为利益相关者进行了总结,包括关于 RSV 疾病引起的疾病负担的最新数据、PVZ 对有更严重 RSV 疾病风险的婴儿的疗效和有效性以及 PVZ 使用的经济影响。NACI 在审议中还考虑了将伤害风险降至最低和使所有潜在关键人群受益最大化的证据。鉴于确定了对证据可用性的一些潜在担忧,应谨慎解释这些发现;针对某些风险群体和情况确定了大量文章,并且使用的方法和研究的结局存在显著异质性。此外,由于没有证据表明 RSV 降低了死亡率或从 PVZ 获得了长期益处,如果这些其他干预措施可能会因提供 PVZ 计划而受到损害,则 PVZ 预防计划的高成本也必须与其他医疗保健干预措施的成本相平衡。因此,NACI 将继续监测与不同群体使用 PVZ 相关的证据,包括 PVZ 计划和替代剂量方案的成本效益以及可能更具成本效益的新产品,并将根据需要更新声明及其建议。
一般性考虑因素
NACI 审查了 RSV 的流行病学和关于与加拿大相当的高收入国家幼儿 RSV 疾病负担的系统评价结果(在第 III 节中总结),以确定与 COVID-19 相关的明显不平等、这些不平等的潜在原因,并建议干预措施以减少不平等和改善疫苗的可及性疫苗可用。
严重 RSV 疾病的风险受出生胎龄、潜在健康状况和年龄的影响。由于向所有 RSV 疾病风险增加的婴儿提供 PVZ 预防是不可行的,因此原则上应将其提供给具有同等严重疾病风险的高风险人群。对于可识别的高危婴儿和儿童亚组,需要对选择性 PVZ 预防提出具体建议,这些婴儿和儿童亚组比其他人更容易受到 RSV 感染的不利影响,他们的严重结局风险在相似范围内,并且 PVZ 预防已被证明对他们有效。然而,可用数据的有限性和异质性使得对风险程度的评估有些武断。对于某些非常罕见的情况,严重 RSV 疾病的风险可能很高,但没有流行病学数据,并且患有某些罕见疾病的儿童数量可能不足以研究 PVZ 的有效性。在这些情况下,可以根据病理生理学相似性与记录的 RSV 风险增加以及 PVZ 已被证明有效的情况的数据进行推断。在大多数省份和地区,医生可能会破例要求不符合 PVZ 特定标准的儿童进行 PVZ。虽然这允许灵活地用于患有罕见疾病的儿童,但它也可能带来不平等。提出例外请求的人和评估这些请求的人必须一般地这样做,以避免不一般。
生活在偏远的北部因纽特社区和其他偏远农村社区的婴儿也可能面临因 RSV 感染而导致严重后果的风险增加。当地获得医疗服务的机会有限,可能需要医疗后送,需要空运到医院设施。因此,可能需要额外的资源来提供 PVZ 预防以及监测和随访生活在偏远地区的婴儿。PVZ 预防也应尽可能在家附近提供,因为如果家庭必须长途跋涉接受 PVZ 和/或请假进行这些访问,那么短时间内就诊的次数和频率以及严格的注射间隔可能会成为家庭的障碍,因为自付费用。在这些情况下,可能需要向一些家庭提供帮助,以便他们能够从 PVZ 预防计划中受益。NACI 将继续监测与患有既往疾病的婴儿以及生活在偏远北部因纽特人社区和其他偏远农村社区的婴儿的 RSV 疾病严重程度相关的证据。
可行性考虑
提供 PVZ 预防很复杂,由于给药方案和疾病的季节性,将其整合到现有的主动疫苗接种计划中是不可行的。特别是,需要在短时间内多次注射可能会带来调度挑战;在当地年度 RSV 爆发期间,必须每隔 28-35 天接种最多 4 剂。与疫苗不同,PVZ 剂量取决于体重和准确的就诊时间,PVZ 给药对于适当的保护至关重要,并且不可能将所有就诊与其他疫苗或常规儿童护理相结合。此外,PVZ 以多剂量小瓶形式提供,一旦打开,必须在 6 小时内使用,否则将被丢弃和浪费。在较小的社区中,样品瓶共享可能很困难,因为很少有儿童适合 PVZ,这进一步增加了成本。因此,实施新的 PVZ 预防计划的重要考虑因素包括将预防限制在严重结局风险最高的人群中,在 RSV 季节安排特定的 PVZ 诊所,认识到对现有当地计划的潜在影响,以及让当地护理人员参与计划实施的规划。
可接受性注意事项
目前可用的针对 PVZ 预防和高危婴儿的父母或监护人对 RSV 疾病的看法的可接受性数据非常有限。可接受性和依从性的可能障碍包括:
- 就诊的次数和频率,特别是如果家庭必须长途跋涉才能接受预防,并且无法将 PVZ 就诊与其他疫苗或常规医疗保健需求的就诊相结合。
- 如果预约需要长途前往治疗中心和离开工作地点,则自付费用。
- 缺乏对高危儿童 RSV 感染风险的了解。
有一些证据表明,加拿大的原住民人口比非原住民人口面临更高的不遵守风险,而偏远的北方人口的接受度较低脚注207 脚注208.在加拿大北部与人群一起工作的护士和助产士也对缺乏有关 PVZ 对健康足月婴儿的有效性和安全性的数据表示担忧脚注207.家庭对 PVZ 预防的低接受度可能导致对 PVZ 计划的依从性降低并降低有效性脚注209.因此,新计划的实施应包括对当地医疗保健提供者、需要 PVZ 的婴儿的家庭和监护人的持续教育,以及他们积极参与干预计划。在可行的情况下,在离家尽可能近的当地诊所提供 PVZ,并有足够的资源为可能需要一些额外支持才能前往诊所的家庭提供帮助,这也是重要的考虑因素。
建议
在对上述总结的现有证据进行全面审查,并使用同行评审的 EEFA 框架对道德、一般、可行性和可接受性考虑因素进行系统评估之后,NACI 提出了以下循证建议。
对公共卫生项目层面决策的建议
(即省份/地区为公共资助的免疫接种计划做出决定)
在考虑这些建议以及出于公共资助计划实施的目的,各省和地区可以考虑当地的计划因素(例如,当前的计划、资源)。认识到加拿大各地的运营环境存在差异,如果需要优先实施有针对性的免疫计划,各辖区可能希望参考下面的管理选项表,了解为不同高危人群接种疫苗的相对优势摘要。
1. 无 CHD 或 CLD 的早产儿:
建议 1.1:NACI 建议,在 RSV 季节开始时或期间,应为妊娠 30 周 0 <出生且年龄< 6 个月的婴儿提供 PVZ。(强烈推荐 NACI)
NACI 得出结论,有一般的证据推荐在该人群中使用 PVZ(B 级证据)。
建议 1.2:NACI 建议,对于 30 至 32 周、妊娠 6 天、< 3 个月的婴儿,如果他们因日托所就诊或家中有其他学龄前儿童或儿童而处于 RSV 暴露的高风险,则可以考虑对 30 至 32 周、妊娠 6 天至 3 个月的婴儿进行 PVZ。(酌情 NACI 建议)
NACI 得出结论,没有足够的证据推荐在该人群中使用 PVZ(I 级证据)。因此,此建议基于专家意见。
建议 1.3:NACI 建议不应向妊娠 33 周 0 天或之后出生的其他方面健康的婴儿提供 PVZ(强烈 NACI 建议)
NACI 得出结论,有一般的证据建议反对在该人群中使用 PVZ(C 级证据)。
证据和理由总结:
- 有充分的证据表明,胎龄较小的早产儿患 RSVH 的风险更高,据报道,28 岁或 29 << 岁早产儿在出生后第一年的发生率为 7.7% 至 13.6%脚注41 脚注42 脚注43 脚注44 脚注45 脚注46 脚注47.这些婴儿接受很少或没有母体抗体,他们较窄的气道通道增加了他们对 RSV 感染影响的脆弱性。
- 有充分的证据表明,与足月婴儿相比,30-32 wGA 婴儿患 RSVH 的风险也更高,但住院率较低,在 2014-2018 年出版物的系统评价 (BODsr) 中为 5.1(见第 III.1.1 节),早期文献中为 5.7 – 9.9%脚注41 脚注42 脚注43 脚注45 脚注46在最近的一项研究中为 4.3%脚注38.有充分的证据表明,29-32 岁和 33-35 wGA 婴儿的 RSVH 发生率分别是足月儿的 4.6 倍和 2.8 倍(第 III.1.1 节)。早期研究表明,关于 32-35 wGA 婴儿发生 RSVH 风险的证据不一致。据报道,出生后第一年或第一个 RSV 季节的发病率为 2.85% 至 6.5%脚注40 脚注45 脚注48,而最近的两项研究报告的比率分别为 4.0% 和 3.4%脚注38 脚注39.BODsr 中健康足月婴儿的 RSVH 率为 1.2%。
- 有公正的证据表明,因 RSV 住院的早产儿的 LOS 比足月儿长,早产儿和足月儿之间的 LOS 平均差异为 29-32 wGA 婴儿的 7.97 天和 32/33-35 wGA 的婴儿的 1.06 天。有充分的证据表明,患有 RSVH 的早产儿的 ICU 入住率高于足月儿,29-32 wGA 婴儿的 RR 为 4.0,32-35 wGA 的 RR 为 3.0。有充分的证据表明,患有 RSVH 的 29-35 wGA 早产儿的 MV 发生率高于足月儿,29-32 wGA 婴儿的 RR 为 1.9,33-35 wGA 的 RR 为 1.2。(第 III.1.1 节)
- 有充分的证据表明,实际年龄是 RSVH 的一个重要危险因素,大多数感染发生在出生后的前 2-3 个月脚注16 脚注49.
- 没有足够的证据表明 PVZ 在降低 < wGA 出生的早产儿 RSVH 风险方面的有效性。三项研究,两项被评为良好,一项被评为一般,未显示对该组的 RSVH 有显著影响,但受试者人数很少(三项研究共 228 名)。一项针对 ≤30 wGA 出生的早产儿的更大型研究被评为质量差,结果显示 NNT 为 9 时,早产儿减少了 92%。
- 有充分的证据表明,PVZ 可有效将无 CLD 或 hsCHD 的 ≤32 wGA 早产儿的 RSVH 率降低 38-80% (NNT 53, 5, 17)。
- 关于 PVZ 对 32-35 wGA 出生且无 CLD 或 hsCHD 的早产儿 RSVH 发生率的影响,存在相互矛盾的证据。两项 RCT 和一项观察性研究显示降低 55-82% (NNT 22、24) 和 55%,而 3 项观察性研究未显示显着影响。
- 有一般的证据(一项系统评价)表明 PVZ 接受与 32 wGA ≤出生婴儿的全因死亡率降低之间存在关联,但没有证据表明 PVZ 对 RSV 特异性死亡率有影响脚注74.
- 在 82% 的估计值中(支付者角度),早产儿的 ICER <每 QALY 50,000 美元,并且在 < 32 wGA 的婴儿中占主导地位(即成本更低、更有效)(社会角度)。在 wGA 阈值和 ICER 之间没有检测到特定趋势,但 wGA 组中的估计数量很少。在 100% 的估计中,ICER < 29 wGA 为 <50,000 美元/QALY,29-32 wGA 为 67%,<32 wGA 为 100%,< 33 wGA 为 100%,32-35 wGA 为 67%(付款人视角)。在一项加拿大研究中,对于具有高或中度 RSV 风险评分的 32-35 wGA 婴儿(付款人角度),ICER <每 QALY 50,000 美元。
- 尽管 30-35 wGA 婴儿的疾病负担高于足月婴儿,并且有充分的证据表明 PVZ 对 30-32 wGA 婴儿的有效性,但这些年龄较大的胎龄儿使用 PVZ 的成本令人担忧。在加拿大,估计有 8% 的婴儿是早产儿脚注67,并且 5% 的出生队列可能在 32-35 wGA 时出生脚注34.建议基于为风险最高的早产儿提供预防。
建议 1.4:NACI 建议不应向不符合预防条件的婴儿或多胞胎兄弟姐妹提供 PVZ。(强烈推荐 NACI)
NACI 得出结论,有一般的证据建议反对在该人群中使用 PVZ(C 级证据)。
证据和理由总结:
- 大多数关于双胞胎和其他多胞胎的研究报告了多胞胎和单胎婴儿发生 RSVH 的类似风险,要么没有脚注71 脚注116或之后脚注114 脚注117对混杂因素进行调整。
- 一项研究报告了多胞胎婴儿的 RSVH 发生率较高,但未考虑潜在的混杂因素脚注115.
- 此组中没有有关 PVZ 使用情况的数据。
- 证据基于对关键研究的回顾,没有正式的质量评估。
2. 早产儿慢性肺病和其他慢性肺病
建议 2.1:NACI 建议应向患有慢性早产儿肺病的婴儿(定义为出生时 ≤32 wGA 并需要补充 O2>出生后至少 21 天的前 28%)在 RSV 季节开始时 <24 个月大并且需要持续的补充 O2在 RSV 季节开始前或期间的 6 个月内进行治疗。(强烈推荐 NACI)
NACI 得出结论,有充分的证据推荐在该人群中使用 PVZ(A 级证据)。
证据和理由总结:
- 早产儿 CLD 婴儿在出生后前 2 年的 RSVH 率较高 (12-21%)脚注42 脚注44 脚注48 脚注72.对于住院患者,据报道 ICU 入住率 (29%) 和 MV (24%) 率很高脚注72.
- 有充分的证据表明,PVZ 可降低 ≤ 35 wGA 且 CLD 年龄< 24 m 婴儿的 RSVH (RD 39%, NNT 21)脚注48.有公正的证据表明,PVZ 可降低 CLD 婴儿初次出院后前 6 个月的 RSVH 发生率 (RD 86% NNT13)脚注44在 RSV 季节开始时年龄< 6 m 的 CLD 婴儿中证据不佳 (RD 85%, 72%;NNT 3, 8)脚注46 脚注139.没有足够的证据表明 PVZ 对 < 12 个月或 6-12 个月的 CLD 婴儿的影响。没有证据表明 PVZ 对 CLD 婴儿的其他住院相关结局或 RSV 长期后遗症的影响。没有足够的证据表明 PVZ 对 CLD 患儿的全因死亡率或 RSV 相关死亡率有影响,因为研究的数字不足以检测影响脚注74.
- 关于 PVZ 预防成本效益的研究报告称,在所有估计中(付款人或社会角度),每个 QALY 的 ICER < 50,000 美元;对于吸氧出院回家的婴儿,每次住院避免的 ICER < 50,000 美元,每生命年增加 < 50,000 美元。
建议 2.2:NACI 建议 24 个月大患有其他病因的严重慢性肺病<儿童可以考虑使用 PVZ(例如 先天性囊性肺病、慢性间质性肺病、先天性肺畸形、先天性气道异常或影响气道分泌物清除能力的神经肌肉疾病)或需要家庭呼吸支持(例如 补充 O2、机械通气、持续气道正压通气、气管切开术)如果需要持续的补充 O2或在 RSV 季节开始前或期间的 6 个月内进行辅助通气。(酌情 NACI 建议)
NACI 得出结论,没有足够的证据推荐在该人群中使用 PVZ(I 级证据)。因此,此建议基于专家意见。
证据和理由总结:
- 有充分的证据表明,患有非早产儿病因的慢性肺病的婴儿 RSVH 发生率增加(先天性囊性肺病 8.3%,慢性间质性肺病 30%,先天性肺和气道畸形 8.3-13.7%,以及一些影响气道分泌物清除能力的神经肌肉疾病 9.9-15.9%v脚注21 脚注75 脚注76.
- 没有证据表明在这些情况下 PVZ 对 RSV 疾病的影响。
- 据推测,患有严重程度与早产儿 CLD 相当的 CLD 婴儿可能受益于 PVZ。
3. 囊性纤维化:
建议 3.1:NACI 建议不应常规向 24 个月大的囊性纤维化儿童<提供 PVZ。(强烈推荐 NACI)
NACI 得出结论,有一般的证据建议反对在该人群中常规使用 PVZ(D 级证据)。
证据和理由总结:
- RSVH 在 CF 患儿中的发生率高于健康儿童。系统评价中的 RSVH 为 12.3%(第 III.1.3 节)。关于其他住院相关结局的数据有限。
- 关于对 CF 婴儿常规给药 PVZ 对 RSVH 的影响,证据不一致,除一项研究外,所有研究均显示没有效果脚注77 脚注78 脚注140 脚注142 脚注143 脚注144.
- 有充分的证据表明,对 CF 婴儿常规施用 PVZ 不会显着影响长期肺功能、生长或气道细菌定植脚注78 脚注140 脚注144 脚注145.
- 一项加拿大研究估计,对于囊性纤维化婴儿的常规 PVZ 预防,每个 QALY(付款人角度)的 ICER 超过 600,000 美元脚注189.
建议 3.2:NACI 建议 24 个月大的囊性纤维化儿童可以考虑使用 PVZ,这些<儿童患有严重的慢性肺病,定义为在 RSV 季节开始前或期间的 6 个月内需要持续的补充氧气。(酌情 NACI 建议)
NACI 得出结论,没有足够的证据推荐在该人群中使用。(I 级证据)。因此,此建议基于专家意见。
证据和理由总结:
- 没有证据表明婴儿期患有严重慢性肺病的 CF 婴儿亚组中 RSV 疾病负担。
- 没有证据表明 PVZ 预防对该亚组中 RSV 疾病的影响。
- 据推测,患有严重程度与早产儿 CLD 相当的 CF 肺病的婴儿可能受益于 PVZ。
4. 先天性心脏病和其他慢性心脏病:
建议 4.1:NACI 建议,在 RSV 季节开始时年龄在 1 <岁的血流动力学显著 CHD 婴儿(由儿科心脏病专家评估)应提供 PVZ。(强烈推荐 NACI)
NACI 得出结论,有充分的证据推荐在该人群中使用 PVZ(A 级证据)
证据和理由总结:
- 有充分的证据表明,< 24 个月大的 hsCHD 儿童患 RSVH 的风险增加,据报道发生率为 2.3-10.2%脚注65 脚注79 脚注80.
- 有充分的证据表明,冠心病婴儿在出生后第一年的 RSVH 发生率明显高于第二年脚注43 脚注79 脚注81.
- 有充分的证据表明,PVZ 可降低 24 个月< hsCHD 儿童发生 RSVH 的风险 (RD 45%,NNT 23)脚注80.有充分的证据表明,PVZ 可降低 6 个月< hsCHD 儿童患 RSVH 的风险 (RD 51%, NNT 16),也有 <12 个月儿童的一般证据 (RD 49%-72%, NNT 45, 7)脚注44 脚注80 脚注147.有充分的证据表明,PVZ 减少了 hsCHD 儿童因 RSV 住院的总天数脚注80但不是 RSV 入院患者的 LOS脚注80 脚注146,并且有充分的证据表明 PVZ 不会影响入住 ICU 的住院儿童比例、ICU 住院时间或需要 MV 的比例脚注80 脚注146 脚注148.关于 PVZ 对 hsCHD 患儿全因死亡率或 RSV 死亡率的影响,证据不足脚注80 脚注148.
- 关于 PVZ 预防成本效益的研究报告称,在 80% 的估计值(付款人角度)和 63% 的估计值(社会角度)中,ICER 为 <50,000 美元/QALY。在加拿大的一项研究中,估计每天避免住院治疗的 ICER 为 18,155 美元脚注148.
建议 4.2:NACI 建议,对于 RSV 季节开始时患有其他病因的血流动力学显着慢性心脏病(由儿科心脏病专家评估)的 1 < 岁婴儿,可以考虑使用 PVZ。(酌情 NACI 建议)
NACI 得出结论,没有足够的证据推荐在该人群中使用 PVZ(I 级证据)。因此,此建议基于专家意见。
证据和理由总结:
- 没有证据表明该群体中有 RSV 疾病的负担或使用 PVZ。
- 据推测,严重程度与血流动力学显著 CHD 儿童相似的心功能不全婴儿可能受益于 PVZ。
建议 4.3:NACI 建议,如果 12-24 个月大的儿童正在等待心脏移植或在过去 6 个月内接受过心脏移植,则可以考虑在 RSV 季节开始时使用 PVZ。(酌情 NACI 建议)
NACI 得出结论,没有足够的证据推荐在该人群中使用 PVZ(I 级证据)。因此,此建议基于专家意见。
证据和理由总结:
- 没有证据表明该群体中有 RSV 疾病的负担或使用 PVZ。
- 据推测,这些婴儿将患有严重的心功能不全,并且可能会在 RSV 季节接受免疫抑制治疗,并且他们可能会从 PVZ 中受益。
建议 4.4:NACI 建议,对于同时患有血流动力学显著的 CHD 和慢性肺病的儿童,应遵循慢性肺病(上述)的建议。(强烈推荐 NACI)
NACI 得出结论,没有足够的证据支持针对该人群的建议(I 级证据)
证据和理由总结:
- 没有关于 RSV 疾病负担或 PVZ 对该组有效性的数据。
- 慢性肺病可能需要预防第二个 RSV 季节,而单独的 hsCHD 通常不需要。
5. 唐氏综合症:
建议 5.1:NACI 建议不应常规向 24 个月大的唐氏综合征儿童<提供 PVZ。(强烈推荐 NACI)
NACI 得出结论,有一般的证据建议反对在该人群中常规使用 PVZ(D 级证据)。
证据和理由总结:
- RSVH 在没有 hsCHD、CLD 或早产儿的唐氏综合征儿童中比健康儿童更常见。关于其他住院相关结局的数据有限脚注22 脚注83.
- 对患有唐氏综合征且无 hsCHD、CLD 或早产儿的婴儿进行 PVZ 预防的三项研究显示,对 RSVH 没有影响脚注149 脚注150 脚注151.
建议 5.2:NACI 建议应向因 hsCHD、慢性肺病、早产儿或免疫缺陷而符合预防条件的唐氏综合症儿童提供 PVZ。(强烈推荐 NACI)
NACI 得出结论,有一般的证据推荐在该人群中使用 PVZ(B 级证据)。
证据和理由总结:
- 参见上文 hsCHD、慢性肺病、早产儿或免疫缺陷的证据。
- 一项研究发现,符合接受 PVZ 的标准标准的唐氏综合症婴儿的 RSVH 率降低脚注150.
6. 免疫功能低下的儿童:
建议 6.1:NACI 建议可以考虑对 <24 个月大的严重免疫功能低下的儿童进行 PVZ。(酌情 NACI 建议)
NACI 得出结论,没有足够的证据推荐在该人群中使用 PVZ(I 级证据)。因此,此建议基于专家意见。
证据和理由总结:
- 关于免疫功能低下儿童 RSV 疾病负担的基于人群的数据很少。据报道,患有原发性免疫缺陷 (21.3%) 和癌症 (8.4%) 的儿童 <24 个月大)的 RSVH 发生率增加脚注21.
- 有限的数据表明,≤24 个月大的儿童和绝对淋巴细胞计数为 < 100 / mm3 的儿童患严重 RSV 疾病的风险最高脚注85 脚注87 脚注88.
- 未发现评估免疫功能低下儿童 PVZ 预防有效性的研究。
7. 居住在偏远社区的儿童
建议 7.1:NACI 建议应向生活在偏远北部因纽特社区的 <36 wGA <和 6 个月大的儿童提供 PVZ,这些儿童需要航空运输住院治疗。(强烈推荐 NACI)
NACI 得出结论,有一般的证据推荐在该人群中使用 PVZ(B 级证据)。
证据和理由总结:
- 有充分的证据表明,生活在偏远的北部因纽特人社区的早产儿 RSVH 发生率非常高,经常需要空运到三级护理机构脚注23 脚注91 脚注92.
- 有低质量证据表明 PVZ 对因纽特早产儿 RSVH 发生率的有效性 (NNT 4, 2)脚注92 脚注152.
建议 7.2:NACI 建议不应常规向生活在偏远北部因纽特人社区的健康足月婴儿提供 PVZ。(强烈推荐 NACI)
- NACI 得出结论,没有足够的证据推荐在该人群中进行常规 PVZ 预防。(I 级证据)。因此,此建议基于专家意见。NACI 将继续监测证据的发展。
证据和理由总结:
- 此类社区的 RSVH 发病率因社区和年份而异脚注23 脚注90 脚注91 脚注92.
- 有一项质量一般的研究表明,PVZ 预防对生活在加拿大北部因纽特人人群中的健康足月婴儿的 RSVH 没有影响,所有 1 <婴儿的 RSVH 发生率为 5%脚注90.
- 一项关于生活在加拿大北部因纽特人人口中的健康足月婴儿中 PVZ 预防的定性研究确定了重要的可接受性和可行性问题脚注207.
建议 7.3:NACI 建议,对于 RSV 季节开始时或期间生活在偏远北部因纽特社区的 <6 个月大的健康足月婴儿,可以考虑进行 PVZ 预防,这些社区有记录的足月婴儿 RSV 住院率非常高。(酌情 NACI 建议)
- NACI 得出结论,没有足够的证据建议对生活在 RSV 住院率非常高的偏远北部因纽特人社区的健康足月婴儿使用 PVZ(I 级证据)。因此,该建议基于专家意见,并考虑到这些社区的疾病负担很高,以及如果需要住院或专门的门诊护理,需要航空运输。NACI 将继续监测证据的发展。
证据和理由总结:
- 生活在北部一些偏远的因纽特人社区的足月儿的 RSVH 发生率非常高,经常需要空运到三级护理机构脚注23 脚注91 脚注92.据报道,在一些偏远社区,RSVH 的发生率高达所有活产婴儿的 20% 至 50%。
- 没有关于生活在 RSVH 率非常高的偏远北部因纽特人社区的健康足月婴儿进行 PVZ 预防的研究。
- PVZ 预防成本效益的研究估计,居住在加拿大东部北极地区 RSV 住院率高的足月婴儿的 ICER 为 < 50,000 美元/QALY,而 PVZ 在其他选定社区占主导地位(即成本更低、更有效)。然而,这些估计使用了早产儿 PVZ 有效性的数据,而足月儿的有效性尚未确定脚注196.
- 一项关于生活在加拿大北部因纽特人人群中的健康足月婴儿中预防 PVZ 的定性研究确定了重大的可接受性和可行性挑战脚注207.
建议 7.4:NACI 建议,对于居住在其他偏远社区的 36 wGA << 6 个月大的婴儿,可以考虑使用 PVZ,这些社区的 RSV 住院率记录在案,需要航空运输住院治疗。(酌情 NACI 建议)
- NACI 得出结论,没有足够的证据推荐在该人群中使用 PVZ(I 级证据)。因此,此建议基于专家意见。
证据和理由总结:
- 关于生活在北美其他偏远土著社区的婴儿的 RSV 疾病负担的证据有限,也没有关于其他偏远社区婴儿的证据。
- 没有证据表明 PVZ 对这些社区的 RSV 疾病有影响。一项关于另一种 RSV 单克隆抗体 motavizumab 的研究报告称,居住在美国西南部保留地的健康足月美洲原住民婴儿患 RSVH 的风险相对降低了 87%脚注89.
8. 预防后续复发性喘息
建议 8.1:NACI 建议在没有其他适应症的情况下,不应使用 PVZ 来预防复发性喘息或哮喘。(强烈推荐 NACI)
- NACI 得出结论,没有足够的证据推荐使用 PVZ 来预防这一结局(I 级证据)。因此,此建议基于专家意见。
证据和理由总结:
- 目前尚不清楚婴儿期 RSV 是否易患哮喘,或者遗传易患哮喘的婴儿患严重 RSV 疾病的风险是否增加,需要在婴儿期发生 RSVH。
- 儿童期复发性喘息发生在婴儿期因 RSV 住院的健康足月婴儿中,其比例与婴儿期 RSVH 高危婴儿报告的比例相似脚注29.
- 尽管对 36 wGA 出生<婴儿施用 PVZ 对医生诊断的出生后前 1-6 年(NNT 3 至 15)复发性喘息有影响,但在不存在特应性家族史的情况下,PVZ 有效性的研究结果相互矛盾脚注111 脚注134 脚注135 脚注136 脚注137 脚注138.
- 没有关于早期接受 PVZ 对 7 岁以上儿童或成人后续喘息或哮喘影响的数据。
9. PVZ 在住院婴儿中的使用
建议 9.1:NACI 建议 PVZ 不应常规用于控制或预防新生儿重症监护室 (NICU) 或其他医院病房的 RSV 感染。(强烈推荐 NACI)
- NACI 得出结论,有一般的证据建议反对在该人群中使用 PVZ(D 级证据)。
证据和理由总结:
建议 9.2:NACI 建议,当控制 NICU 中 RSV 爆发的所有其他措施都失败时,可以考虑 PVZ 预防。(酌情 NACI 建议)
- NACI 得出结论,没有足够的证据推荐在这种情况下使用 PVZ(I 级证据)。因此,此建议基于专家意见。
证据和理由总结:
建议 9.3:NACI 建议符合 PVZ 预防条件并在 RSV 季节出院的婴儿应尽可能在出院回家前 48-72 小时接受第一剂,或在出院后立即接受。(强烈推荐 NACI)
- NACI 得出结论,没有足够的证据推荐在这种情况下使用 PVZ(I 级证据)。因此,此建议基于专家意见。
证据和理由总结:
- 出院前接种第一剂可避免在出院后立即前往医疗机构就诊,并可能提高依从性。
- 在医院,为避免为个别婴儿打开小瓶时浪费,可以协调给药至每周 3 次。
建议 9.4:NACI 建议,在季节早期开始 PVZ 预防并在到期剂量之日再次住院的婴儿应按计划接受该剂量,前提是收治机构能够在到期时提供 PVZ。(强烈推荐 NACI)
- NACI 得出结论,没有足够的证据推荐在这种情况下使用 PVZ(I 级证据)。因此,此建议基于专家意见。
证据和理由总结:
- 遵守孩子现有的 PVZ 时间表可以避免重新安排预约的需要,并可能提高依从性。
10. PVZ 剂量:
建议 10.1:NACI 建议 PVZ 应以 15 mg/kg 的剂量通过肌内注射给药。第一剂应在当前 RSV 季节开始时接种,由当地实验室数据或儿科住院数据确定。如果这些数据不能及时获得,则可以根据之前当地 RSV 季节的日期预先确定开始日期。第一剂和第二剂之间的间隔应为 21-28 天,后续剂量之间的间隔应为 28-35 天。(强烈推荐 NACI)
- NACI 得出结论,此 PVZ 时间表有一般的证据(B 级证据)。
证据和理由总结:
- 每 30 天 15 mg/kg 的剂量导致根据动物研究假设目标血清 PVZ 水平具有保护作用脚注162.
- 根据 19-27 天的 PVZ 半衰期和在第二次给药后观察到的 PVZ 积累,使用了更长的剂量间隔脚注48 脚注164 脚注166 脚注167.
- 证据基于对关键研究的回顾,没有正式的质量评估。
建议 10.2:NACI 建议最多应接种 4 剂,但以下情况除外:(强烈 NACI 建议)
- 如果儿童接受心脏搭桥手术,并且在手术后继续需要 PVZ,则应在搭桥手术后尽快给予剂量
- 如果儿童接受体外膜肺氧合并继续需要 PVZ,则应在手术结束时给予一剂
- 在偏远的北部地区,也可以考虑额外剂量,那里的 RSV 爆发可能比其他地方通常持续的时间更长
- NACI 得出结论,没有足够的证据来确定 PVZ 剂量的最佳数量(I 级证据)。因此,此建议基于专家意见。
证据和理由总结:
- 研究表明,4 剂足以在整个通常的 RSV 季节提供保护脚注166 脚注167 脚注168 脚注169.
- 一项针对接受心脏搭桥手术的儿童的研究报告称,搭桥手术后 PVZ 水平降低了 58%脚注80.假设体外膜肺氧合可能具有类似的效果脚注6.
- 可以通过以下方式实现剂量节省:
- 证据基于对关键研究的回顾,没有正式的质量评估。
建议 10.3:NACI 建议,如果儿童因 RSV 感染而住院,则应在本季节停止 PVZ。(强烈推荐 NACI)。NACI 得出结论,有一般的证据表明,在单个季节内反复出现严重 RSV 感染的情况很少见(B 级证据)。
证据和理由总结:
- 在同一季节第二次发作 RSVH 的报告率在所研究的队列中从 0% 到 1.0% 不等脚注80 脚注108 脚注109 脚注110 脚注111,除了 3.3 年一项非常小的研究中 1988% 的比率脚注107.
- 证据基于对关键研究的回顾,没有正式的质量评估。
个人层面决策的建议
(例如,希望预防 RSV 疾病的个人或希望为患有目前未包含在公共卫生计划中的疾病的个体患者提供预防 RSV 的建议的临床医生)。
PVZ 在加拿大不容易供私人购买,价格昂贵,而且私人保险计划可能会报销也可能不会报销费用。没有针对个人层面的决策提出具体建议。
上述建议可应用于公共卫生计划层面的决策。请参阅下面的管理选项表。
管理选项表
(公共卫生计划层面决策的建议)。
使用 PVZ 的各种选项以及决定哪些选项更可取将取决于下面列出的注意事项:
| 选项 | 考虑 | 决策点 |
|---|---|---|
| 有风险的群组: | PVZ 是一种单克隆抗体,可针对严重的 RSV 感染提供临时被动保护,是目前唯一可用的预防措施。 PVZ 仅在 24 个月大<儿童中进行了调查,这些儿童的潜在疾病使他们患严重 RSV 疾病的风险增加,不建议健康足月婴儿或 24 个月以上的个体使用。 | 流行病学 严重 RSV 疾病的风险受出生胎龄、潜在健康状况和年龄的影响。婴儿在第 1 个 RSV 季节患严重 RSV 疾病的风险最高,尤其是在 < 3 个月大时。
RSV 导致从冬季到早春的年度流行病
安全 PVZ 是安全的,除了短暂的局部反应外,几乎没有不良反应。在接种超过 2,000,000 剂 PVZ 后报告了两例过敏反应。 经济学: PVZ 成本高昂,预防计划的主要成本是产品本身。研究报告了广泛的 ICER,具体取决于人群、环境、基线住院率以及模型结构和研究设计。在选定的情景中,估计每 QALY 的 ICER 为 <50,000 美元,但在极少数情况下占主导地位(即成本更低且更有效)。 与疫苗不同,PVZ 剂量随体重而变化。一旦打开,小瓶必须在当天使用或丢弃。
由于没有证据表明 RSV 的死亡率降低或 PVZ 的长期益处,如果 PVZ 计划的提供可能会损害这些干预措施,则必须平衡 PVZ 预防的高成本与其他医疗保健干预措施的成本。 |
| 1. 其他方面健康的早产儿: | 与足月儿相比,健康的早产儿患严重 RSV 感染的风险增加。30 wGA <人群住院风险最高(7.7% 至 13%),但 29-32 岁和 33-35 wGA 人群的住院风险也有所增加(足月婴儿的 4.6 倍和 2-3 倍)。 在对 ≤32 wGA 婴儿的研究中,PVZ 可有效预防住院 (率降低 38-74%,不同研究中 NNT 为 9 至 54)。对于 32-35 岁的婴儿,据报道 NNT 为 12-14 的 wGA 率降低了 72-83%,但一些研究显示没有影响。针对 < 29 wGA 婴儿的研究未显示效果,但研究的人数非常小。 在加拿大,7.7-8% 的出生体重为 < 37 wGA,估计 5% 的出生体重为 32-35 wGA。 对其他方面健康的早产儿进行PVZ预防的成本效益研究报告称,ICERs从6,216美元/QALY到938,623美元/QALYs,随着胎龄的增加,ICERs呈增加的趋势。没有估计值占主导地位(即成本更低、效果更高),82% 的估计值显示 ICER 为 <50,000 美元/QALY。 | |
| 2. 患有早产儿慢性肺病或其他病因的儿童: PVZ 的使用可以根据慢性肺病的严重程度(例如 氧气依赖) | 早产儿 CLD 患儿因 RSV 住院的风险为 12-21%。PVZ 可有效预防住院治疗(出生后前 2 年的发病率降低 39% 和 NNT 21,86%,第一年 NNT 13)。 有数据表明其他病因的慢性肺病中 RSV 住院率增加,但尚未对 PVZ 进行调查。 有数据表明,患有囊性纤维化的儿童患 RSV 住院的风险增加,但迄今为止的研究表明,PVZ 没有保护作用。 慢性早产儿肺病儿童 PVZ 预防的成本效益报告称,ICER 从 4,786 美元/QALY 到 46,821 美元/QALY。没有估计是占主导地位的(即成本更低、更有效)。 | |
| 3. 血流动力学显著的 CHD 或其他病因的血流动力学显著的心脏病患儿: PVZ 的使用可以根据心功能不全的严重程度进行个体化 | 患有血流动力学显着的 CHD 的儿童因 RSV 住院的风险为 9.7%,几乎所有感染都发生在出生后的第一年。在大多数研究中,PVZ 可有效预防住院 (率降低 45-72%,NNT 7-45),尽管两项小型研究显示没有效果。 没有关于 RSV 疾病和 PVZ 在患有其他病因的血流动力学显着心脏病的儿童中使用 PVZ 的数据。 PVZ 预防对血流动力学显著的 CHD 儿童的成本效益报告的 ICER 从 11,668 美元/QALY 到 164,946 美元/QALY。没有估计占主导地位(即成本更低、更有效),80% 的估计显示成本< 50,000 美元/QALY。 | |
| 4. 唐氏综合症、免疫功能低下和其他慢性病 | 建议基于 PVZ 有效性和不同风险人群患严重 RSV 疾病的风险。对于某些非常罕见的情况,严重 RSV 疾病的风险可能很高,但没有流行病学数据。 同样,患有某些罕见疾病的儿童数量不足以研究 PVZ 的有效性。 在这些情况下,可以根据病理生理学相似性的数据进行推断,并记录的 RSV 和 PVZ 有效性风险增加。 未发现针对这些人群的 PVZ 预防成本效益的研究。 | |
| 5. PVZ 用于 <37 wGA 的早产儿或生活在偏远因纽特人社区的足月儿 足月儿使用 PVZ 可能基于当地 RSV 足月婴儿的住院率和前往遥远医院的交通费用 | 研究表明,生活在一些偏远因纽特人社区的儿童,包括足月婴儿,患 RSV 住院的风险很高。 有限的数据表明,PVZ 减少了生活在偏远因纽特社区的 <37 wGA 婴儿的 RSV 住院率(降低率 96%、66%、NNT 2,4)。 一项在 RSVH 基线发生率不是很高的地区为足月因纽特婴儿提供 PVZ 的研究显示没有效果。 加拿大的模型表明,足月儿的 PVZ 预防可能在基线 RSV 住院率非常高的偏远因纽特人社区占主导地位(即成本更低且更有效)。在 75% 的估计中,ICER 为 < 50,000 美元/QALY,但疗效基于对早产儿的研究 | |
| 6. 生活在其他偏远原住民或其他偏远社区的足月婴儿使用 PVZ 足月儿使用 PVZ 可能基于当地 RSV 足月婴儿的住院率和前往遥远医院的交通费用 | 有限的数据表明,RSV 住院率在其他孤立的土著社区可能会增加。没有来自加拿大的数据。 没有关于这些社区使用 PVZ 的数据。 |
研究重点
鼓励进行研究以解决以下悬而未决的问题:
- 保护的血清学相关性:
- 确定预防人类严重 RSV 感染所需的最低抗体水平并开发市售的 RSV 抗体检测将允许更明智地使用昂贵的单克隆抗体产品,因为许多婴儿会在出生后的第一年或第二年产生天然抗体。
- RSV 单克隆抗体对生活在偏远社区的婴儿的疗效/有效性,尤其是对远北地区的因纽特婴儿:
- 有(良好的)证据表明,远北地区的因纽特婴儿患有 RSV 疾病的负担很高,但关于 PVZ 在预防住院和空气转移需求方面的有效性的数据有限。
- 唐氏综合征婴儿 RSV 疾病的负担以及 RSV 单克隆抗体预防该人群住院的功效/有效性:
- 文献表明,没有公认的 PVZ 预防临床标准的唐氏综合征婴儿可能具有较高的 RSV 住院率。这种易感性的原因尚不清楚,但可能与该人群的免疫缺陷有关。关于使用患有唐氏综合症的 PVZ 婴儿的数据非常有限。
- RSV 单克隆抗体对 < 29 wGA 出生的其他方面健康的早产儿的疗效/有效性:
- 关于 PVZ 预防对 < 29 wGA 严重早产儿的疗效/有效性的研究未能显示保护作用,但研究的婴儿数量非常少。在现在建议对这些婴儿进行 PVZ 的国家无法进行此类研究。请注意,英国和瑞士不建议健康的早产儿使用 PVZ。
监控问题
流行病学:
- 开发一个包含每个省份和地区数据的 RSV 监测系统,类似于 FluWatch,可以提供及时的数据,以确定 RSV 单克隆抗体预防计划何时应该最有效地开始和结束。
- 免疫功能低下人群中严重 RSV 疾病负担的研究,按年龄组(特别是关注 2 ≤人群)和免疫抑制严重程度(特别关注抗体缺陷人群,因为这些人将来可能无法从 RSV 疫苗中受益,因此可能继续保证 RSV 单克隆被动预防)。
对单个研究进行排名、推荐强度、证据等级
| 水平 | 描述 |
|---|---|
| I | 来自随机对照试验的证据。 |
| II-1 | 来自无随机化的对照试验的证据。 |
| II-2 | 来自队列或病例对照分析研究的证据,最好来自多个使用疫苗功效临床结果测量的中心或研究小组。 |
| II-3 | 从有或没有干预的多个时间序列中获得的证据。不受控制的实验中的戏剧性结果(例如 1940 年代引入青霉素治疗的结果)也可以被视为此类证据。 |
| III | 受人尊敬的权威机构的意见,基于临床经验、描述性研究和病例报告,或专家委员会的报告。 |
| 质量评级 | 描述 |
|---|---|
| 好 | 满足所有设计特定标准的研究(包括荟萃分析或系统评价)表 12 脚注*井。 |
| 一般 | 一项研究(包括荟萃分析或系统评价)不符合(或不清楚是否满足)至少一项设计特定标准表 12 脚注*但没有已知的“致命缺陷”。 |
| 差 | 至少有一项针对设计的研究(包括荟萃分析或系统评价)表 12 脚注*“致命缺陷”,或较轻缺陷的累积,以至于研究结果被认为无法为建议提供信息。 |
| |
| naci 建议的强度 | 证据等级 |
|---|---|
| 基于不与证据强度无关的因素(例如 公共卫生需求) | 基于对证据主体的评估(如证据概要表表 1 中总结的,其中评估了单个研究的水平和质量) |
| 强烈 “应该/不应该提供”
| A – 推荐的良好证据 |
| B – 推荐一般的证据 | |
| C – 证据相互矛盾,但其他因素可能会影响决策 | |
| D – 建议反对的一般证据 | |
| E – 推荐反对的良好证据 | |
| I – 证据不足(质量或数量),但其他因素可能会影响决策 | |
| 酌情 “可以考虑”
| A – 推荐的良好证据 |
| B – 推荐一般的证据 | |
| C – 证据相互矛盾,但其他因素可能会影响决策 | |
| D – 建议反对的一般证据 | |
| E – 推荐反对的良好证据 | |
| I – 证据不足(质量或数量),但其他因素可能会影响决策 |
缩写列表
| 缩写 | 全称 |
|---|---|
| AAP | American Academy of Pediatrics(美国儿科学会) |
| AEs | Adverse events(不良事件) |
| AMSTAR | A Measurement Tool to Assess Systematic Reviews(系统评价评估工具) |
| ARCHE | Alberta Research Centre for Health Evidence(艾伯塔省健康证据研究中心) |
| BODsr | Burden of RSV disease in young children(幼儿呼吸道合胞病毒疾病负担) |
| BPD | Bronchopulmonary dysplasia(支气管肺发育不良) |
| CAD | Canadian dollars(加拿大元) |
| CCLD | Congenital cystic lung disease(先天性囊性肺病) |
| CF | Cystic fibrosis(囊性纤维化) |
| CHD | Congenital heart disease(先天性心脏病) |
| CHILD | Chronic interstitial lung disease(慢性间质性肺疾病) |
| CI | Confidence interval(置信区间) |
| CIG | Canadian Immunization Guide(加拿大免疫指南) |
| CLD | Chronic lung disease(慢性肺病) |
| COE | Certainty of evidence(证据确定性) |
| CPS | Canadian Paediatric Society(加拿大儿科学会) |
| EEFA | Ethics, equity, feasibility, and acceptability(伦理、一般性、可行性和可接受性) |
| FEV1 | Force Expiratory Volume in one minute(第一秒用力呼气量) |
| FVC | Forced Vital Capacity(用力肺活量) |
| GRADE | Grading of Recommendations Assessment, Development and Evaluation(推荐分级评估、制定与评价) |
| HA | Hospitalizations avoided(避免住院) |
| hsCHD | Hemodynamically significant congenital heart disease(血流动力学显著的先天性心脏病) |
| ICER | Incremental cost-effectiveness ratio(增量成本效益比) |
| IQR | Interquartile range(四分位距) |
| IRR | Incidence rate ratio(发病率比率) |
| LOS | Length of hospital stay(住院时间) |
| LY | Life year(生命年) |
| MEF | Maximum Expiratory Flow(最大呼气流量) |
| MV | Mechanical ventilation(机械通气) |
| NACI | National Advisory Committee on Immunization(国家免疫咨询委员会) |
| NICU | Neonatal intensive care (unit)(新生儿重症监护室) |
| NNT | Number needed to treat(需治疗人数) |
| NT | Neutralization titre(中和滴度) |
| NVK | Dutch Association for Pediatrics(荷兰儿科学会) |
| O2 | Oxygen(氧气) |
| OR | Odds ratio(优势比) |
| PHAC | Public Health Agency of Canada(加拿大公共卫生署) |
| PT | Provinces and territories(省和地区) |
| PVZ | Palivizumab(帕利珠单抗) |
| QALY | Quality-adjusted life year(质量调整生命年) |
| QUIPS | Quality in Prognosis Studies(预后研究质量) |
| RD | Risk difference(风险差异) |
| ROB | Risk of bias(偏倚风险) |
| RSV | Respiratory syncytial virus(呼吸道合胞病毒) |
| RSVH | RSV hospitalization(呼吸道合胞病毒感染住院) |
| SAE | Serious adverse event(严重不良事件) |
| SD | Standard deviation(标准差) |
| SENeo | Spanish Neonatology Society(西班牙新生儿学会) |
| SOP | Standard operating procedures(标准操作程序) |
| wGA | Weeks gestational age(孕周) |
致谢
本声明由以下人员编写:D Moore、A Sinilaite、R Stirling、MW Yeung 代表 NACI RSV 工作组并经 NACI 批准。
NACI 衷心感谢以下方面的贡献:P Doyon-Plourde、S Duschesne-Belanger、E Poirier、A House、SJ Ismail、A Sumner、C Tremblay、MC Tunis、V Mouajou Feujio、L Zhao、A Killikelly、N St-Pierre 以及阿尔伯塔省健康证据研究中心 (ARCHE) 的研究团队,包括 J Pillay、A Wingert 和 L Hartling
NACI RSV 工作组
成员:D Moore (主席), M Salvadori, V Dubey, J Papenburg, J Robinson
前成员:S 甘特, W 沃德里
PHAC 参与者:S Duschesne-Belanger、A Killikelly、R Pless、A Sinilaite、R Stirling、A Sumner、MC Tunis、MY Yeung 和 L Zhao
NACI 公司
成员:S Deeks(主席)、R Harrison(副主席)、J Bettinger、N Brousseau、P de Wals、E Dubé、V Dubey、K Hildebrand、K Klein、J Papenburg、C Rotstein、B Sander、S Smith 和 S Wilson。
前成员:C Quach (主席)
联络代表:LM Bucci(加拿大公共卫生协会)、E Castillo(加拿大妇产科医师协会)、A Cohn(美国疾病控制和预防中心)、L Dupuis(加拿大护士协会)、J Emili(加拿大家庭医生学院)、D Fell(加拿大免疫研究和评估协会)、M Lavoie(卫生首席医疗官委员会)、 D Moore(加拿大儿科学会)、M Naus 博士(加拿大免疫委员会)、A Pham-Huy(加拿大医学微生物学和传染病协会)、P Emberley(加拿大药剂师协会)、L Bill(加拿大土著护士协会)和 S Funnel 博士(加拿大土著医师协会)。当然代表:K Robinson(HC 上市保健品局)、E Henry(免疫和呼吸道传染病中心 [CIRID]、PHAC)、M Lacroix(公共卫生伦理咨询小组)、S Ogunnaike-Cooke(CIRID、PHAC)、C Lourenco(加拿大卫生部生物和放射性药物局)、G Poliquin(国家微生物学实验室)、V Beswick-Escanlar(国防和加拿大武装部队)、 和 T Wong(加拿大土著服务部原住民和因纽特人健康处)。
附录 A:加拿大各省和地区以及国际上接受帕利珠单抗的当前标准
PVZ (PVZ) 预防的资格标准来自加拿大所有省份和地区以及 10 个北半球国家。数据总结如下表所示。
加拿大:
无慢性肺病或血流动力学显著的先天性心脏病 (hsCHD) 的早产儿
NACI 在 2003 年建议对 ≤ 胎龄 32 周 (wGA) 和 <6 个月大的婴儿在 RSV 季节开始时进行 PVZ 预防。目前的加拿大免疫指南 (CIG) 指出,根据当地的考虑,选定的 33-35 wGA 婴儿也可能受益。加拿大儿科学会 (CPS) 在 2015 年指出,对 < wGA 出生且 < 6 个月大的早产儿进行预防是合理的,但不是必需的。
六个省和地区 (PT) 遵循了针对 32 ≤ wGA 婴儿和部分 33-35 wGA 婴儿(AB、MB、NB、NT、ON、SK)的现行 CIG 建议。所有 6 个 PT 都使用定义的风险评分来确定该组的资格,但所有 PT 使用的风险标准和评分系统都不同。两项 PT 为≤ 29 wGA 的患者和有危险因素 (BC、YT) 的 29-35 wGA 患者提供预防。一个地区为所有 36 wGA (NU) <提供 PVZ。只有一个省份遵循了 NACI 建议 (QC)。三个省份遵循了 CPS 的建议,对 30 wGA (NL、NS、PE) <的人进行预防。
慢性早产儿肺病 (CLD) 和其他慢性肺部疾病
2003 年,NACI 建议在 RSV 季节开始时 < 24 个月大且在过去 6 个月内需要治疗的 CLD 或患有其他需要氧疗的肺部疾病的儿童进行 PVZ,而目前的 CIG 仅提及患有 CLD 的儿童。CPS 建议对 RSV 季节开始时年龄< 12 个月且需要持续治疗的 CLD 患者进行预防, 但只有在仍然需要补充氧气或在过去 3 个月内断氧的情况下,才能用于他们的第二个 RSV 季节。患有囊性纤维化、上气道阻塞或除 CLD 以外的慢性肺部疾病的儿童不应常规进行预防,但可以考虑用于 24 个月以上、正在接受家庭吸氧或因严重肺部疾病长期住院<儿童。
8 例 PT 遵循 NACI 对 CLD 儿童 (AB、MB、NB、NS、ON、PE、QC、SK) 进行预防的建议,而 3 例 PT 婴儿仅符合 12 个月龄的条件 (BC、NL、YT)。在一个地区,所有年龄< 12 个月大的 CLD 婴儿和在过去 3 个月内需要治疗的 12-24 个月婴儿都符合条件 (NU),而在另一个选定的地区,wGA < 36 岁且年龄< 24 个月的 CHD 婴儿仅符合具体情况 (NT)。
9 项 PT 为 <24 个月 (8) 或 <12 个月 (1) 的婴儿提供其他慢性肺部疾病的预防,其中一些 PT 需要单独评估。病症包括囊性纤维化 (7)、先天性肺或气道异常 (4) 以及影响清除气道分泌物能力的神经肌肉疾病 (5)。其他包括需要家庭呼吸支持(O2、机械通气、气管切开术、CPAP)和其他严重肺残疾。
先天性心脏病
2003 年的 NACI 和当前的 CIG 建议对年龄< 24 个月的 hsCHD 儿童进行预防。CPS 建议仅对 <12 个月大的患者进行预防。
6 名 PT 为 24 个月< (AB、NB、NT、NS、PE、SK) 的 hsCHD 儿童提供预防,4 名为 12 个月大<的儿童和个体评估后 12-24 个月的儿童提供预防 (BC、MB、ON、YK)。前 12 个月的 3 次有限预防 (NL、NU、QC)。
其他临床情况:
CPS 指出,如果 24 个月大<的唐氏综合症或免疫缺陷儿童使用家庭氧气、因严重肺部疾病长期住院或严重免疫功能低下,则可以考虑对 24 个月大的唐氏综合症或免疫缺陷儿童进行预防。
10 项 PT 列出了其他预防临床标准,其中一些需要单独评估。7 项提供了唐氏综合征的预防 (1 项需要额外的合并症);8 例针对免疫缺陷(严重程度不同),1 例针对神经肌肉疾病,未提及呼吸道分泌物的清除。
在 4 例 PT 中,如果一个兄弟姐妹符合预防条件 (AB、BC、ON、YK),则对多胞胎兄弟姐妹进行预防,但只有一个 (ON) 例外,只有当婴儿早产时。在一个省份,所有年龄≤ 35 岁的多胞胎婴儿(双胞胎除外)6/7wGA 和 < 3 个月大符合预防条件 (AB)。在另一种情况下,经批准的儿童的双胞胎可能在评估后 (NT) 符合资格。
除了两个 PT (NB, YK) 外,所有方案都规定,在单独评估后,可以根据要求考虑其他医疗状况。
偏远地区:
5 个省份对生活在偏远北部地区的儿童(MB、NL、ON、QC、SK)有具体标准,而其他 4 个 PT (AB、BC、NT、YT)在风险评分中考虑了偏远地区。一个地区为所有 36 wGA (NU) <提供 PVZ。大多数包括 ≤36 wGA 和 < 6 个月大的婴儿。一项研究纳入了 < 3 个月大 (QC) 的足月婴儿。
定义 RSV 季节和 PVZ 剂量:
在 6 个 PT (AB、BC、ON、SK、YT、NT) 中,RSV 预防期基于当地的 RSV 流行病学,在 5 个 PT (NL、NS、PE、QC、NU) 中使用固定日期。未找到两个 PT 的信息。
PVZ 剂量之间的推荐间隔为 28 天,分 6 个 PT (NS、NU、NT、PE、QC、SK) 和每月 1 个 (NB)。在 AB 中,AB 北部的推荐间隔为 28 天,但第二剂为 21 天,后续剂量为 28 天。BC 和 ON,第二剂的推荐间隔为 21-28 天,后续剂量为 28-35 天,而在 NL 中,第二剂的推荐间隔为 28 天,后续剂量为 35 天。在 YK 中,第二剂的间隔为 18-24 天,后续剂量为 28-30 天。建议的 MB 间隔为第 4 剂前 28 天,第 4 剂和第 5 剂之间为 35 天,第 5 剂和第 6 剂之间为 42 天。
最大剂量为 7 PT (AB、NB、NS、PE、ON、QC、SK) 中 5 剂,1 剂 6 剂 (MB),根据当地流行病学延长剂量 6 剂 (NU) 和 1 剂 4 剂 (NL)。在 BC 中,< wGA 的婴儿和患有 CLD 或 hsCHD 的婴儿的最大剂量数为 4 剂,≥29 wGA 且无 CLD 或 hsCHD 的早产儿的最大剂量数为 3 剂。2 项没有说明最大值 (YK, NT)。
国际:
无慢性肺病或血流动力学显着的先天性心脏病 (hsCHD) 的早产儿。
三个国家单独使用胎龄,具有不同的 wGA 限值: < 26 (瑞典) 、 < 29 (美国) 和 <32 (荷兰)。四个国家(奥地利、德国、意大利、西班牙)建议使用风险评分对低于特定 wGA 的所有婴儿(< 28 至 <31)和较少早产儿(高达 34 至 36 wGA)进行预防。三个国家(法国、瑞士、英国)没有单独提供早产儿的预防。
慢性早产儿肺病 (CLD) 和其他慢性肺部疾病
所有 10 个国家都建议对患有慢性早产儿肺病的婴儿进行预防。除瑞士和英国外,8 个国家/地区包括在过去 6 个月内需要治疗的 24 个月<婴儿,其中 5 个国家包括所有 12 个月<婴儿,1 个国家包括所有 6 个月大的<婴儿,无论是否接受治疗。瑞士建议仅对 1 < 岁儿童进行预防。英国建议使用胎龄和实际年龄网格进行预防,包括 ≤ 34 wGA 和 9 至 1.5 个月大的婴儿。
除法国和西班牙外,8 个国家还建议对 1 岁或 << 2 岁患有其他肺部疾病的儿童进行常规或个体评估的预防措施。这些疾病包括 5 个国家的囊性纤维化,2 个国家干扰呼吸道分泌物清除的神经肌肉疾病,4 个国家的呼吸道或肺部先天性异常,以及其他疾病,例如需要长期需要氧疗、机械通气或气管切开术的慢性肺部疾病。
先天性心脏病
所有 10 个国家都建议对重度 CHD 婴儿进行预防,在法国、西班牙和荷兰为 2 岁以下,仅在意大利、瑞典、瑞士为第一年进行预防,在美国为第一年进行预防,并考虑延长至第二年。德国建议在 6 月龄时进行预防,在 6-12 月龄时单独考虑。英国纳入了 ≤26 至 ≤32 wGA 和 1.5 至 6 个月大的婴儿,基于使用这两个参数的网格。奥地利建议,无论年龄大小,在手术矫正或心脏移植之前都应进行预防。
其他临床情况:
在 8 个国家 (除法国和西班牙外) 进行个体评估后,考虑了其他临床状况。这些疾病包括奥地利、德国、瑞典和瑞士所有 8 种不同程度的免疫缺陷,神经或神经肌肉疾病,未提及呼吸道分泌物清除,意大利和瑞士的 21 三体综合征,以及瑞典的染色体异常或贮积病。
缩写:AB Alberta;不列颠哥伦比亚省不列颠哥伦比亚省;马尼托巴省;NB 新不伦瑞克省;NL 纽芬兰和拉布拉多;北领地西北地区;NS 新斯科舍省;NU 努纳武特地区;安大略省:PE 爱德华王子岛;QC 魁北克;SK 萨斯喀彻温省;YT 育空地区;美国 美国;英国
| 管辖 | 群 | 其他脚注* | ||
|---|---|---|---|---|
| 无 CLD 的早产儿 | 患有呼吸系统疾病的儿童 | 患有心脏病的儿童 | ||
| NACI (2003 年) | “推荐” 当地 RSV 季节开始时 ≤32 wGA 和 <6 m 龄 | “推荐” <24 m 龄,早产儿 CLD 需要 O2和/或前 6 m 的药物治疗,或其他需要 O 的肺部疾病2疗法 | “推荐” <24 m 龄 hsCHD | “可以考虑” 偏远社区:根据对获得医疗服务的评估和其他已知会增加风险的因素,< 35 wGA 且年龄 < 6 m |
| CIG (2013 年) | “推荐” 当地 RSV 季节开始时 ≤32 wGA 和 <6 m 龄 在当地 RSV 季节开始时出生 33 至 35 wGA 且年龄 <6 m 的选定婴儿可能会受益;根据当地因素做出的决定。 | “推荐” <24 m 龄,早产儿 CLD 需要 O2和/或药物治疗前 6 m | “推荐”< 24 m 的 hsCHD(紫绀型和非紫绀型) | “可以考虑” 根据对获得医疗服务的评估和其他已知会增加风险的因素,在 RSV 季节开始时出生的 32-35 wGA < 6 m,并生活在农村或偏远社区 “应考虑” |
| CPS (2015) | “合理但并非必须提供”: <300/7在 RSV 赛季开始时年龄 < 6 m 的 wGA | “should receive”: CLD(定义为需要 O236 wGA) 或需要持续利尿剂、支气管扩张剂、类固醇或补充 O2如果在 RSV 季节开始时 <1 岁。 如果仍在补充 O 中,则第二个 RSV 季节2或在过去 3 m 内断奶 如果年龄 <24 m 并且在家中 O,则“可以考虑” | 如果在 RSV 季节开始时年龄 <12 m,则“应该接受” hsCHD。 在第二个 RSV 季节中不指示 | “应该提供” 偏远社区需要航空运输的儿童,出生< 36 wGA,在 RSV 季节开始时年龄< 6 m。 目前尚不清楚是否应该仅适用于因纽特人、所有土著或偏远社区的所有婴儿。考虑 RSV 住院的当地发生率。 “可以考虑”:如果生活在 RSV 住院率持续较高的社区,则 6 m < 的足月因纽特婴儿 “可以考虑: |
| 阿尔伯塔省(2020-21) | ≤ 286/72020 年 5 月 31 日之后出生的 wGA 290/7– 326/7wGA,2020 年 9 月 30 日之后出生 330/7– 356/72020 年 10 月 31 日之后出生的 wGA 且风险评分为 >55 早产儿: 330/7– 356/7wGA 其他方面健康且符合 RSV 免疫预防条件的患者的双胞胎/ 早产儿:多胞胎(不包括双胞胎)≤ 35 岁6/7wGA 且出生于 2020 年 9 月 30 日之后 | ≤356/7wGA 且截至 2020 年 12 月 1 日年龄 <2 岁患有 CLD(家 O22020 年 5 月 31 日之后或长期预防或需要全身性类固醇的近期恶化) 气管切开术年龄 < 2 岁 2020 年 12 月 1 日。 可以考虑:
| <2020 年 12 月 1 日年满 2 岁,患有严重的 hsCHD(提供符合条件和不符合条件的疾病列表;由心脏病专家审查的转诊) | 21 三体,年龄< 1 岁,截至 2020 年 12 月 1 日 严重免疫缺陷:
神经肌肉疾病: 无年龄限制的例外情况:体重低于 15 公斤的 1 型脊髓性肌萎缩症 其他 24 个月<儿童可以单独考虑 |
| 不列颠哥伦比亚省 (2020-21) | < 29 wGA 并在 2020 年 9 月 1 日或之后出院回家 29 – 346/7wGA 并在 2020 年 10 月 1 日或之后出院回家,风险因素评分为 ≥42 分 < 35 wGA 和经批准的儿童的多胞胎,并且在 2019 年 11 月 1 日或之后出生(即 RSV 赛季开始时< 1 岁) | BPD/CLD (O2或 CPAP 在 > 28 天)且在 2019 年 11 月 1 日或之后出生并需要持续 O22020 年 7 月 1 日或之后 其他:
| 2020 年 11 月 1 日患有 hsCHD 和 <1 岁需要婴儿心脏病专家的支持 严重的心肺残疾(即肺动脉高压、心脏姑息治疗等)且在 2018 年 11 月 1 日或 | 2020 年 4 月 1 日或之后出生的 21 三体 需要裁决:
|
| 曼尼托巴 省(2020-21) | <33 wGA 和 RSV 季节开始时年龄 <6 m 2020 年 10 月 31 日之后出生的 33-35 wGA 并且居住在或将居住在偏远的北部社区 将考虑风险评分为 ≥65 的 33-35 wGA | < 24 个月大的 BPD 患者,已接受 O2RSV 季节开始前 6 m 内接受治疗 | < 12 m 龄,患有儿科心脏病学的 hsCHD。应通过 12-24 m 龄患有 hsCHD 的儿科心脏病学 转诊,但将根据具体情况进行评估 | 其他 24 个月<儿童可以单独考虑 |
| 新不伦瑞克省 (2020-21) | 应考虑用于 32 <的婴儿0/7≤ RSV 季节开始时 wGA 和年龄 6 m(出生于 2020 年 6 月 1 日或之后) 321/7达到 35 wGA 且风险评分为 >49 | 应考虑用于 24 ≤ m 患有 CLD/BPD 且需要 O2或 RSV 季节前 6 m 内的药物治疗(即 2020 年 6 月至 11 月) 根据具体情况进行审查: | 对于 24 < m 的 hsCHD 儿童(需要矫正手术或出于血流动力学考虑而服用心脏药物),应考虑进行此项检查 | 根据具体情况进行审查: 与家人讨论后的唐氏综合症;<12 m 龄将获得批准 |
| 纽芬兰和拉布拉多省 (2020-21) | ≤ 300/7wGA 且 RSV 季节开始时年龄≤ 6 m(即必须在 2020 年 6 月 1 日或之后出生) | ≤ 300/7wGA 和年龄≤ 6 m 年龄在 RSV 季节开始时患有 CLD/BPD(即必须在 020 年 6 月 1 日或之后出生) ≤ 12 m 龄且患有 CLD/BPD 且需要 O2和/或 RSV 季节前 6 m 内的药物治疗(即 2020 年 6 月 1 日之后) | ≤ 12 m 大患有紫绀性或无紫绀性 hsCHD(需要矫正手术或出于血流动力学考虑而正在服用心脏药物),由儿科心脏病专家确定 | ≤ 360/7wGA 和<在 RSV 季节开始时年龄为 6 m 并且居住在孤立或偏远的北部社区,根据获得医疗服务和其他已知会增加风险的因素(必须在 2020 年 6 月 1 日或之后出生),绝对应考虑进行预防 其他儿童可能会根据个人情况予以考虑 |
| 西北地区 (2020-2021) | 早产≤326/7截至 2020 年 12 月 1 日,wGA 且年龄< 6 m(2020 年 5 月 31 日之后出生) 可能符合条件,将被评估: | 可能符合条件,将接受评估:
| 可能符合条件,将进行评估: 截至 2020 年 12 月 1 日,hsCHD 年龄< 2 岁 | 可能符合条件,将接受评估:
其他儿童可能会根据个人情况予以考虑 |
| 新斯科舍省, PEI (2020-21) | ≤300/7wGA 和 ≤6 m 年龄(即必须在 2020 年 6 月 1 日或之后出生) | ≤300/7患有 BPD/CLD 且年龄 ≤6 m 的 wGA(即必须在 2020 年 6 月 1 日或之后出生) <24 m 年龄 BPD/CLD 且需要 O2和/或 RSV 季节前 6 m 内的药物治疗(即 2020 年 6 月 1 日至 11 月) 需要咨询:
| ≤24 m 龄患有 hsCHD(需要药物治疗的 LR 分流,CHD 待手术,持续发绀), 由儿科心脏病专家确定 | 需要咨询:
其他儿童可能会根据个人情况予以考虑 |
| 努纳武特 地区(2020-21) | ≤356/7在 RSV 季节开始时或期间 wGA 和 ≤6 m 岁(7 月 1 日或之后出生) | <RSV 季节开始时 12 m 龄患有 CLD(需要 O236 wGA)目前需要持续的补充 O2和/或药物治疗(利尿剂、支气管扩张剂、类固醇) RSV 季节开始时 <24 m 龄,BPD 需要持续的补充 O2或断奶补充 O2过去 3 个月内 24 个月大的儿童可以考虑<:
仅在 Home O 上2或因严重肺部疾病长期住院 | hsCHD < RSV 季节开始时 12 m 龄(CHD 需要补充 O2和/或正在进行的药物治疗) | 可考虑用于 24 < m 且
其他儿童可能会根据个人情况予以考虑 |
| 安大略省 (2020-21) | ≤32 wGA 且年龄≤ 6 m,在当地 RSV 季节开始时或期间 33 – 35 人完成了 wGA,在当地 RSV 季节开始时或期间年龄≤ 6 m,不生活在孤立的社区,风险评分为 49 – 100 33 – 35 人完成了 wGA,在当地 RSV 季节开始时或期间年龄≤ 6 m,并且居住在因无法立即获得医疗服务(< 30 分钟,I 级医院)和/或无法及时获得儿科服务(<90 分钟)而定义的孤立社区 | <24 m 年龄 BPD 需要 O2和/或 RSV 季节前 6 m 内针对 CLD 的药物治疗 | <12 m 龄伴有紫绀性或无紫绀性 hsCHD;需要矫正手术或因充血性心力衰竭而服用心脏药物或被诊断患有中度至重度肺动脉高压 12-24 岁患有持续 hsCHD 的儿童将根据具体情况予以考虑 需要心脏会诊 | 患有唐氏综合症< 24 米儿童 多胞胎的兄弟姐妹,如果一个孩子符合预防条件 其他儿童可能会根据个人情况予以考虑 |
| 魁北克 省(2020-21) | <33 wGA 年龄 < RSV 季节开始时 6 m | 早产 <24 m 龄在 RSV 季节开始时患有 BPD(定义为需要 O2治疗持续至出生后至少 28 天和胎龄≥36 周) 并且需要 O2在 RSV 季节之前或期间的 6 m 足月,RSV 季节开始时年龄 <24 m,并且 < RSV 季节开始时 24 m 龄,并且
| <RSV 季节开始时 1 岁患有 CHD、心肌病或心肌炎,导致临床上显着的血流动力学后果 <RSV 季节开始时 1 岁患有中度或重度肺动脉高压 必须由儿科心脏病专家要求) | 在 RSV 季节之前或期间的 6 个月内进行 HSCT、干细胞或实体器官移植,在 RSV 季节开始时< 24 m ≤36 wGA < 6 m 发病或 RSV 季节,居住在努纳维克 <发病时或在 RSV 季节居住于努纳维克的 3 m 龄足月婴儿(正在审查中) 其他儿童可能会根据个人情况予以考虑 |
| 萨斯喀彻温省 (2020-21) | <2020 年 6 月 1 日或之后出生的 30 名 wGA < 2020 年 9 月 1 日或之后出生的 33 名 wGA < 36 名 wGA 在当前 RSV 季节(11 月至 2 月)出生,且风险评分 ≥60 < 36 名在当前 RSV 季节出生的 wGA 妊娠,居住在 La Ronge 或北部。 | < 2 岁患有 BPD/CLD 且需要 O2RSV 季节前 6 个月内 < 1 岁患有囊性纤维化 | < 由儿科心脏病学评估的 2 岁 hsCHD 儿童 | 其他儿童可能会根据个人情况予以考虑 |
| 育空 地区(2020-21) | < 290/7wGA 并在 2020 年 9 月 1 日或之后出院回家 290/7– 346/7wGA 且在 2020 年 10 月 1 日或之后出院回家且危险因素评分> 41 经批准的多胞胎和符合条件的双胞胎符合早产儿条件 | 早产于 BPD/CLD(氧气或 CPAP 超过 28 天)且在 2019 年 11 月 1 日或之后出生,并且在 2020 年 7 月 1 日或之后持续吸氧 2020 年 11 月 1 日或之后气管切开术/持续家庭氧气/通气,并在 2018 年 11 月 1 日或之后出生 2018 年 11 月 1 日或之后出生的无法清除分泌物的进行性神经肌肉疾病(需要裁决) 2018 年 11 月 1 日或之后出生的严重肺残疾(肺畸形、严重 BPD、有症状的囊性纤维化等)(需要裁决) | 血流动力学显着的 CHD 且出生于 2019 年 11 月 1 日或之后(需要临床详情和支持心脏病专家) 严重的心肺残疾(肺动脉高压、心脏姑息治疗、其他)并且在 2018 年 11 月 1 日或之后出生(需要裁决) | 2020 年 4 月 1 日或之后出生的 21 三体 严重免疫缺陷(例如干细胞移植)且在 2018 年 11 月 1 日或之后出生 |
BPD: 支气管肺发育不良;CLD : 慢性肺病;CPAP:持续气道正压通气; | ||||
| 风险因素 | 艾伯塔省 (评分 >55) | 不列颠哥伦比亚省 (分数 ≥42) | 曼尼托巴省 (得分 ≥65) | New Brunswick (得分 ≥49) | Northwest Territories (得分 ≥55 | 安大略省 (得分 ≥49) | 萨斯喀彻温省 (分数 ≥60) | 育空 地区 (得分 >41) |
|---|---|---|---|---|---|---|---|---|
| 出生月份 | √(11 月至 2 月) | N/A | √ (11 月至 3 月) | √(11 月至 1 月) 25 | N/A | √(11 月至 1 月)25 | √ (11 月至 2 月) 27 | N/A |
| 婴儿或兄弟姐妹参加托儿所 | N/A | N/A | √ | √ 17 | N/A | N/A | N/A | N/A |
| 4 ≤ 岁的婴儿或兄弟姐妹参加托儿所 | √ | N/A | N/A | N/A | N/A | N/A | N/A | N/A |
| 4 ≤婴儿或兄弟姐妹每周 3 个半天≥托儿所 | N/A | N/A | N/A | N/A | √ 19 | N/A | N/A | N/A |
| 婴儿或兄弟姐妹参加托儿所≥每周 20 小时或幼儿园/学前班≥ 3 个半天/周 | N/A | N/A | N/A | N/A | N/A | N/A | √ 19 | N/A |
| 婴儿将在出院后的前 3 个月内定期参加日托 | N/A | √ 22 | N/A | N/A | N/A | N/A | N/A | √ 22 |
| 婴儿在这个冬天参加日托或兄弟姐妹在日托或幼儿园 | N/A | N/A | N/A | N/A | N/A | √ 17 | N/A | N/A |
| 婴儿参加家庭或设施团体 | N/A | N/A | N/A | N/A | N/A | N/A | N/A | N/A |
| >5 个人在家中,包括申请人和申请人的倍数 | √ | √ 12 | √ | √ 13 | √ 15 | √ 13 | √ 15 | √ 12 |
| 其他 < 5 岁的儿童(不包括申请人的倍数) | N/A | √ 14 | N/A | N/A | N/A | N/A | N/A | √ 14 |
| 出院回家 12 月至 2 月 | N/A | √(北部卫生区至 3 月) 20 | N/A | N/A | N/A | N/A | N/A | √ 20 |
| 出院回家 11 月或 3 月 | N/A | √(北部卫生区至 4 月) 10 | N/A | N/A | N/A | N/A | N/A | √ 10 |
| 出院回家 11 月至 2 月 | N/A | N/A | N/A | N/A | √ 27 | N/A | N/A | N/A |
| 总 29-306/7骷髅王 | N/A | √ 10 | N/A | N/A | N/A | N/A | N/A | √ 10 |
| GA 较小(GA 的出生体重<第 10 个百分位数) | √ | N/A | √ | √ 12 | √ 14 | √ 12 | √ 14 | √ 8 |
| GA 较小(出生体重≤ GA 的第 10 个百分位数 | N/A | √ 8 | N/A | N/A | N/A | N/A | N/A | N/A |
| 雄 | √ | N/A | √ | √ 11 | √ 13 | √ 11 | √ 13 | N/A |
| 男性(全部)或未接受母乳的女性 | N/A | √ 8 | N/A | N/A | N/A | N/A | N/A | √ 8 |
| 直系亲属(母亲、父亲、兄弟姐妹)均无湿疹 | N/A | N/A | √ | √ 12 | N/A | √ 12 | N/A | N/A |
| 家中有 2 个或更多吸烟者 | √ | √ 8 | √ | √ 10 | N/A | N/A | N/A | √ 8 |
| 家中的吸烟者 | N/A | N/A | N/A | N/A | √ 13 | √ 10 | √ 12 | N/A |
| 居住距离最近的提供毛细支气管炎治疗的医院 2 小时以上 | √ | N/A | N/A | N/A | N/A | N/A | N/A | N/A |
| 居住地距离最近的提供毛细支气管炎治疗的医院 1 小时车程以上 | N/A | N/A | N/A | N/A | √ 20 | N/A | N/A | N/A |
| 地处偏远,没有永久的道路通道 | √ | N/A | N/A | N/A | N/A | N/A | N/A | N/A |
| 偏远位置 从医院/儿科护理点出发 100 公里或 1 小时的地面交通 | N/A | √ 10 | N/A | N/A | N/A | N/A | N/A | N/A |
| 远程居住(育空地区被视为偏远地区) | N/A | N/A | N/A | N/A | N/A | N/A | N/A | √ 10 |
N/A:不可用 | ||||||||
| 管辖 | 群 | |||
|---|---|---|---|---|
| 早产儿 | 患有肺病的儿童 | 患有心脏病的儿童 | 其他 | |
| 奥地利 2008 奥地利儿科和青少年医学 会 (OGKJ) Resch 2009, 2017 | < 28 wGA 且年龄≤ 12 m 28-<32 wGA 且年龄≤ 6 m 且有危险因素 32-<36 wGA 且年龄 ≤ 6 m 且有危险因素(不同量表) | BPD 年龄< 2 岁且在过去 6 个月内 需要治疗可以考虑:其他 CLD、< 2 岁的囊性纤维化 | hsCHD 直至矫正或移植 | 可以考虑; 年龄 ≤ 24 米和免疫缺陷、神经肌肉疾病 |
| 法国 ,2017,Haute autorité de santé Commission de la transparence | – | ≤ 32 wGA,RSV 季节开始时年龄 < 6 m,呼吸系统疾病(需要 > 28 天的 O2新生儿期) ≤ 32 wGA,RSV 季节开始时年龄 < 24 m,呼吸系统疾病(需要 > 28 天的 O2在新生儿期)和前期需要治疗的中度或重度 BPD | < 2 岁患有 hsCHD | N/A |
| 德国 2017/18 德国儿科传染病学会 (DGPI) | 可给予: ≤ 286/7wGA 和年龄 ≤ 6 m 290/7至 346/7wGA 和年龄 ≤ 6 m,考虑危险因素 | 应接受: 早产儿年龄 ≤ 24 m,BPD/CLD 接受 O 治疗2或在 RSV 季节开始前 3 个月内通气 CLD 的基础综合征或神经系统疾病 | 应接受: hsCHD 年龄 < 6 m 且需要手术,患有肺动脉高压、肺静脉充血或发绀、药物治疗的严重心力衰竭 可能收到: | 可考虑: 严重免疫缺陷 应接受: |
| 意大利 2018 意大利医药局 (AIFA) Bollani 2015 Belleudi 2018 | < 29 wGA 和年龄 ≤12 m,29-35 wGA 和年龄 ≤ 6 m,考虑危险因素 | BPD 年龄≤ 12 m 伴有 BPD(定义为需要 O2≥出生后 28 天治疗) BPD 年龄 1-2 岁,需要在过去 6 m | < 1 岁患有严重 CHD(手术前或姑息手术后紫绀型心脏病,正在接受充血性心力衰竭治疗并计划接受手术)、中度至重度肺动脉高压、手术修复的 CHD 仍需要治疗充血性心力衰竭、等待心脏移植或处于移植后的婴儿。 | 考虑一下: 免疫缺陷、唐氏综合征 |
| 西班牙 2005 年、2015 年西班牙新生儿学会 (SENeo) 标准委员会Figueras-Aloy 2015 | ≤ 286/7wGA 和年龄 < 9 m 29-316/7wGA 和年龄 < 6 m 321/7至 346/7wGA 和年龄 < 6 m(如果存在危险因素) | CLD 且年龄< 2 岁,在过去 6 个月内需要治疗 | hsCHD 且年龄< 2 岁且在过去 12 个月内需要治疗 | N/A |
| 瑞典 2015 瑞典药品管理局 | < 26 wGA 且年龄< 6 个月 | BPD 和年龄< 12 m 需要 O2前 6 m 治疗年龄 12-24 m,如果仍然需要 O2 年龄< 12 m 的严重 CLD(食管闭锁、膈疝、气管畸形、支气管和/或肺 | CHD 和年龄< 12 m 且血流动力学显着的心力衰竭,明显的肺动脉高压,心肌病伴明显的心力衰竭 2 岁以下患有复杂性心力衰竭 | 可根据个人情况考虑: 年龄< 1 岁患有神经肌肉疾病、染色体异常、贮积病或免疫缺陷 |
| 瑞士 2016 跨学科工作组 Aygeman 2016 | 不推荐 | BPD 年龄 < 1 岁 重度:推荐 中度:可能认为 轻度:不推荐 (定义分类) 年龄 < 24 m 患有囊性纤维化或解剖学肺畸形,在特定病例中可考虑, | 可能考虑: hsCHD 年龄 < 12 m 和紫绀型 CHD、严重肺动脉高压、心力衰竭 | 其他: 年龄 < 24 米且有免疫缺陷、唐氏综合症、神经肌肉疾病等特定病例可予考虑 |
| 荷兰 2006 荷兰儿科学会 (NVK) Whelan 2016 | < 32 wGA 且年龄< 6 m | < 1 岁患有 BPD 或肺动脉高压 < 2 岁患有 BPD(如果需要 O)2或药物 < 1 岁患有囊性纤维化引起的严重肺部病变 | hsCHD 年龄 < 2 岁 | 已选 : 严重免疫缺陷 年龄 < 1 岁 |
| 英国 2015 年绿皮书,JCVI) | 不仅适用于早产儿 | 患有中度或重度 BPD 的早产儿(定义为具有相容 X 线变化并继续接受补充 O 的早产儿2或胎龄 36 周时的呼吸支持。应提供以下预防性治疗: 321/7– 340/7wGA 年龄 < 1.5 m 281/7– 320/7wGA 年龄 < 3 m 241/7– 280/7wGA 年龄 < 6 m ≤ 24 岁0/7wGA 年龄 < 9 m b) 患有呼吸系统疾病的婴儿,不一定是早产儿,但仍处于 O2在 RSV 季节开始时,包括:
如果年龄< 24 m 且根据氧依赖性反映的其他合并病理,则在季节开始时接受长期通气的人 | 在 RSV 季节开始时的实际 年龄和出生时胎龄以下为血流动力学显著的无紫绀型 CHD 的早产儿:301/7– 320/7wGA 年龄 < 1.5 m 261/7– 30 wGA 年龄 < 3 m ≤ 26 岁0/7GA 年龄 < 6 m 紫绀型或无紫绀型冠心病加上严重的合并症,尤其是累及多个器官系统时 | < 24 m 龄的 SCID 无法产生 T 细胞反应或产生抗体 – 直到免疫重组。 |
| 美国 2014 (AAP) | 文本中的“可以管理”;summary 显示 “推荐” < 290/7在 RSV 季节 | 文本中的“可以考虑”;summary 显示 “推荐” <320/7早产儿 CLD 的 wGA(定义为出生后至少前 28 天,出生后第一年需要 >21% 的氧气。 第二年:仅在上述情况加上持续需要医疗支持(类固醇、利尿剂、O2) 在第二个 RSV 季节开始前 6 m 内。 可以考虑: 出生后第一年患有囊性纤维化伴 CLD 或营养不良;如果既往因肺部加重或胸部 X 线检查或 CT 异常在稳定时持续住院,则可在第二年考虑该检查;身长体重 < 十分之一 | “可能受益于”。摘要说“可以施用”某些患有 hsCHD 的婴儿 < hsCHD 的 RSV 季节开始时年龄 1 岁(咨询儿科心脏病专家) “可以考虑”:年龄< 2 岁并在 RSV 季节接受心脏移植 | 其他: 可以考虑: 没有足够的数据证明: 根据当地流行病学,阿拉斯加本土婴儿的选择可能有所不同 不建议用于预防哮喘 |
N/A:不可用 | ||||
来源:
加拿大:
- 国家免疫咨询委员会。关于单克隆抗 RSV 抗体 (PVZ) 推荐用途的声明。CCDR 2003;29。ACS-7,8 的。
- 加拿大公共卫生署。加拿大免疫指南:第 5 部分 – 被动免疫。
https://www.canada.ca/en/public-health/services/publications/healthy-living/canadian-immunization-guide-part-5-passive-immunization.html - Robinson JL, Le Saux N, 加拿大儿科学会传染病和免疫委员会。预防呼吸道合胞病毒住院。儿科儿童健康 2015;20(6):321.26
- 阿尔伯塔省卫生服务:https://www.albertahealthservices.ca/assets/info/hp/rsv/if-hp-rsv-criteria.pdf;https://www.albertahealthservices.ca/frm-18957.pdf
- 不列颠哥伦比亚省卫生服务管理局:
https://www.childhealthbc.ca/sites/default/files/b.c.-rsv-manual-2020-21v2.pdf - Manitoba Children’s Hospital:个人通信
- 新不伦瑞克省卫生部:个人通信
- 纽芬兰和拉布拉多东部卫生局:个人通信
- 西北地区:
https://www.hss.gov.nt.ca/professionals/en/services/seasonal-rsv-prophylaxis-synagis%C2%AE-program-package-2020-2021 - 新斯科舍省 IWK 健康中心
https://www.iwk.nshealth.ca/PVZ/provincial-guidelines/indications-for-use - 努纳武特卫生部:
https://www.gov.nu.ca/sites/default/files/11.0_specialized_and_annual_immunization_protocols_december_2020.pdf - 爱德华王子岛:个人通信(使用新斯科舍省协议)
- 安大略省卫生部:
https://www.health.gov.on.ca/en/pro/programs/drugs/funded_drug/pdf/rsv_season2020-2021.pdf - Hema-Quebec:https://www.hema-quebec.qc.ca/userfiles/file/media/francais/hopitaux/20-030.pdf
- 萨斯喀彻温省卫生局:https://www.saskatoonhealthregion.ca/locations_services/Services/Childrens-Services/RSV-Program/Pages/Forms.aspx
- 育空地区卫生和社会服务部:https://yukon.ca/sites/yukon.ca/files/hss/hss-imgs/Section_5_-_immunization_of_special_populations_october_2020.pdf
国际:
奥地利,奥地利儿科和青少年医学会:
- Resch B、Manzoni P、Lanari M 等人。患有神经肌肉疾病和免疫缺陷综合征的婴儿的严重呼吸道合胞病毒 (RSV) 感染。Paediatr Respir Rev. 2009;10:148–53.
- Österreichische Gesellschaft für Kinder- und Jugendheilkunde (ÖGKJ).Konsensuspapier zur prophylaxe der RSV-infektion mit PVZ und post-RSV-atemwegserkrankung Monatsschr Kinderheilkd 2008:156:381-383.https://doi.org/10.1007/s00112-008-1722-y
- Resch B, Bramreiter VS, Kurath-Koller S, Freidl T, Urlesberger B. 使用 PVZ 预防风险评分工具对 29 至 32 周胎龄早产儿的呼吸道合胞病毒相关住院治疗。欧洲临床微生物感染疾病杂志 (2017) 36:1057–1062。
France, Haute autorité de santé Commission de la transparence:
- https://www.has-sante.fr/portail/upload/docs/evamed/CT-15884_SYNAGIS_QD_INS_Avis2_CT15884.pdf 访问时间 2021 年 3 月 22 日
德国,德国儿科传染病学会:
- https://www.awmf.org/uploads/tx_szleitlinien/048-012l_S2k_Prophylaxe-von-schweren_RSV-Erkrankungen-Risikokindern-PVZ_2018-11.pdf 访问时间 2021 年 3 月 22 日
意大利意大利医药局:
- Bollani L、Baraldi E、Chirico G 等人。关于呼吸道合胞病毒 (RSV) PVZ 预防的修订建议。意大利儿科杂志 2015;15:97。
- Belleudi V、Trotta F、Pinnarelli L 等人。意大利 Arch Dis Child 2018 年 PVZ 新报销限制后的新生儿结局;103:1163–1167。
西班牙,西班牙新生儿学会标准委员会:
- Figueras Aloy J, Quero J, Comité de Estándares de la Sociedad Española de Neonatología.预防呼吸道合胞病毒感染的建议。儿科 (Barc) 2005;63(4):357-62.
- Figueras Aloy J, Carbonell Estrany X, Comité de Estándares de la Sociedad Española de Neonatología.使用 PVZ 预防晚期早产儿(妊娠 321 至 350 周)呼吸道合胞病毒感染的建议。儿科 (Barc) 2010;73 (2) 2010:98.e1-98.e4.
- Figueras Aloy J, Carbonell Estrany X, Comité de Estándares de la SENeo.关于使用 PVZ 预防 RSV 感染的建议更新。儿科 (Barc) 2015;82(3):199.e1-199.e2
瑞典,医疗产品署:
- http://www.lakemedelsverket.se/malgrupp/Halso—sjukvard/Behandlings–rekommendationer/Behandlingsrekommendation—listan/RSV-infektioner/ 访问时间:2021 年 3 月 22 日
瑞士,跨学科工作组:
- Agyemana P, Barazzoneb C, Hammerb J et al. Prävention von RSV-Infektionen mit dem humanisierten monoklonalen Antikörper PVZ.2017 年瑞士医学论坛;17(28-29):611-614.
荷兰,荷兰儿科协会;卫生部
- 卫生、健康和体育部(报销)。https://zoek.officielebekendmakingen.nl/stcrt-2006-218-p29-SC77527.pdf 2021 年 3 月 21 日访问。
- Whelan B、Musters E、Murray A 等人。爱尔兰和荷兰呼吸道合胞病毒 (RSV) 预防的家庭护理计划综述。药物 Ther Perspect 2016;32:119–130
英国,英格兰公共卫生部:
- https://assets.publishing.service.gov.uk/government/uploads/system/uploads/attachment_data/file/458469/Green_Book_Chapter_27a_v2_0W.PDF 评估时间 2021 年 3 月 22 日
美国,美国儿科学会:
- 传染病和毛细支气管炎指南委员会。更新了因呼吸道合胞病毒感染住院风险增加的婴幼儿的 PVZ 预防指南。儿科 2014;134:415–420
附录 B:帕利珠单抗的安全性
介绍
PVZ (PVZ) 被认为是安全的商品。由于 NACI 2003 PVZ 声明中对不良事件 (AE) 的描述脚注4没有安全警报,但暴露于 PVZ 的婴儿数量已大幅增加。NACI 确定,这需要对 PVZ 安全数据进行新的评估,并需要快速文献检索和审查加拿大警戒计划的数据脚注210将执行。
方法
2.1. 快速文献综述
使用以下来源对 PVZ 的安全性进行了快速文献综述:
- 2013 年发表的 PVZ 安全性系统评价(AMSTAR 评为平均)用于确定 2013 年之前发表的研究脚注211.对这些研究进行了综述。
- 根据下面的研究问题进行了文献检索。检索策略是与加拿大卫生部图书馆员 (LG) 一起制定的,包括 2013 年以后的出版物,并于 2019 年 4 月 24 日进行。详细的搜索策略如下所示。由于时间限制,文献检索仅限于两个书目数据库 (MEDLINE 和 EMBASE)
- 还审查了检索中获得的参考文献中引用但未包含在 (1) 或 (2) 中的研究。
筛选、合格性评估、资料提取和质量评估由一名评价员完成。制作了一份数据汇总表,其中包含使用 NACI 的标准方法(表 B)对证据质量进行评级(表 C)。接受的研究结果以叙述方式进行综合。
研究问题:PVZ 对人类使用的安全性如何?
P(人口):人类(无年龄限制)
I(干预):肌内注射 PVZ
C(比较):安慰剂、其他单克隆抗体或无单克隆抗体
O(结局):不良事件
确定符合条件的研究:
在加拿大卫生部文献检索中检索到的文章被加载到 RefWorks(ProQuest LLC,密歇根州安娜堡)并上传到 DistillerSR(Evidence Partners,加拿大渥太华)。已删除重复记录。按标题和摘要筛选记录。检索根据纳入和排除标准相关的文章的全文,或没有足够的信息来排除的文章,并通过全文筛选评估合格性。
如果研究符合以下标准,则纳入:
- 该研究涉及对儿童肌肉注射 PVZ。
- 该研究提供了有关安全性或 AE 的数据。(如果进行了 PVZ 但摘要中没有提及这些,则该研究仍被纳入全文审查,因为研究可以包括安全数据,而无需在摘要中引用)。
如果研究符合以下一项或多项标准,则被排除在外:
- 该研究没有提供有关 AE 或安全性的数据
- PVZ 未肌肉注射
- 该研究使用英语或法语以外的语言
- 这项研究是非人类的
- 这篇文章是一篇社论或一篇观点。
- 该研究仅介绍了二级研究(接受系统评价)。
2.2. 来自加拿大警戒计划的数据
加拿大警戒计划 (CVP) 是加拿大卫生部在上市保健品局 (MHPD) 内的上市后监测计划,旨在收集和评估对保健品的疑似不良反应报告。CVP 的目的是检测与保健品相关的不良反应的可能安全信号。不良反应报告是可疑的关联,反映了个别报告者的观点或观察,并不反映加拿大卫生部对保健品与反应之间关联的任何评估。包含特定反应并不一定意味着它是由可疑的保健品引起的。严重不良事件 (SAE) 是指需要住院治疗或延长现有住院治疗、导致先天性畸形、导致持续或严重残疾或无能力、危及生命或导致死亡的事件。其他可能危及患者或可能需要干预的重要医疗事件也可能被视为严重事件。
截至 2018 年 12 月 31 日向 CVP 提交的报告已于 2019 年 4 月 5 日下载。如果出现安全信号,MHPD 还会定期进行安全审查 (MedEffect™ Canada)。没有必要进行安全审查。
3. 结果
3.1. 文献综述
3.1.1. 随机对照试验
确定了 9 例双盲 RCT。4 项是安慰剂对照的脚注48 脚注80 脚注111 脚注140 脚注141,两个比较了冻干和液体形式的 PVZ脚注212 脚注2133 项将 PVZ 与 otavizumab (MVZ)(另一种针对呼吸道合胞病毒的单克隆抗体,未经许可)进行了比较脚注214 脚注215 脚注216.7 人的质量被评为良好,而 1 人被评为脚注111被评为一般。第九篇是在系统评价中评估的会议摘要,其中包括更多信息,被评为良好。
在胎龄 ≤ 35 周出生且年龄≤ 6 个月≤或 24 个月大患有支气管肺发育不良 (BPD) 的儿童的初始 PVZ IMPACT RCT 中,盲法研究者报告的可能与研究药物相关的 AE 发生率在 PVZ 组和安慰剂组中相似(分别为 11% 和 10%)。AE 类型(包括注射部位反应)无显著差异。没有 SAE。因 AE 而停用 PVZ 的情况很少见 (0.3%)。PVZ 组有 4 例 (0.4%) 死亡,安慰剂组有 5 例 (1%) 死亡,原因被判断为与研究药物无关。接受 PVZ 的婴儿人数为 1002 人脚注48.
一项针对 24 个月大血流动力学显著 CHD (hsCHD) 儿童≤随机对照试验报告称,PVZ 组和安慰剂组的 AE 总发生率相似(96% 对 97%)和盲法研究者判断与研究药物相关的 AE 发生率相似(7.2% 对 6.9%)。安慰剂组的 SAE 更高 (63% vs 55%,p=0.005),但 RSV 住院被纳入 SAE。判断与研究药物相关的 SAE 很少见(PVZ 和安慰剂组分别为 0% 和 0.5%)。没有因 AE 而停药。PVZ 组有 3.3% 的死亡,安慰剂组有 4.2% 的死亡,但没有一个归因于研究药物。接受 PVZ 的婴儿人数为 639 人脚注80.
PVZ 在 <2 岁囊性纤维化儿童中的 RCT 结果作为会议摘要呈现脚注141并且是后来系统评价中唯一的研究脚注140.PVZ 与安慰剂相比,AE 、 SAE、研究药物相关 AE 发生率 (5.4% 对 4.4%) 或研究药物相关 SAE 发生率 (0 对 2.1%) 的总体差异无统计学意义。PVZ 在一个案例中因 SAE 而停止。没有死亡。接受 PVZ 的儿童人数为 92 人。
一项针对 33-35 wGA 出生且年龄≤ 6 个月的其他方面健康的早产儿的 RCT 仅报告了住院和死亡为 AE。安慰剂组的住院率高于 PVZ 组 (21.9% vs 12.6%,p=0.04),但当去除 RSV 住院治疗时,差异不显著 (19.1% vs 安慰剂组 vs PVZ 组 14.0%)。没有死亡。接受 PVZ 的婴儿人数为 214 人脚注111.
两项随机对照试验,比较 24 个月大或出生体重 ≤≤ 35 周重且年龄≤ 6 个月的慢性肺病儿童的冻干和液体 PVZ 制剂脚注212或在 ≤ wGA 出生的婴儿脚注213发现 AE 的总体发生率无显著差异脚注213或 SAE脚注212 脚注213.在两项研究中,SAE 发生在 5.9% 和 2.6% 的冻干 PVZ 受者以及 8.5% 和 3.3% 的液体 PVZ 受者中,但没有一个被判断为与研究药物有关。一名接受冻干 PVZ 的儿童有 1 例死亡,被认为与研究药物无关脚注212.暴露于 PVZ 的婴儿总数为 413 人脚注212和 305脚注213.
在一项比较 PVZ 与 MVZ 的随机对照试验中,≤ 35 wGA 龄且年龄≤ 6 个月或 ≤ 24 个月患有慢性肺病的早产儿中,AE 和 SAE 的总体发生率相似。在 PVZ 组中观察到的 AE 包括皮肤和皮下疾病 18.5%;2.7% 的注射部位反应,2.9% 的精神疾病 (烦躁、嗜睡、不安、易怒)。AE 被认为是可能的皮肤超敏反应发生在 0.2% 的 PVZ 受者中。没有过敏反应病例。PVZ 组的 SAE 发生率为 15.3%。AE 与研究药物的关系尚未确定。PVZ 因 0.3% 的 AE 而停药。PVZ 的死亡率为 0.1%,没有死亡被认为与 PVZ 相关。接受 PVZ 的儿童人数为 3298 人脚注214.PVZ 与 MVZ 的第二项研究包括 ≤ 24 个月的 hsCHD 儿童。两种产品的 AE 和 SAE 总体发生率相似。在 PVZ 组中,判断与研究药物相关的 AE 和 SAE 分别占 8.8% 和 1.0%。1 例患者 (0.2%) 因黄斑皮疹而停用 PVZ。死亡率为 1.6%,无与研究药物相关的死亡。接受 PVZ 的儿童人数为 612 人脚注216.III项研究比较了 PVZ 与 MVZ 在 ≤ 35 wGA 龄≤ 6 个月或 ≤ 24 个月患有慢性肺病的早产儿中的疗效,使用了交叉设计,报告了交叉前后每种药物的 AE。与 PVZ 相关的 AE 发生率为 9.3%。没有与 PVZ 相关的 SAE。PVZ 在 1 例 (0.6%) 因 AE 而停药。没有死亡。接受 PVZ 的儿童人数为 161 人脚注215.
3.1.2 基于人群的队列研究
在瑞典和丹麦进行了两项基于人群的队列研究,被评为高质量,使用国家健康登记册调查 PVZ 接受者与其他人群相比发生的特定事件。年龄调整后的人群为 1,351,265 人,其中 1192 名儿童接受了 PVZ。第一项研究着眼于自身免疫性疾病的发病率,自身免疫性疾病的发病率在 PVZ 接受者中没有显着增加,瑞典儿童的发病率为 0.54%,未暴露于 PVZ 的丹麦儿童的发病率为 0.60%,PVZ 接受者的发病率为 0.76%;调整后风险比 (HR) 1.54,95% CI 0.80,2.95脚注217.第二项研究调查了特应性。暴露于 PVZ 后哮喘风险增加 (HR 1.49, 95% CI 1.32, 1.68),但在事后分析使用倾向评分平衡混杂因素后,这不再显著 (HR 0.91;95% CI 0.56, 1.48)。特应性皮炎 (HR 1.18;95% CI 0.94, 1.48) 或过敏性鼻结膜炎 (HR 1.14;95% CI 0.92, 1.42) 的风险没有增加脚注218.
3.1.3 前瞻性登记和队列研究
加拿大 RSV PVZ 评估研究 (CARESS) 登记处描述了 13,025 名 PVZ 受者(出生时年龄≤ 35 wGA 或患有 hsCHD 或 BPD 或其他复杂疾病)的 SAE,这些受者从 2008 年到 2013 年接受了 57,392 剂 PVZ。排除了因呼吸道感染住院的情况。52 名婴儿中有 62 例 SAE。被认为可能与或可能与 PVZ 相关的 SAE 发生率为 2.8/10,000 患者月或每 10,000 剂 2.4,其中 14 例 SAE 发生在 6 名患者中 (0.05%)。所有提示超敏反应,并在 4 名再次挑战的儿童的后续剂量中复发:第二次和III次给药后全身性红斑和支气管痉挛;第 3 剂后不久出现全身性荨麻疹;注射后 5 分钟出现面部红斑;第 2 剂和第 3 剂后注射部位附近出现局部皮疹;以及 2 名婴儿在 4 剂中每剂后出现长时间呕吐和鼻塞。这 6 名患者和另外 14 名患者停用了 PVZ,其中 3 名患者因呼吸道感染住院,11 名患者因 AE 不符合 SAE 条件(大腿皮疹、胃肠道不适、烦躁和“不适”)而停用。有 5 例死亡,与 PVZ 无关脚注170.在 2005 年至 2009 年 CARESS 登记处的早期数据报告中,5286 名儿童接受了 19,485 剂 PVZ。有 61 例 SAE,其中 56 例因呼吸道感染住院。没有提供有关其他 5 个 SAE 的详细信息。由于 AE,1.7% 的受者停用了 PVZ。有 5 例死亡被认为可能与 PVZ 无关或无关脚注219.对 2010 年 CARESS 数据的回顾报告了 8 例死亡,其中与 PVZ 无关脚注220.报告了 2001-2014 年来自 CARESS 的数据与来自意大利的前瞻性队列相结合。在 14,468 名 PVZ 接受者中,7 名患者 (0.05%) 报告了 15 例与 PVZ 相关的 SAE。所有 15 例 SAEs 均为超敏反应。这些结果与上述 Chen 的结果重叠脚注221.
2002 年至 2007 年德国 PVZ 登记处的数据表明,10,686 名受试者接受了 49,608 剂 PVZ。SAE 可能或可能与 PVZ 相关,发生在 10 名受试者 (0.09%) 中,发病率为每 10,000 剂 2 例)。SAE 为呼吸困难或发绀伴或不伴发热 (4),以及皮疹、血小板减少症、骨髓炎、癫痫发作、反应性低下和发热伴烦躁不安。有 3 例死亡,1 例与 PVZ 无关,2 例无法评估脚注222.后来的出版物报告了来自同一登记处的 2009-2016 年数据,当时 12,729 名受试者接受了 63,572 剂。8 例 (0.06%) 或 1.3/10,000 剂报告了可能与 PVZ 相关的 SAE。这些事件被描述为呼吸停止 (2)、皮疹、发热皮疹、荨麻疹、激动、注射部位红斑和腿部活动急性受限 (各 1 例)。有 9 例死亡,与 PVZ 无关脚注223.
一项来自 15 个北半球国家的国际前瞻性观察研究报告了 565 名早产儿 (≤ 35 wGA) 和 6 个月或 24 个月≤≤ BPD 婴儿,他们在 1998-9 年接受了 PVZ。45 名婴儿有 1 项或多项 AE,其中 39 名有 40 项 AE 被认为与 PVZ 相关 (7%)。最常见的相关 AE 是注射部位反应 (12) 、发烧 (8) 、腹泻 (4) 和紧张或易激惹 (4)。没有一个是 SAE。11 例因 AE 停用 PVZ,其中 3 例被认为可能与或可能与 PVZ 相关:注射后立即氧饱和度下降、腹部和外周水肿以及胃肠炎。有 2 例死亡,与 PVZ 无关脚注224.一项来自 17 个欧洲国家和沙特阿拉伯的国际前瞻性观察研究研究了 2000-2001 年接受 PVZ 治疗的 285 名 29-32 岁 ≤ 6 个月大的早产儿。5 例患者 (2.5%) 有 7 例 AE (发热、肠炎、支气管炎、鼻炎、咳嗽、细菌性肺炎、结膜炎) 与 PVZ 相关,其中 1 例 (细菌性肺炎) 为 SAE (0.35%)。此外,一例 RSV 毛细支气管炎被归类为可能与 PVZ 相关的 SAE。2 例因 AE 停用 PVZ,其中 1 例 (发热) 被认为可能与 PVZ 有关。没有死亡脚注225.一项来自 7 个拉丁美洲国家的国际前瞻性观察研究报告了 459-2011 年 12 名 PVZ 受者(出生时 ≤ 35 wGA 或患有 BPD 或 hsCHD)。有 1165 个 AE。102 例患者共发生 135 例 SAE,但均无 1 例被认为与 PVZ 相关。有 3 例与 PVZ 无关的死亡脚注226.
来自法国的一项多中心前瞻性观察研究报告了 516 名接受 PVZ 治疗早产儿 (≤ 32 wGA 且年龄≤ 6 个月或 ≤ 35 wGA 且年龄< 2 岁)的数据。有 15 例 AE 被判断为可能与 PVZ 相关: 呼吸暂停 (n=3) 发热 (n=3) 注射部位疼痛 (n=2) 过度通气 (n=2) 和虚弱、呕吐、支气管炎、咳嗽、荨麻疹 (各 1 例)。没有 SAE。有 10 人死亡,没有人归因于 PVZ脚注227.后来来自法国的一项多中心前瞻性观察研究报告了 1371 名 6257 剂 PVZ 接受者的 SAE。没有判断与 PVZ 相关的 SAE。有 6 人死亡,无人归因于 PVZ脚注228.来自日本的一项多中心前瞻性观察研究跟踪了 304 名 24 个月< 岁且在 2013-15 年接受 PVZ 且免疫功能低下或患有唐氏综合症的儿童。99 名儿童共发生 220 例 AE,其中 25 例儿童 (8%) 的 33 例 AE 被认为可能与 PVZ 有关:(肺炎 (3)、RSV 感染 (3)、其他感染 (11)、上呼吸道炎症 (5)、哮喘 (1)、腹泻 (2) 和其他 (8)。89 例 SAE 发生在 53 例患者中。其中,7 名患者 (2.3%) 的 8 例 SAE 被认为与 PVZ(肺炎 (4 例)、RSV 感染 (2 例)和支气管炎和上呼吸道炎症 (各 1 例)有关。对于 4 例患者的另外 5 例 SAE (感染性休克、设备相关感染、哮喘、药物相关肝损伤、肾母细胞瘤),与 PVZ 的关系被认为无法确定。7 例患者因 AE 停止 PVZ脚注229.来自西班牙的一项多中心前瞻性观察研究对 1919 名 GA ≤ 周龄 32 周、6 个月大≤早产儿报告没有与 PVZ 相关的死亡脚注46.
在 7 项较小的前瞻性观察研究中,共有 560 名婴儿接受了 PVZ;未报告与 PVZ 相关的 SAE脚注44 脚注230 脚注231 脚注232 脚注233 脚注234 脚注235.
来自波兰的一项多中心回顾性观察性研究报告了 3241 名儿童的 1021 剂 PVZ 剂量。84 名受者 (8.2%) 有 108 例 AE,最常见的是紧张 (40) 、发烧 (24)、注射部位反应 (15)、腹泻 (4)、呕吐 (4)。没有报告任何 AE 是否为 SAE 以及与 PVZ 的关系,也没有报告因 AE 导致的死亡或 PVZ 停药脚注236.卡塔尔的一项描述性回顾性/前瞻性单中心研究报告称,429 名 ≤ wGA ≤ 6 个月或 2 ≤ 岁患有 CLD 或 hsCHD 的早产儿无 AE 和无归因于 PVZ 的死亡脚注237.一项针对加拿大 187 名 < 2 岁囊性纤维化儿童的回顾性多中心研究报告称,没有与 PVZ 相关的 SAE脚注77.韩国一项对 75 名 35 岁 35 岁出生的 2 ≤< 岁慢性肺病早产儿进行的回顾性单中心队列研究报告了 3 例注射部位反应,无系统性、呼吸或胃肠道事件症状脚注238.
两项针对接受 PVZ 一季或两季的儿童的研究发现,第一季与第二季的 AE 频率或类型没有差异,但受试者数量很少(第一季 103 人;第二季 119 人)脚注231 脚注232.
3.1.4 归因于 PVZ 的严重不良事件的病例报告
一份病例报告描述了在服用 PVZ 后 20 分钟发作的非致命性过敏反应。脚注239孩子在上一季接受了 5 剂 PVZ,在本季接受了 1 剂前一剂)。过敏反应很少见报道。制造商在 2002 年报告了 2 例在服用 2,000,000 剂 PVZ 后出现过敏反应脚注240.
在另一例病例报告中,一名儿童在第一次服用 PVZ 后 8 小时出现呼吸暂停、心动过缓和氧饱和度下降。鼻咽拭子发现患儿有副流感病毒 1 型和鼻病毒/肠道病毒。对 1998 年至 2017 年向德国医学会药物委员会报告的数据的审查显示,PVZ 给药后有 93 例呼吸暂停/心动过缓、氧饱和度下降或心肺事件报告,其中除 29 例外,其余均与并发感染有关。PVZ 后 48 小时内有 3 例心肺事件死亡病例,均无伴随感染,但均伴有重度 CHD。作者得出结论,没有足够的信息来评估 PVZ 给药后心肺事件的关联脚注241.
3.1.5 抗 PVZ 抗体的检测和临床意义:
在一项早期研究中,在 1.2% 的 PVZ 和 2.8% 的安慰剂接受者中检测到 PVZ 抗体,这表明 PVZ 与抗体的结合是非特异性的脚注48.在随后的研究中,在 1.5-5.9% 的 PVZ 受者中检测到抗 PVZ 抗体脚注212 脚注213 脚注216 脚注230 脚注231 脚注232.抗体通常以短暂和低水平存在,并且在 PVZ 暴露的第一年和第二年之间没有后续剂量或反应差异脚注231 脚注232.抗 PVZ 抗体与 AE 事件的存在或类型无关,包括潜在的免疫介导的反应,并且不影响 PVZ 水平。
3.2 来自加拿大警戒计划的数据
截至 2018 年 12 月 31 日,PVZ 给药后有 259 例独特的 AE 病例报告,其中 237 例被认为严重。最常见的事件是呼吸道事件,137 例 (53%),其中 113 例是感染 (主要是由于 PVZ 产品失败报告),其次是超敏反应,23 例 (9%)。报告的其他事件是推荐使用 PVZ 的潜在疾病的预期并发症,并且与产品专论中报告的事件一致。PVZ 在这些 AE 中的作用尚不清楚,因为未评估因果关系。
总结
被认为与 PVZ 相关的最常见报告的 AE 是注射部位反应、发烧、紧张或易怒、咳嗽、鼻炎和腹泻。PVZ 相关 SAE 很少见,在 1% 或更少的受者中报告,大多数研究没有报告。大多数是超敏反应。确定了 3 例过敏反应报告。因 AE 而停用 PVZ 的受者发生在 0-2.3% 的受者中。没有可归因于 PVZ 的死亡。
重复注射人源化单克隆抗体引起了对免疫介导疾病发展的关注脚注217 脚注242.研究表明,暴露于 PVZ 的儿童患自身免疫性疾病或特应性疾病的风险没有增加。
表 A:搜索策略和结果
Medline
数据库: Ovid MEDLINE(R) ALL 1946年至2019年4月23日
检索策略:
| # | 搜索 | 结果 |
|---|---|---|
| 1 | PVZ/ | 688 |
| 2 | EXP 抗体,单克隆/和(呼吸道合胞病毒疫苗/或呼吸道合胞病毒、人类/或呼吸道合胞病毒感染/) | 863 |
| 3 | (PVZ* 或 medi 493 或单克隆抗体 medi-493 或单克隆抗体 medi 493 或单克隆抗体 medi493 或 medi-493 或 medi493 或 synagis 或 abbosynagis 或 synagys 或((呼吸道合胞病毒* 或 RSV)adj5 单克隆*)).ti,kf,kw。 | 600 |
| 4 | (PVZ* 或 medi 493 或单克隆抗体 medi-493 或单克隆抗体 medi 493 或单克隆抗体 medi493 或 medi-493 或 medi493 或 synagis 或 abbosynagis 或 synagys 或((呼吸道合胞病毒* 或 RSV)adj5 单克隆*))).ab. /频率=2 | 556 |
| 5 | 1 或 2 或 3 或 4 [PVZ] | 1141 |
| 6 | 死亡 / 或 EXP “药物相关副作用和不良反应”/ 或 EXP 产品监测、上市后 / 或风险评估/ 或风险因素/ 或 EXP 安全性/ 或异常、药物诱导 / 或 EXP 毒性试验/ 或过敏原/ 或 EXP 超敏反应/ 或 EXP 诱变/ 或 EXP 食物-药物相互作用/ 或 EXP 草药-药物相互作用/ 或药物致死/ | 1755435 |
| 7 | (上市后或上市后或不良或过敏*或并发症?或皮炎*或超敏反应*或伤害或伤害或有害或不耐受*或耐受*或有毒*或荨麻疹或毒物*或心脏毒素*或细胞毒素*或皮肤毒素*或dermotox*或胚胎毒素*或胎儿氧毒素*或Genotox*或肝毒素*或免疫毒素*或物质毒素*或肾毒素*或神经毒素*或耳毒性*或医原*或致畸剂*或诱变剂*或致癌物*或死亡*或致命*或危害*或致命*或“危及生命”或 “危及生命”或mortal* 或 Safe or Safety or unsafe or ((side or unintentional or unintentional or unwanted or unexpected or undesirable or serious or serious or serious or interactive* or interaction* or outcome* or reaction* or reaction* or reaction* or response*))).ti,kf,kw. | 1746562 |
| 8 | (上市后或上市后或不良或过敏*或并发症?或皮炎*或超敏反应*或伤害或伤害或有害或不耐受*或耐受*或有毒*或荨麻疹或毒物*或心脏毒素*或细胞毒素*或皮肤毒素*或dermotox*或胚胎毒素*或胎儿氧毒素*或Genotox*或肝毒素*或免疫毒素*或物质毒素*或肾毒素*或神经毒素*或耳毒性*或医原*或致畸剂*或诱变剂*或致癌物*或死亡*或致命*或危害*或致命*或“危及生命”或 “危及生命”或mortal* or safe or safety or unsafe or ((side or unintentional or unintentional or unwanted or unexpected or undesirable or serious or serious or serious or interactive* or interaction* or outcome* or react* or response*))).ab. /freq=2 | 2287607 |
| 9 | 6 或 7 或 8 [不良事件] | 4455565 |
| 10 | 5 和 9 | 398 |
| 11 | 限制 10 到 yr = “2013 – Current” | 150 |
Embase 公司
数据库: Embase 1974 年至 2019 年 4 月 23 日
检索策略:
| # | 搜索 | 结果 |
|---|---|---|
| 1 | *PVZ/ | 817 |
| 2 | *单克隆抗体/ 和 (*呼吸道合胞病毒感染/ 或 *呼吸道合胞病毒疫苗/ 或 EXP *人类呼吸道合胞病毒/) | 48 |
| 3 | (PVZ* 或 medi 493 或单克隆抗体 medi-493 或单克隆抗体 medi 493 或单克隆抗体 medi493 或 medi-493 或 medi493 或 synagis 或 abbosynagis 或 synagys 或((呼吸道合胞病毒* 或 RSV)adj5 单克隆*))).ti,kw。 | 934 |
| 4 | (PVZ* 或 medi 493 或单克隆抗体 medi-493 或单克隆抗体 medi 493 或单克隆抗体 medi493 或 medi-493 或 medi493 或 synagis 或 abbosynagis 或 synagys 或((呼吸道合胞病毒* 或 RSV)adj5 单克隆*))).ab. /频率=2 | 808 |
| 5 | 1 或 2 或 3 或 4 [PVZ] | 1317 |
| 6 | exp *死亡/或 *药物安全/ 或 exp *上市后监测/ 或 *风险评估/ 或 *风险因素/ 或 *安全/ 或 *发育毒性/ 或 exp *生殖毒性/ 或 exp *毒性试验/ 或 exp *毒性测试/ 或 exp *毒理学/ 或 exp *毒性和中毒“/ 或 exp *毒理学参数/ 或 exp *毒性物质/ 或 exp *过敏性/ 或 exp *致癌性/ 或 exp *致突变性/ 或 exp *诱变性/ 或 exp *诱变/或 exp *药物禁忌症/ 或 *药物效应/ 或 exp *不良药物reaction/ 或 exp *“药物毒性和中毒”/ 或 *食品药物相互作用/ 或 *草药药物相互作用/ 或 exp *副作用/ | 1204250 |
| 7 | (上市后或上市后或不良或过敏*或并发症?或皮炎*或超敏反应*或伤害或伤害或有害或不耐受*或耐受*或有毒*或荨麻疹或毒物*或心脏毒素*或细胞毒素*或皮肤毒素*或dermotox*或胚胎毒素*或胎儿毒素*或Genotox*或肝毒素*或免疫毒素*或物质毒素*或肾毒素*或神经毒素*或耳毒性*或医源性*或致畸剂*或诱变剂*或致癌物*或死亡*或致命*或危害*或致命*或“危及生命”或mortal* 或 Safe or Safety or unsafe or (((side or unintentional or unintentional or unintentional or unwanted or unexpected or undesirable or serious or serious or serious or serious or allergy or allergy) adj3 (效果* 或事件* 或影响* or 互动* or 结果* or 反应* or 响应*))).ti,kw. | 2146080 |
| 8 | (上市后或上市后或不良或过敏*或并发症?或皮炎*或超敏反应*或伤害或伤害或有害或不耐受*或耐受*或有毒*或荨麻疹或毒物*或心脏毒素*或细胞毒素*或皮肤毒素*或dermotox*或胚胎毒素*或胎儿氧毒素*或Genotox*或肝毒素*或免疫毒素*或物质毒素*或肾毒素*或神经毒素*或耳毒性*或医原*或致畸剂*或诱变剂*或致癌物*或死亡*或致命*或危害*或致命*或“危及生命”或 “危及生命”或mortal* or safe or safety or unsafe or ((side or unintentional or unintentional or unwanted or unexpected or undesirable or serious or serious or serious or interactive* or interaction* or outcome* or react* or response*))).ab. /freq=2 | 3293097 |
| 9 | 6 或 7 或 8 [不良事件] | 4866691 |
| 10 | 5 和 9 | 302 |
| 11 | 限制 10 到 yr = “2013 – Current” | 131 |
图 1:PVZ 安全性文献综述研究选择过程的 PRISMA 流程图
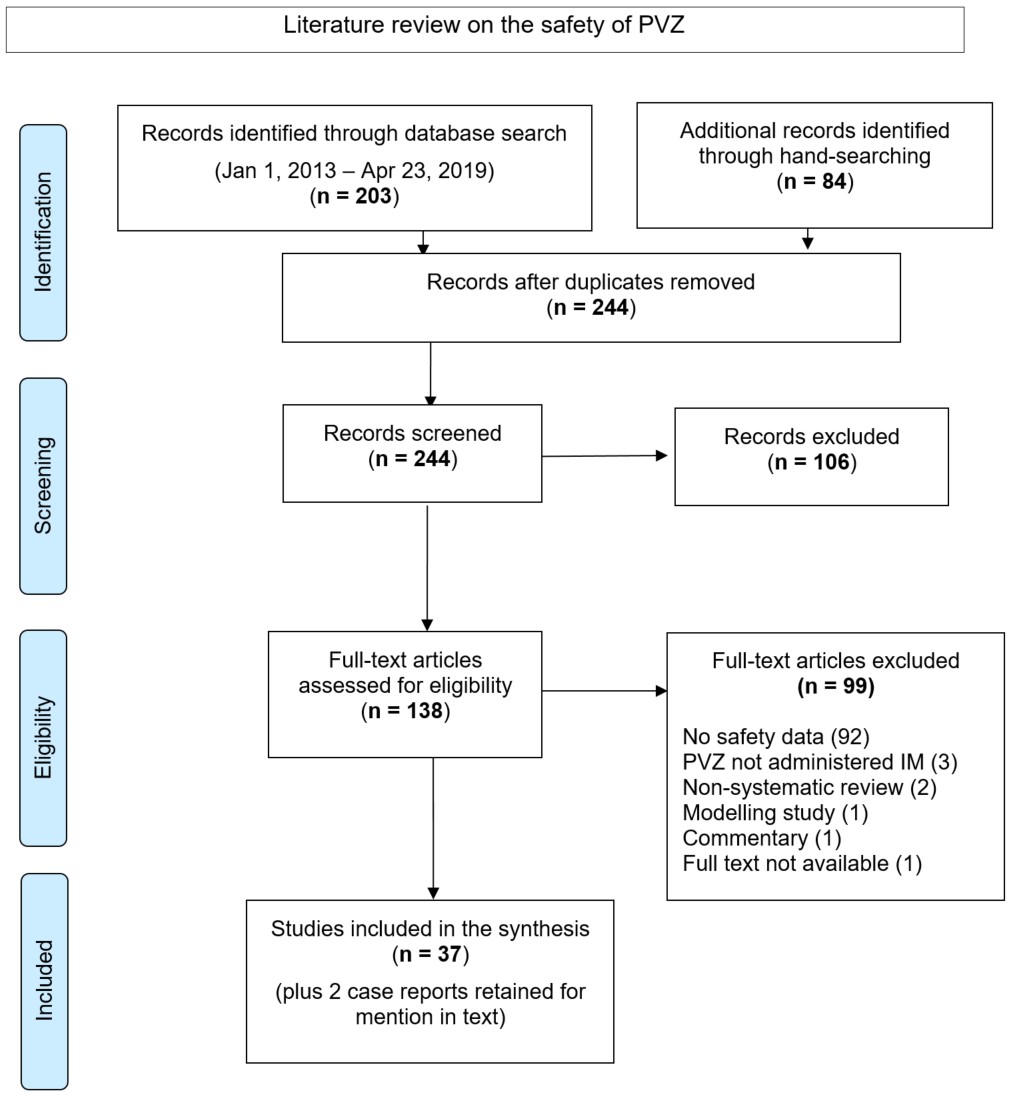
图 1:文本描述
缩写:PRISMA,系统评价和荟萃分析的首选报告项目;PVZ,帕利珠单抗;IM,肌内注射。
PRISMA 流程图描述了为 PVZ 安全性文献综述选择文章的过程。该过程分为四个阶段:识别、筛选、资格和包括。
第 1 阶段:识别
- 通过 2013 年 1 月 1 日至 2019 年 4 月 23 日的数据库检索确定了 203 条记录,通过手工检索确定了 84 条记录。
- 删除重复项后,仍保留 244 条记录。
第 2 阶段:筛选
- 然后筛选了 224 条记录。
- 在这 224 条记录中,排除了 106 条记录。
第 3 阶段:资格
- 对 138 篇全文文章进行了合格评估。
- 在这 138 篇全文文章中,99 篇被排除在外。排除细分如下:92 项未报告安全性数据,3 项未报告肌内注射 PVZ,2 项为非系统评价,1 项为建模研究,1 项为评论,1 项研究为评论,1 项研究的全文不可用。
第 4 阶段:包括
- 共收录 37 篇文章。
- 对 2 例病例报告进行了重新训练,以便在文本中提及。
表 B:基于研究设计和证据质量(内部效度)评级的证据水平
| 水平 | 描述 |
|---|---|
| I | 来自随机对照试验的证据。 |
| II-1 | 来自无随机化的对照试验的证据。 |
| II-2 | 来自队列或病例对照分析研究的证据,最好来自多个使用疫苗功效临床结果测量的中心或研究小组。 |
| II-3 | 从有或没有干预的多个时间序列中获得的证据。不受控制的实验中的戏剧性结果(例如 1940 年代引入青霉素治疗的结果)也可以被视为此类证据。 |
| III | 受人尊敬的权威机构的意见,基于临床经验、描述性研究和病例报告,或专家委员会的报告。 |
| 质量评级 | 描述 |
|---|---|
| 好 | 满足所有设计特定标准的研究(包括荟萃分析或系统评价)表 B2 脚注*井。 |
| 一般 | 一项研究(包括荟萃分析或系统评价)不符合(或不清楚是否满足)至少一项设计特定标准表 B2 脚注*但没有已知的“致命缺陷”。 |
| 差 | 至少有一项针对设计的研究(包括荟萃分析或系统评价)表 B2 脚注*“致命缺陷”,或较轻缺陷的累积,以至于研究结果被认为无法为建议提供信息。 |
| |
表 C:与 PVZ 安全性相关的证据摘要
列出顺序:系统评价(按字母顺序),然后根据证据级别按降序排列单个研究,然后是证据质量,然后按字母顺序排列
| 研究详细信息 | 总结 | ||||
|---|---|---|---|---|---|
| 研究 | 研究设计 | 参与者 | 主要发现摘要 | 证据级别 | 质量 |
| Robinson 等人,2016 年脚注140 原始 RCT 的资金:工业 审查资金: | RCT 系统评价:1 项 RCT 发现 美国多中心 (40 个地点) 1998-2001 每月 x 5 个月以 1:1 的比例随机分配到 PVZ 15 mg/kg 或安慰剂 | 2 < 岁的囊性纤维化儿童 PVZ:92 96% 的人接种了所有 5 剂疫苗 | 只发现了一项 RCT:Cohen et al 2005。系统评价的作者从作者那里获得了更多信息。 随访 150 天(最后一次给药后 30 天) 有事件的子对象数: 任何 AE: 相关 AE: 任何 SAE: 相关 SAE: 未提供 | 我 | 好 使用 |
| Wegzyn et al., 2014脚注211 由 AbbVie Inc. 资助 | 随机对照试验和前瞻性观察研究的系统评价 1996-2013 PVZ (PVZ) 预防与无干预 | 出生时 ≤35 wGA 或患有慢性肺病或 CHD 的儿童 (N ≈ 42,000) | 没有荟萃分析的系统评价。本综述中确定的 PVZ 安全性的个别研究按作者单独在本表中列出。请参阅本表其他部分,了解以下研究的结果:
(未使用来自系统评价的数据) | 在 NACI 方法下没有评级 | 平均 使用 AMSTAR 评估) |
| NBlanken 等人,2013 年脚注111 资金来源: | RCT Multicenter The Netherlands (16 个站点) 2008 年 4 月至 2010 年 12 月 冬季以 1:1 的比例随机分配至 PVZ 15 mg/kg 或安慰剂。 | RSV 季节开始时 33 – 35 wGA 和 ≤6 个月大的健康早产儿 PVZ:214 中位注射 = 每组 4 次。 | 随访至 1 岁 (父母记录每日日志) 仅报告死亡和住院情况。未记录局部注射部位反应和非呼吸道症状的就诊。 没有死亡。 住院 住院儿童人数 住院人数 RSV 感染 其他呼吸系统疾病 胃肠炎 手术 生长迟缓 其他 非 RSV 住院人数 * p=0.04 ** p= 0.16 | 我 | 一般 (有限的 AE 确定) |
| Carbonell-Estrany 等人,2010 年脚注214 赞助商: MedImmune | RCT International – 欧洲、美洲、澳大利亚、新西兰、保加利亚、土耳其、以色列、冰岛、俄罗斯的 24 个国家。 (347 个站点)。 2004 年 11 月至 2006 年 5 月 RSV 赛季 以 1:1 至 15 mg/kg PVZ 或 motavizumab 的间隔 30 天随机分配 | 早产儿≤ 35 周且年龄≤ 6 个月大或 24 个月大≤在过去 6 个月内需要 药物治疗的 CLD PVZ:3298 莫维珠单抗:3315 | 随机分组后随访 150 天(最后一次预定剂量后 30 天), 定义了 AE 和 SAE。 AE 与研究药物的关系未说明 死亡率 PVZ 4 (0.1%),莫维珠单抗 8 (0.2%)。没有人被认为与研究药物相关。 事件: ≥1 AE 精神疾病 * 皮肤和皮下疾病 *** 注射部位反应 ≥1 AE,3 级为最高严重程度 ≥1 4 级 AE ≥1 SAE 导致药物停药 * 烦躁不安、嗜睡、不安和易怒; | 我 | 好 AE 与研究药物的关系未说明 |
| Feltes 等人,2003 年脚注80 由 MedImmune 支持 | RCT International – 美国、加拿大、瑞典、波兰、法国、英国 (76 个站点) 1998-2002 每 30 天以 1:1 的比例随机分配至 PVZ (15 mg/kg) 或安慰剂,共 5 剂 | ≤24 个月大患有 hsCHD 的婴儿 每个孩子只随访一个季节 PVZ:639 安慰剂:648 | 随后 150 天 (最后一次预定剂量后 30 天)。由盲法研究者报告和评估的儿童医疗状况与研究药物相关的任何不良变化。定义 AE 和 SAE。 3.3% 的 PVZ,4.2% 的安慰剂死亡;没有一个归因于 PVZ。 不良事件类别: 不良事件类别:否。AE 不良事件类别:否。AE 不良事件类别:心血管 不良事件类别:呼吸系统 不良事件类别: 需要医疗干预 不良事件类别: 严重不良事件 不良事件类别: 死亡人数 不良事件类别: 相关 AE 不良事件类别: 导致永久停药 不良事件类别: 相关 SAE * 当从分析中去除 RSV 住院期间报告的严重 AE 时,P 值为 0.043 | 我 | 好 |
| Feltes 等人,2011 年脚注216 由 MedImmune 支持 | RCT International – 北美、欧洲、保加利亚、以色列、黎巴嫩、俄罗斯 的 16 个国家(134 个站点) 2005-6、2007-8 motavizumab 与 PVZ 的非劣效性研究 随机分配 1:1 至 15 mg/kg PVZ 或 MVZ,每 30 天一次,共 5 剂 | ≤ 24 个月 hsCHD 的儿童 莫维珠单抗:624 | 随后 150 天 (最后一次给药后 30 天)。由盲法研究者报告和评估的儿童医疗状况与研究药物相关的任何不良变化。定义 AE 和 SAE。 结果 n (%): ≥ 1 AE: ≥ 1 相关 AE: ≥ 1 SAE: ≥ 1 相关 SAE: ≥ 1 项导致研究药物停药的相关 AE: 死亡人数**: * 与研究药物 | 我 | 好 |
| Fernandez 等人,2010 年脚注215 由 MedImmune 资助 | RTC International 南半球 – 智利、新西兰、澳大利亚 (18 个站点) 2006-7 Motavizumab (M) 或 PVZ (P) | 早产儿 ≤35 wGAk 且年龄 ≤6 个月或 年龄 ≤24 个月且在过去 6 个月内需要药物治疗 的早产儿 CLD MMPPP: 83 PPMMM:84 MMMMM: 93 (未提取最后一组的数据) | 从随机分组到研究第 150 天,定义 AE 和 SAE 并评估 因果关系 所有 4 组的 AE 类型相似 AE (n): 第 3 剂前 MVZ ≥ 1 AE: 第 3 剂前 MVZ ≥ 1 个相关 AE : 第 3 剂前 MVZ ≥ 1 SAE: 第 3 剂前 MVZ ≥ 1 相关 SAE: 第 3 剂前 MVZ 导致停药的 AE: 第 3 剂前 MVZ 死亡: 第 3 剂前 MVZ * 葡萄球菌烫伤样皮肤综合征 | 我 | 好 |
| IMPACT-RSV 研究组 1998脚注48 资金:未说明;来自 MedImmune 的贡献 | RCT International(加拿大 9 个研究中心,英国 11 个研究中心,美国 119 个研究中心) 1996–1997 RSV 赛季 每 30 天以 2:1 的比例随机分配至 PVZ 15 mg/kg 或安慰剂;共 5 剂 | 在 ≤35 wGA 出生且在 RSV 季节 开始时年龄≤ 6 个月的儿童,或 在过去 6 个月内 年龄 ≤24 个月且患有 BPD 需要持续医疗管理 PVZ:1002 | 从随机分组开始随访 150 天 (最后一次预定注射后 30 天) 在整个研究期间报告了 AE。由研究人员评估严重程度和与研究药物的潜在关系。 AE 和 SAE 未定义 盲法研究者判断为与研究药物相关的报告 AE 的儿童人数:安慰剂 (10%) PVZ (11%)。因 PVZ 相关 AE 而停止注射的情况很少见 (0.3%)。 注射部位反应包括红斑、疼痛、硬结/肿胀、瘀伤。这些通常是轻微的,持续时间短;没有一个是严重的。 事件 发烧: 紧张: 注射部位反应: 腹泻: 皮疹: AST 升高: URI: 肝功能异常†: ALT 增加: 呕吐: 咳嗽: 鼻炎: 缩写: AST,天冬氨酸氨基转移酶;URI,上呼吸道 | 我 | 好 |
| Makari 等人,2014 年脚注212 资助 MedImmune | RTC Multicenter USA (51 个站点) 2005-2007 随机分配 1:1 至 15 mg/kg PVZ | 年龄≤ 24 个月或出生时 ≤ wGA 且年龄≤ 6 个月的 CLD 儿童 211:液体 | 监测至第 150 天(仅报告 SAE) 定义 SAE 并评估 因果关系 SAE 发生率无差异 冻干 PVZ 组中有一名受试者死于窒息;死亡被认为与 PVZ 无关。 没有一个 SAE 被确定与 PVZ 有关 SAE (n, 9%) ≥1 SAE 的受试者: SAE: 毛细支气管炎: 呼吸窘迫: 其他相关: 病毒感染: 其他感染: 胃肠炎: 脱水: 畸形: 癫痫发作: 其他 *: * 腹股沟疝 (2)、脐疝、生长迟缓、肛裂、胃食管反流、肾积水 (各 1) | 我 | 好 |
| Robbie 等人 2014脚注213 由 MedImmune 支持 | 2 期 RCT 交叉设计 多中心 美国(21 个站点) 2002 年 11 月至 2003 年 2 月 第 0 天随机分配 1:1 至 15 mg/kg 液体 PVZ 或冻干 PVZ;在第 30 天交叉到替代制剂,一剂 | 出生≤ 35 wGA 的 ≤ 6 个月早产儿 液体 PVZ 第 0 天:75 | 每次研究剂量后 30 天随访。(第 60 天后,在赛季剩余时间内接受冻干 PVZ)。 SAE 定义和与研究药物的关系评估 两组 的 AE 相似 没有 SAE 被认为与 PVZ 相关 研究期间没有发生死亡 AE,n (%) 患有≥ AE的婴儿: AE 数量: 与 PVZ 相关的 AE: 发热: 注射液: 肺炎: 患有≥ SAE 的婴儿: SAE 数量: RSV: 发热: 胃肠道: 肺炎: 呼吸暂停: 脱水: UTI: 与 PVZ 相关的 SAE: | 我 | 好 |
| Haerskjold 等人,2016 年脚注217 由 艾伯维 资助 | 基于人群的队列研究 瑞典、丹麦 1999-2010 年 | 1,351,265 名儿童 1999 年 1 月 1 日至 2010 年 12 月 31 日出生(丹麦)或 2005 年 7 月 1 日至 2010 年 12 月 31 日(瑞典) 暴露于 PVZ:(早产儿、BPD、HSCHD) 平均 PVZ 剂量:瑞典 5.4 | 随后于 2010 年 12 月 31 日在丹麦和 2011 年 12 月 31 日在瑞典举行。 自身免疫定义。 PVZ 暴露后自身免疫性疾病的风险没有显著增加(根据年龄和国家调整的风险比:1.54;95% 置信区间 0.80-2.95)。 未暴露:0.54% 的瑞典儿童和 0.60% 的丹麦儿童患上自身免疫性疾病 暴露:1192 例中有 9 例 (0.76%) 发展为自身免疫性疾病。乳糜泻 (4)、糖尿病 (2)、炎症性肠病 (2)、幼年关节炎 (1) | II-2 | 好 |
| Haerskjold 等人,2017 年脚注218 由 艾伯维 资助 | 基于人群的队列研究 瑞典、 丹麦 1999-2010 来自国家健康登记册的数据 | 1,351,265 名儿童 1999 年 1 月 1 日至 2010 年 12 月 31 日 – 12 月 (丹麦) 或 2005 年 7 月 1 日 – 2010 年 12 月 31 日 (瑞典) 暴露于 PVZ:(早产儿、BPD、HSCHD) 平均 PVZ 剂量: | 随访至 4 岁或研究结束,以先 到者为准 特应性疾病定义 在 总出生队列(风险比 [HR] 1.49;95% 置信区间 [CI] 1.32,1.68)和早产儿亚队列(HR 1.24;95% CI 1.07-1.44)中观察到 PVZ 暴露后哮喘风险增加。 然而,使用确定的倾向评分来平衡混杂因素的事后分析发现,早产儿患哮喘的风险没有增加(HR 0.91;95% CI 0.56,1.48) 特应性皮炎的风险没有增加(HR 1.18;95% CI 0.94,1.48) 过敏性鼻结膜炎的风险没有增加(HR 1.14;95% CI 0.92,1.42) | II-2 | 好 |
| Abushahin 等人,2018 年脚注237 未说明资金 | 描述性单中心队列研究 卡塔尔 2009 年 – 2011 年 3 月 31 日 回顾性;2011 年 11 月 1 日至 2012 年 11 月 1 日 展望 卡塔尔 PVZ 每月 15 mg/kg,共 3-5 剂 | 出生≤ 35 wGA 且年龄< 6 个月或 ≤ 35 wGA 且 2 岁≤患有 BPD 或 hsCHD n= 429 | 在接受 PVZ 期间每月随访一次,最后一次给药后 30 天 注射后 7 天内记录的 AE(过敏反应、发烧、红斑、肿胀、皮疹、咳嗽、喘息、呕吐和/或腹泻) 无 AE 和与 PVZ 相关的死亡。 | III | N/A |
| al-Alaiyan 等人 2015脚注230 由 艾伯维 资助 | 前瞻性单中心观察 性非比较研究 沙特阿拉伯 2000-2001 PVZ 15 mg/kg 每 25-30 天一次,共 7 剂 | 儿童 ≤35 wGA 和 ≤6 个月大或慢性肺病 ≤24 个月大 N= 17 | 每 25-30 天随访一次,持续 7 个月 定义 SAE 并评估与研究药物的关系 5 例患者共 7 例 AE (27.8%);4 例患者 6 例 SAE SAE:毛细支气管炎:3 例(1 例 RSV 阳性,2 例 RSV 阴性);肺炎:1 胸部感染:2 (均为 RSV 阴性) | III | N/A |
| Bjornson 等人,2018 年脚注77 由 艾伯维 资助 | 回顾性多中心观察性比较队列 艾伯塔省全省(2 个中心) 2000-2017 PVZ 每月 15 mg/kg | 267 名 <2 岁患有囊性纤维化的儿童 183 个 PVZ 接收者 平均 4.4 ± 1.5 次注射 84 人未收到 PVZ | 病历 回顾 记录了所有 SAE,包括对 PVZ 的过敏反应。 没有 SAE 与 PVZ 相关 | III | N/A 摘要和方法中提到了 AE,但结果中没有 |
| Borecka 等人,2016 年脚注236 由 艾伯维 资助 | 回顾性观察性多中心登记 波兰 2008-9, 2009-10 | 2008-9: 2008 年 BPD 和 早产 ≤30 wGA 或 2007 年 ≤28 wGA 早产或需要持续药物治疗的严重 BPD 2009-10 年: 1021 名儿童 3241 剂 平均 3.2 ± 1.04 | 医疗记录 回顾 AE 的随访方法和 AE 的定义未说明。未评估因果关系 75.5% 的儿童接受了所有预期的注射 总体:108 例 AE / 3241 剂 (3.33%) 84 名接受者 (8.2%) AE 最常见的 AE:紧张 (40);发烧 (24),部位反应 (15),腹泻 (4),呕吐 (4);其他 = 21 | III | N/A AE 的随访方法和 AE 的定义未说明 |
| Castillo 等人,2017 年脚注226 资助 艾伯维 | 前瞻性国际观察性非比较研究 拉丁美洲 – 阿根廷、智利、哥伦比亚、厄瓜多尔、墨西哥、秘鲁、乌拉圭。 (24 个站点) 2011 年 2 月至 2012 年 9 月每月 PVZ 15 mg/kg,最多 5 剂 | 出生于 ≤35 w GA 或患有 BPD 或 hsCHD 458 名儿童 共 1744 剂 (平均 3.8 ± 1.3 剂) | 在 PVZ 期间的每月访问量;第一次 PVZ 剂量后一年内每月打电话。 定义 AE 和 SAE。评估与 PVZ 的关系 397 例完成了一年的随访。 1165 年。 | III | N/A |
| Chang 等人 2010脚注238 未说明资金 | 回顾性队列 韩国 单中心 2005-2009 15 mg/kg/剂,每 30 天 | 出生≤ 35 wGA 患有慢性肺病,年龄 <2 岁 n=75 | 没有关于随访的信息。AE 未定义 注射后 7 天内记录 3 例患者发现注射部位红斑和肿胀,并在 3 天内消退 | III | N/A |
| Chen JJ 等人,2015 年脚注170 由 艾伯维 资助,MedImmune | 前瞻性多中心 观察登记 加拿大 RSV 季节 2008-2013 PVZ 15 mg/kg,第一剂和第二剂之间间隔 | 早产儿 ≤35 wGA (n = 8224) hsCHD 年龄 <2 岁 (n = 1442) BPD 年龄 < 2 岁 (n = 978) 其他复杂的疾病 (n = 2381) 总计 = 13,025 57,392 剂 给予 92.7% (±16.1%) 的预期注射 | 主动监测 SAE,每月随访一次,直至最后一次 PVZ 给药后 30 天。 定义 AE 和 SAE;因果关系评估 SAE(不包括呼吸道感染住院):52 名婴儿 中有 62 名 PVZ 相关: 14(6 名婴儿):10 名可能(3 名婴儿) 4 名可能(3 名婴儿); 发病率 2.8/10,000 患者月。 (每 10,000 剂 2.4) PVZ 无关:44(42 名婴儿) 与 PVZ 的关系未分类:4(4 名婴儿)记录不完整 由于感知到 AE 而停用 PVZ:20。 9 SAE:3 RIH 与 PVZ 无关;6 个 PVZ 相关(见表);11 例非 SAE:大腿皮疹 (2)、胃肠道不适 (1)、烦躁 (3)、不适 (2) 未指明 (3) 5 例与 PVZ 无关的死亡 患有 PVZ 相关 SAE 的婴儿: 年龄 (m): 18 年龄 (m):0.7 年龄 (m):0.7 年龄 (m): 2.4 年龄 (m): 7.3 年龄 (m): 18 | III | N/A |
| Chi 等人 2014脚注44 资金: 台湾台北麦偕纪念医院和台湾 | 前瞻性单中心观察性非比较研究 台湾 2011-2013 PVZ 每月 15 mg/kg,共 6 剂 | 28 ≤婴儿 wGA:108 29-35 wGA 伴 CLD:19 总计 127 718 剂 | 在接受 PVZ 时每月随访一次,并通过电话随访至定义首次给药 AE 后 12 个月;如果需要就诊,则归类为严重。没有提到 SAE。 无因果关系评估 46 AE 当地: 红斑: 疼痛: 系统的: 发热: 咳嗽: 流涕: 呕吐: 腹泻: 易怒: | III | N/A |
| Groothuis 2001 年脚注224 基金资助: 雅培实验室 | 前瞻性国际观察性非比较研究 15 个北半球国家/地区)( 1998 年 11 月 – 1999 年 3 月 RSV 季节每 30 天 | 早产儿 ≤35 wGA,年龄 ≤6 个月或 BPD,年龄 ≤24 个月,需要医疗干预<在过去 6 个月内 565 人入组,530 人完成学习 | 随访最多 150 天(最后一次给药后 30 天)。 AE 和 SAE 定义 (通过引用)。评估 的与 PVZ 的关系 93.8% 完成了研究 因 AE 停药:11 例。3 例可能或可能与 PVZ 相关:(第 3 剂后立即氧饱和度下降;胃肠炎;腹部和外周水肿) ≥ 1 AE:254 ≥ 1 个相关 AE 相关 AE 更多常见的相关 AE: 注射部位反应 发热:8 / 530 腹泻 紧张/易 相关 SAE | III | N/A |
| Groothuis 2003 年脚注225 技术支持:Abbot Laboratories | 前瞻性国际 观察性非比较研究 欧洲(17 个国家/地区)和沙特阿拉伯 2000 年 10 月至 2001 年 4 月 | 入组时 29-32 wGA 无 CLD 年龄 < 6 个月 285 人注册 24 人未完成 | 每月一次,最后一次给药后 30 天出现。 定义 AE 和 SAE;与评估的研究药物的关系 PVZ 因 2 例 AE 而停药: 胃肠道疾病伴外周水肿和呼吸暂停,中度严重程度,与 PVZ 无关;第 3 次 PVZ 给药后发烧持续 15 小时,中度严重程度,可能与 PVZ 最常见的 AE:鼻炎 (18%)、咳嗽 (10%)、发烧 7%、腹泻、细支气管炎、咽炎(各 5%)。多数 轻度-中度。 事件:发烧 事件: 肠炎 事件:支气管炎和鼻炎 事件:咳嗽 事件:细菌性肺炎和结膜炎 | III | N/A |
| Kashiwagi 等人 2018 年脚注229 由 艾伯维 资助 | 前瞻性多中心上市后监测 日本 2013 年 12 月至 2015 年 12 月 RSV 季节每月 PVZ 15 mg/kg | 接受 PVZ < 24 个月的儿童。 免疫功能低下:167 唐氏综合症:138 (一名患者同时患有两者) 总计 = 304 每季剂量 数(平均值 ±SD): 5.3 (±2.4) | 随访至最后一次给药 后 30 天,定义 AE 和 SAE 并评估与 PVZ 的关系 AE:220 (99 名患者)。33 例(25 例患者)被认为是药物不良反应 (ADR) ADR:25 例患者中 33 例(肺炎 3 例,RSV 感染 3 例,其他感染 11 例,上呼吸道炎症 5 例,哮喘 1 例,腹泻 2 例,杂项 8 例) SADR:11 例患者中 13 例: 在 7 中停止用于 AE。提到了 1 例死亡(感染性休克),但未说明死亡总数。 | III | N/A |
| Lacaze- Masmonteil 等人,2002 年脚注227 资金未说明。Abbott France 认可 | 前瞻性多中心 观察 性非比较研究 法国 1999 年 9 月至 2000 年 1 月 RSV 季节每月 PVZ 15 mg/kg | 早产≤ 32 wGA 且患有 BPD 且年龄< 6 m 或 早产≤ 35 wGA 且年龄< 2 岁 且患有 BPD 并接受长期治疗 547 人注册;516 人至少接受了 1 剂 | 随访至最后一次 PVZ AE 和 SAE 给药后 30 天,未定义。评估与 PVZ 的关系。 10 例死亡 (1.9%): (急性呼吸衰竭新生儿严重慢性肺病患儿 (5 例)、气管切开插管阻塞 (2 例)、术中心脏骤停、百日咳、心循环衰竭 (各 1 例)。 有 15 例 AE 被医生判断为可能与 PVZ 相关。: AE:呼吸暂停 AE:发热 AE:注射部位 AE:过度换气 AE: 虚弱 AE: 呕吐 AE:支气管炎 AE:咳嗽恶化 AE: 荨麻疹 事件总数: | III | N/A |
| Lacaze-Masmonteil 等人,2003 年脚注231 由 Abbott Laboratories 提供支持 | 前瞻性国际观察研究 欧洲和加拿大 1999-2000 RSV 赛季 PVZ 15 mg/kg 每 25-30 天一次,最多 5 剂 | ≤ 2 岁出生时 ≤35 wGA 患有 BPD 且在过去 6 个月内需要医疗管理或被研究者判断为有严重 RSV 感染 风险的儿童 第一季:71 第二季:63 | 如果 PVZ 第一季首次收到 PVZ,则第一季与第二季的事件比较。如果在上一季节 接种了 2 剂疫苗,则≥第二季节 每月跟进一次,直至最后一次注射后 30 天。 定义 AE 和 SAE。评估与 PVZ 的关系 研究 科目数量 ≥1 AE *: ≥1 SAE **: 可能与 PVZ 有关系的 AE: 发烧: 感染: 注射部位反应: 腹泻: 厌食症: 鼻衄: 共济失调: SAE: * 大多数 AE 的严重程度为轻度或中度 (90%),被认为 | III | N/A |
| Manzoni 等人,2017 年脚注221 由 艾伯维 资助 | 前瞻性国际 观察登记 加拿大 (CARESS) 和意大利(未说明站点数量) 2001-2014 RSV 季节每月 PVZ 15 mg/kg | 出生在 ≤35 wGA 的婴儿和患有慢性病且符合 PVZ 条件的婴儿 N= 14,468 | 确定每月 随访 AE 和 SAE,评估与 PVZ 的关系 7 例患者 15 例 SAE。所有超敏反应。另外 49 例与 PVZ 无关的患者的 SAE。 与上述 CHEN 的数据有相当大的重叠。 | III | N/A 与 Chen 等人的数据有显著重叠 |
| Mitchell 等人,2011 年脚注219 基金资助: 雅培实验室 | 前瞻性多中心 观察登记 加拿大 | 符合 PVZ 条件的儿童:5286 仅早产儿:3741 19,485 剂(3.7 剂± 1.5 剂) | 每月随访至 RSV 季节 结束 AE,SAE 未定义 61 SAE,56 = 因呼吸道感染住院)。 | III | N/A 随访细节有限,无 AE 定义,无 AE 细节 |
| Mori 等人,2014 年脚注234 由 AbbVie Inc. 支持 | 前瞻性多中心非比较研究 日本 2011 年 10 月至 2012 年 3 月 在 RSV 季节,PVZ 15 mg/kg, | ≤24 个月龄免疫 功能低下的儿童 28 个科目 平均 6.2 剂 | 随访至最后一次给药后 30 天。 AE 和 SAE 未定义。评估与 PVZ 的关系 最常见的 AE 是上呼吸道感染、胃肠炎和湿疹,发生在 ≥10% 的受试者中。大多数 SAEs 被认为是轻度或中度的。 经历≥ 1 个 AE 经历≥ 1 个 SAE 总支气管炎 (n=28) N (%): 2 胃肠炎 总 (N=28) N (%): 3 脑病、胃穿孔 SAE 至少可能与 PVZ 导致停药 导致死亡 * 脑病 104 d(第 4 剂 PVZ 后) | III | N/A 随访信息少 |
| Null 等人 2005脚注232 来自 MedImmune 的贡献 | 先前 RCT 受试者的前瞻性观察研究 美国多中心 (6) 1997-98 RSV 赛季 PVZ 每 30 天 15 mg/kg 剂量;共 5 剂 | 参与者:来自 RCT IMPACT 1998 第一年 第二年 | IMPACT 研究的开放标签随访:第二季预防 每月和最后一次 PVZ 给药后 30 天随访。 (根据 IMPACT 1998 的定义和评估) 无死亡 与 PVZ 相关的 AE: 注射部位疼痛(轻度): 轻至中度海拔 AST 或 ALT: 发烧: | III | N/A |
| Paes 等人 2012脚注220 基金资助: 雅培实验室 | 加拿大前瞻性多中心登记处 (29 个站点) 2006-2010 RSV 赛季 | 无既往疾病的早产 儿 ≤35 wGA:4880 >35 wGA,无 BPD 或 CHD 但有其他基础疾病:952 总计 5832 22,465 剂 | 每月进行一次电话随访,直到 RSV 季节结束。如果住院,则审查医院记录。 没有提到 AE 8 名婴儿在研究过程中死亡,原因被认为与 PVZ 没有直接关系。 | III | N/A 与 Chen 的数据重叠 |
| Pedraz 2003 年脚注46 基金资助: 雅培实验室 | 观察性多中心前瞻性非干预队列研究 西班牙 2000-2002 | 早产儿 ≤32 wGA 且年龄≤ 6 个月 N= 1919 年 | 每月跟踪一次,而在 PVZ 上有 6 例死亡,与 PVZ 无关 没有提到 AE | III | N/A |
| Pinquier 等人 2009脚注228 由 Abbott Laboratories 资助 | 前瞻性多中心观察性非比较研究 法国 PVZ 15 mg/kg 每 31± 6 天 | 1371 名儿童:早产儿 ≤ 35 wGA:878 名 ≤ 2 岁患有 BPD:104 名 ≤ 2 岁患有 hsCHD 163 其他:226 6257 剂 | 第一次注射后 1 年随访。4、8 和 12 个月时图表审查加电话,12 个月 时就诊AE 的定义未说明 6 例死亡 (潜在的心肺疾病 (3),NEC (1),原因未说明,均患有 CHD (2)。没有归因于 PVZ 的死亡 研究人员报告称,30 例 SAE 可能与 PVZ 相关(24 例来自一个中心)。主要是呼吸道和 ORL 症状。评估委员会对这 30 个项目进行了匿名审查,得出的结论与 PVZ 无关。 未因 AE 停药 | III | N/A AE 的定义未说明,无 AE 类型的详细信息 |
| Saez-Llorens 等人 1998脚注235 未说明资金 | 多国观察性非比较剂量递增研究 美国(7 个地点)、哥斯达黎加(1 个地点)、巴拿马(1 个地点) 未说明学习年份 PVZ 5 毫克/公斤、10 毫克/公斤和 15 毫克/公斤 | 出生体重 ≤ 35 岁且年龄≤ 6 个月或患有 BPD 且年龄≤ 24 个月的婴儿 5 毫克/千克 (11) (2 至 5 剂,间隔 30 天;共 190 剂) | 给药后第 2、14 和 30 天随访。 每次注射当天和最后一次注射后 30 天的尿液分析、AST、ALT、BUN、肌酐、全血细胞计数和分类计数。在所有研究访问期间,评估注射部位的局部反应。 2 例与 PVZ 无关的死亡 研究者判断 3 例患者出现可能与研究药物相关的 AE: | III | N/A |
| 佐治 2005脚注243 未提及的资金 | 调查 多中心 日本 (61 个站点) 2002 年 10 月至 2003 年 3 月 PVZ 每月 15 mg/kg/剂 | 患有 CHD 的婴儿 (n=108) 平均 3.0 ±1.4 剂 | 对使用 PVZ 的机构的问卷调查。 没有随访的详细信息或 AE 的定义。未根据严重性或严重性进行分类 5 例患者 9 例 AE。 无死亡 | III | N/A 问卷不可用;文本和表格之间的 AE 数据存在差异 以上文本中未包含的数据 |
| 西蒙 2011脚注222 由德国Abbott GmbH & Co.支持。 | 德国前瞻性多中心观察登记处 (483 个地点,2002 年至 1354 年,2007 年) 2002-2007 在 RSV 季节每月 PVZ 15 mg/kg/剂量。 | 10,686 名受者 (早产儿、BPD、CHD) 49,608 剂 | 随访至最后一次给药 后 4 周,仅报告 SAE。SAE 未定义。评估了因果关系。 22 例患者 (0.21%) 的 SAE。 3 例死亡:SIDS;发热伴腹泻和呼吸窘迫;复杂 CHD 儿童心脏骤停,评估为可能与 PVZ 无关 (1) 且不可评估 (2) | III | N/A SAE 未定义 |
| 西蒙 2018 (Klin Padiatr)脚注223 由AbbVie Deutschland GmbH & Co资助, | 前瞻性多中心观察登记 德国 2009-2016 在 RSV 季节每月 PVZ 15 mg/kg/剂量。 | 12,729 名受者(早产儿、BPD、HDCHD) 仅报告每个孩子的第一个季节的数据 63,572 剂 每位患者平均 5.0 剂 | 在 PVZ 治疗期间观察到,直到该 RSV 季节的 6 月 30 日。 仅报告了 SAE。定义 SAE 并评估因果关系 报告了 668 例 SAE(每 10,000 剂 105 例)( 与 PVZ 的可能关系:8 例 (每 10,000 剂 1.3 例): 9 人死亡。与 PVZ 无关。 | III | N/A |
| Simon 等人 2018 (Euro J Ped)脚注244 由 AbbVie GmbH 提供支持 | 德国前瞻性多中心(登记处)( 未说明的站点数量) 2009-2016 RSV 季节每月 15 mg/kg PVZ | 唐氏综合症婴儿 年龄 <25 个月:249 其他严重 RSV 疾病高危婴儿:12,480 平均 5.0 剂 | 未描述 的随访 SAE 定义(AE 未报告)。因果关系评估 总体而言,668 次 PVZ 剂量后有 63,572 例 SAE(105 例 SAE/10,000 剂)。 唐氏综合症: 不包括 RSV 相关住院,大多数 SAE (n = 20) 是未检测到 RSV 的 RTI 住院。 没有 SAE 与 PVZ | III | N/A 随访程序不明确;SAE 数据有限 以上文本中未包含的数据 |
| Turti 等人 2012脚注233 | 前瞻性、多中心 非比较研究 俄罗斯(19 个地点) 2009-10 | 100 名符合严重 RSV 感染 高风险标准的儿童出生时体重为 ≤35 wGA,年龄 ≤6 个月或年龄 ≤24 个月患有 BPD 或 hsCHD 总计 = 100 | 每月随访一次,并在定义最后一次 PVZ AE 给药后 30 天和 100 天进行随访,但未定义 SAE。评估与 PVZ 的关系 1 例因非严重特应性皮炎而停药。 AE: 可能与 PVZ 相关的 AE: 鼻炎 : 特应性皮炎 (轻度): SAE: 可能与 PVZ 相关的 SAE: * 44 门科目 | III | N/A |
附录 C:帕利珠单抗有效性:附加数据表
| 研究详细信息 | 总结 | ||||
|---|---|---|---|---|---|
| 研究 | 研究设计 | 参与者 | 主要发现摘要 | 证据级别 | 质量 |
| Gilca 等人,2020 年AppC 脚注‡ 由魁北克省卫生和服务部支持。 | 回顾性队列研究 多中心(魁北克省努纳维克);3 个中心 2013 年 11 月 1 日至 2019 年 6 月 31 日 PZV 预防 RSV 住院的有效性 PVZ 每 28 天一次,第一季干预最多 3 剂,随后的 2 季最多 5 剂。 通过快速抗原检测测试 (RADT)(干预前和干预期间均为 97%)和/或 PCR(干预前 24%,干预期间为 73%)诊断的 RSV。 | 1 < 岁婴儿的整个队列(2012 年 11 月至 2019 年 6 月出生): n=2503 足月健康 (HFT) 婴儿 n=2347 干预时间: HFT 在 RSV 季节开始时< 3 个月大或在 RSV 季节出生,随后至 <1 岁: 469 名(73% 的合格婴儿)接种了 PVZ,237 | 在六个季节中,所有 1 <婴儿的 RSVH 率为 50.2/1000(调整后为 72.6/1000 * 检测不足)。 * 对由于 RADT 敏感性较低而可能漏诊的 RSV 病例进行调整。 干预期:通过比较 RSV 住院率 在接受或未接受 PVZ 的组中,或者在 PVZ 保护或未受保护的日子里,RSVH 没有差异: 未接受 PVZ 的婴儿: 按时接受所有 PVZ 剂量的婴儿: 无保护天数 **: PVZ 保护天数 **: * 1 – 相对风险保护/无保护 x 100% | II-2 | 一般AppC 脚注† 通过将洗脱期视为有 PVZ 保护的天数或没有 PVZ 保护的天数来进行敏感性分析;PVZ 有效性基本没有变化。 病例数量少,不同年份的 RSVH 数量差异很大。 与其他呼吸道病毒的混合感染在受保护和无保护的婴儿中都很常见 |
| |||||
脚注
- 脚注 1
- Bont L、Checchia PA、Fauroux B 等人。定义西方国家婴儿和儿童严重呼吸道合胞病毒感染的流行病学和负担。传染病和治疗。2016 年 8 月 1 日;5(3):271-98.doi:10.1007/s40121-016-0123-0.
- 脚注 2
- Shi T、McAllister DA、O’Brien KL 等人。2015 年幼儿呼吸道合胞病毒引起的急性下呼吸道感染的全球、区域和国家疾病负担估计:一项系统评价和建模研究。柳叶刀。2017 年 9 月 2 日;390(10098):946-58.doi: 10.1016/S0140-6736(17)30938-8.
- 脚注 3
- Mazur NI、Higgins D、Nunes MC 等人。呼吸道合胞病毒疫苗景观:来自墓地和有希望的候选人的经验教训。柳叶刀感染病学 2018 年 10 月;18(10):e295-311 doi: 10.1016/S1473-3099(18)30292-5.
- 脚注 4
- 国家免疫咨询委员会。关于单克隆抗 RSV 抗体 (PVZ) 的推荐用途的声明。Canada Com Dis Rep = Releve des maladies transmissibles au Canada JID – 9303729 2003 [Internet].渥太华 (ON) : 加拿大公共卫生署;2003 年 9 月 15 日 [引用于 2022 年 5 月 10 日]。可从:https://pubmed.ncbi.nlm.nih.gov/14524195/。
- 脚注 5
- 传染病委员会。来自美国儿科学会:政策声明–使用 PVZ 预防呼吸道合胞病毒感染的修改建议。小儿科。2009 年 12 月;124(6):1694-701.doi:10.1542/peds.2009-2345。
- 脚注 6
- 美国儿科学会传染病委员会;美国儿科学会毛细支气管炎指南委员会。更新了因呼吸道合胞病毒感染住院风险增加的婴幼儿的 PVZ 预防指南。小儿科。JID – 0376422。2014 年 8 月;134(2):415-20.doi: 10.1542/peds.2014-1666.
- 脚注 7
- 美国儿科学会传染病委员会;美国儿科学会毛细支气管炎指南委员会。技术报告。更新了因呼吸道合胞病毒感染住院风险增加的婴幼儿的 PVZ 预防指南。小儿科。JID – 0376422。2014 年 8 月;134(2):e620-38。doi:10.1542/peds.2014-1665。
- 脚注 8
- Robinson J.L., Saux NL 预防呼吸道合胞病毒感染住院 [互联网]。渥太华(安大略省):加拿大儿科学会;传染病和免疫委员会;2015 年 9 月 8;20:321-6。[引用时间 2022 年 5 月 10 日]可从:https://cps.ca/documents/position/preventing-hospitalizations-for-rsv-infections。
- 脚注 9
- Ismail SJ、Langley JM、Harris TM 等人。加拿大国家免疫咨询委员会 (NACI):疫苗和免疫的循证决策。疫苗。2010 年 4 月 19 日;28:A58-A63。doi:10.1016/j.vaccine.2010.02.035.
- 脚注 10
- Shea BJ、Grimshaw JM、Wells GA 等人。AMSTAR 的开发:一种评估系统评价方法学质量的测量工具。BMC 医学研究方法。2007 年 2 月 15;7。https://doi.org/10.1186/1471-2288-7-10。
- 脚注 11
- Wingert A、Pillay J、Moore DL 等人。因呼吸道合胞病毒住院的婴幼儿的疾病负担。Can Commun Dis Rep. 2021 年 9 月 10 日;47(9):381-396.doi:10.14745/ccdr.v47i09a05。
- 脚注 12
- 国家免疫咨询委员会。关于 PVZ 预防对减少婴儿呼吸道合胞病毒相关并发症影响的 NACI 文献综述。2021.
- 脚注 13
- Ismail SJ、Hardy K、Tunis MC 等人。在疫苗计划建议中系统考虑道德、一般、可行性和可接受性的框架。疫苗。2020 年 8 月 10 日;38(36):5861.doi:10.1016/j.vaccine.2020.05.051.
- 脚注 14
- 美国儿科学会,传染病委员会。红皮书 (2018):传染病委员会报告,第 31 版 [互联网]。伊塔斯卡(伊利诺伊州):美国儿科学会 2018:2018:682-692 [引用时间 2022 年 5 月 10 日]。可从:https://seciss.facmed.unam.mx/wp-content/uploads/2021/02/Red-Book-31th-Edition.pdf。
- 脚注 15
- 尚泽 DL、兰利 JM、谭 TW。加拿大儿童因流感和其他病毒性呼吸道疾病住院。儿科传染病杂志。2006 年 9 月 1 日;25(9):795–800.doi: 10.1097/01.inf.0000232632.86800.8c.
- 脚注 16
- Hall C, Weinberg G, Blumkin A, et al. 24 个月以下儿童的呼吸道合胞病毒相关住院。小儿科。2013 年 8 月;132(2):e341-8 http://dx.doi.org/10.1542/peds.2013-0303。
- 脚注 17
- Pisesky A、Benchimol EI、Wong CA 等人。加拿大安大略省儿童因呼吸道合胞病毒感染住院的发生率:一项使用经过验证的卫生管理数据的基于人群的研究。公共科学图书馆一号。2016 年 3 月 9 日;11(3):e0150416。doi: 10.1371/journal.pone.0150416.
- 脚注 18
- Scheltema NM, Gentile A, Lucion F, et al. 幼儿全球呼吸道合胞病毒相关死亡率 (RSV GOLD):回顾性病例系列。柳叶刀全球健康。2017 年 10 月 5 日;5(10):e984-e991。doi: 10.1016/S2214-109X(17)30344-3.
- 脚注 19
- Tam J, Papenburg J, Fanella S, et al. 加拿大儿科研究人员感染合作网络 2003-2013 年加拿大儿科患者呼吸道合胞病毒相关死亡研究。Clin Infect Dis. 2019 年 1 月 1 日;68(1):113-9.http://dx.doi.org/10.1093/cid/ciy413。
- 脚注 20
- Kua KP, Lee S. PVZ 在患有囊性纤维化的婴幼儿中的安全性和有效性的系统评价。药物。2017 年 6 月;37(6):755-69.http://dx.doi.org/10.1002/phar.1936。
- 脚注 21
- 慢性疾病、染色体异常和先天性畸形是呼吸道合胞病毒住院的危险因素:一项基于人群的队列研究。Clin Infect Dis. 2012 年 3 月;54(6):810-7.http://dx.doi.org/10.1093/cid/cir928。
- 脚注 22
- Manzoni P、Figueras-Aloy J、Simoes EAF 等人。定义慢性病儿童严重呼吸道合胞病毒感染的发病率和相关发病率和死亡率。传染病和治疗。2017 年 9 月;6(3):383-411.doi:10.1007/s40121-017-0160-3。
- 脚注 23
- Banerji A, Panzov V, Young M, et al. 加拿大北极地区婴儿下呼吸道感染的住院率:一项队列研究。CMAJ 开放。2016 年 10 月 18 日;4(4):E615-22。https://dx.doi.org/10.9778/cmajo.20150051。
- 脚注 24
- Shi T, Denouel A, Tietjen AK, et al. 2015 年老年人呼吸道合胞病毒相关急性呼吸道感染的全球疾病负担估计:系统评价和荟萃分析。J Infect Dis. 2020 年 10 月 7 日;222:S577-S583。doi:10.1093/infdis/jiz059。
- 脚注 25
- 免疫和呼吸道传染病中心 (CIRID)。2014-2021 年加拿大呼吸道病毒检测 [互联网]。渥太华(安大略省):加拿大公共卫生署。[引用 2022 年 5 月 10 日]。可从:https://www.canada.ca/en/public-health/services/surveillance/respiratory-virus-detections-canada.html。
- 脚注 26
- Doucette A, 江 XH, Fryzek J, et al.1997-2012 年美国全国代表性数据库中高危婴儿呼吸道合胞病毒和细支气管炎住院率的趋势。公共科学图书馆一号。2016 年 4 月 6 日;11(4):e0152208。doi:10.1371/journal.pone.0152208。
- 脚注 27
- Farber HJ、Buckwold FJ、Lachman B 等人观察到 PVZ 对 29-36 周妊娠婴儿的有效性。小儿科。2016 年 8 月;138(2):e20160627。doi:10.1542/peds.2016-0627。
- 脚注 28
- Helfrich AM、Nylund CM、Eberly MD 等。胎龄 33-36+6 周出生的健康晚期早产儿患呼吸道合胞病毒住院的风险更高。Early Hum Dev. 2015 年 9 月;91(9):541-6.doi: 10.1016/j.earlhumdev.2015.06.009.
- 脚注 29
- Fauroux B, Gouyon JB, Roze JC, et al. 无支气管肺发育不良的妊娠小于 33 周早产儿的呼吸系统发病率:CASTOR 研究队列的 12 个月随访。流行病菌感染。2014 年 7 月;142(7):1362-74.doi:10.1017/S0950268813001738。
- 脚注 30
- Ambrose CS, Anderson EJ, Simoes EAF, et al. 美国妊娠 32-35 周出生未接受免疫预防的早产儿呼吸道合胞病毒病。儿科感染疾病杂志 2014 年 6 月;33(6):576-82.doi: 10.1097/INF.00000000000000219.
- 脚注 31
- Blanken MO, Korsten K, Achten NB, et al. 中度早产儿出生后第一年复发性喘息危险因素的人群归因风险。Paediatr Perinat Epidemiol.2016 年 7 月;30(4):376-85.doi:10.1111/ppe.12295.
- 脚注 32
- Carbonell-Estrany X, Perez-Yarza EG, Garcia LS, et al. 早产儿呼吸道合胞病毒住院的长期负担和呼吸影响 – SPRING 研究。公共科学图书馆一号。2015 年 5 月 8 日;10(5):e0125422。doi:10.1371/journal.pone.0125422.
- 脚注 33
- Korsten K, Blanken MO, Nibbelke EE, et al. 晚期早产儿 RSV 住院预测模型:一项更新和验证研究。早期嗡嗡声开发 2016 年 4 月;95:35-40。doi: 10.1016/j.earlhumdev.2016.01.020.
- 脚注 34
- Ryan VMJ、Langley JM、Dodds L 等人估计妊娠 32-35 周出生的婴儿在出生后第一年与呼吸道合胞病毒相关的住院率。儿科感染疾病杂志 2016 年 8 月;35(8):851-855.doi: 10.1097/INF.00000000000001186.
- 脚注 35
- Straňák Z、Saliba E、Kosma P 等人。胎龄 33 至 35 周出生婴儿 RSV LRTI 住院的预测因子:一项大型多国研究 (PONI)。公共科学图书馆一号。2016 年 6 月 16 日;11(6):e0157446。doi:10.1371/journal.pone.0157446。
- 脚注 36
- Zomer-Kooijker K, Uiterwaal CSPM, van der Gugten AC, et al. 足月儿肺功能下降先于严重的呼吸道合胞病毒感染和呼吸道合胞病毒后喘息。Eur Respir J. 2014 年 9 月;44(3):666-74.doi:10.1183/09031936.00009314。
- 脚注 37
- McLaurin KK、Farr AM、Wade SW 等。足月儿和早产儿的呼吸道合胞病毒住院结果和费用。J 佩里纳托尔。2016 年 11 月;36(11):990-6.doi:10.1038/jp.2016.113.
- 脚注 38
- Griffin MP, Yuan Y, Takas T, et al. 单剂量 Nirsevimab 预防早产儿 RSV。N Engl J Med. 2020 年 7 月;30(5);383:415-425.doi: 10.1056/NEJMoa1913556.
- 脚注 39
- Papenburg J、Defoy I、Massé E 等人。取消 PVZ 免疫预防对加拿大魁北克省胎龄 33 至 35 周婴儿呼吸道合胞病毒 (RSV) 住院率的影响:RSV-魁北克研究。儿科感染疾病协会 2021 年 4 月 3 日;10(3):237-244.doi:10.1093/jpids/piaa046。
- 脚注 40
- Anderson EJ、Carbonell-Estrany X、Blanken M 等人。在多个呼吸道合胞病毒季节出生的 33-35 周胎龄婴儿的严重呼吸道合胞病毒病负担。儿科感染疾病杂志 2017a 年 2 月;36(2):160-7.doi: 10.1097/INF.00000000000001377.
- 脚注 41
- Notario G, Vo P, Gooch K, et al. 无支气管肺发育不良早产儿的呼吸道合胞病毒相关住院治疗:按胎龄组划分的 IMpact-RSV 试验的亚组疗效分析。儿科健康医学 Ther.2014 年 5 月 30 日;2014(5):43-48.https://doi.org/10.2147/PHMT.S59572。
- 脚注 42
- Stevens TP, Sinkin RA, Hall CB, et al. 呼吸道合胞病毒和妊娠 32 周或更早出生的早产儿:住院和预防的经济影响。Arch Pediatr Adolesc Med. 2000 年 1 月;154:55-61。[引用 2022 年 5 月 10 日]。可从:https://jamanetwork.com/journals/jamapediatrics/fullarticle/348500。
- 脚注 43
- Boyce TG、Mellen BG、Mitchel EF J 等人。Medicaid 儿童呼吸道合胞病毒感染的住院率。儿科杂志。2000 年 12 月;137(6):865-70 doi:10.1067/mpd.2000.110531.
- 脚注 44
- Chi H, Hsu CH, Chang JH, et al.一种新的连续六个月剂量的 PVZ 预防方案,用于预防台湾高危早产儿呼吸道合胞病毒感染。公共科学图书馆一号。2014 年 6 月 27 日;9(6):e100981。doi:10.1371/journal.pone.0100981.
- 脚注 45
- Park HW、Lee BS、Kim AR 等人。胎龄小于 35 周出生的婴儿呼吸道合胞病毒感染的流行病学。儿科感染疾病杂志 2012 年 8 月;31(8):e99-e104。doi: 10.1097/INF.0b013e318257f619.
- 脚注 46
- Pedraz C、Carbonell-Estrany X、Figueras-Aloy J 等人。PVZ 预防对减少早产儿呼吸道合胞病毒住院的影响。儿科感染疾病杂志 2003 年 9 月;22(9):823-7.doi: 10.1097/01.inf.0000086403.50417.7c.
- 脚注 47
- Grimaldi M, Gouyon B, Sagot P, et al. PVZ 对胎龄 <30 周无支气管肺发育不良早产儿的疗效。儿科肺病。2007 年 3 月;42(3):189-92.doi:10.1002/ppul.20503。
- 脚注 48
- IMpact-RSV 的PVZ 是一种人源化呼吸道合胞病毒单克隆抗体,可减少高危婴儿因呼吸道合胞病毒感染而住院的人数。IMpact-RSV 研究组。小儿科。1998 年 9 月;102(3):531-537.[引用 2022 年 5 月 10 日]。可从:https://pubmed.ncbi.nlm.nih.gov/9724660。
- 脚注 49
- Winterstein AG、Knox CA、Kubilis P 等人。中早产儿呼吸道合胞病毒免疫预防的年龄阈值的适当性 – 一项队列研究。美国医学会儿科医师。2013 年 12 月;167(12):1118-24.doi:10.1001/jamapediatrics.2013.2636。
- 脚注 50
- SENTINEL1:一项关于胎龄 29 至 35 周出生且未接受免疫预防的美国婴儿呼吸道合胞病毒住院的观察性研究。Am J Perinatol。2017 年 1 月;34(1):51-51.doi:10.1055/s-0036-1584147。
- 脚注 51
- Rajah B、Sánchez PJ、Garcia-Maurino C 等人。更新后的 PVZ 预防呼吸道合胞病毒感染指南的影响:单中心体验。儿科杂志。2017 年 2 月;181:183-8。doi: 10.1016/j.jpeds.2016.10.074.
- 脚注 52
- Luchsinger V、Ampuero S、Palomino MA 等人。根据临床结果,智利非常年幼的婴儿急性下尿路呼吸道感染中呼吸道合胞病毒和鼻病毒的病毒学特征比较。J Clin Virol。2014 年 9 月;61(1):138-44.doi: 10.1016/j.jcv.2014.06.004.
- 脚注 53
- Caserta MT、Qiu X、Tesini B 等人。婴儿呼吸道合胞病毒感染全球呼吸严重程度评分的制定。J Infect Dis. 2017 年 3 月 1 日;215(5):750-6.doi:10.1093/infdis/jiw624。
- 脚注 54
- Fergie J, Suh M, 江 X, et al. 使用儿科健康信息系统 (PHIS) 的早产儿呼吸道合胞病毒和全因细支气管炎住院。J Infect Dis. 2020 年 7 月 21 日;225(7):1197-1204.doi:10.1093/infdis/jiaa435。
- 脚注 55
- SENTINEL1:29 至 35 周出生且未接受免疫预防的美国婴儿呼吸道合胞病毒住院的 2 季研究。Am J Perinatol。2020 年 3 月;37(4):421-9.doi: 10.1055/s-0039-1681014
- 脚注 56
- Jang MJ, Kim YJ, Hong S, et al. 母乳喂养对住院婴儿呼吸道合胞病毒感染的正相关:一项多中心回顾性研究。韩国儿科杂志。2020 年 4 月;63(4):135-40.doi:10.3345/kjp.2019.00402。
- 脚注 57
- Garcia-Mauriño C, Moore-Clingenpeel M, Thomas J et al. 呼吸道合胞病毒感染婴儿的病毒载量动力学和临床疾病严重程度。J Infect Dis. 2019 年 4 月 19 日;219(8):1207-15.doi:10.1093/infdis/jiy655。
- 脚注 58
- Oz-Alcalay L、Ashkenazi S、Glatman-Freedman A 等人。PVZ 预防时代呼吸道合胞病毒毛细支气管炎住院:需要重新考虑预防时间和资格。Isr Med Assoc J. 2019 年 2 月 1 日;21:110-5 [引用于 2022 年 5 月 10 日]。可从:https://www.semanticscholar.org/paper/Hospitalization-for-Respiratory-Syncytial-Virus-in-Oz-Alcalay- Ashkenazi/eb2d8bda758bc528cd2ffaeaaedb4d7145481905
- 脚注 59
- Midulla F、Nenna R、Scagnolari C 等人。呼吸道合胞病毒基因型如何影响因毛细支气管炎住院的婴儿的临床病程。J Infect Dis. 2019 年 1 月 29 日;219(4):526-34.doi:10.1093/infdis/jiy496。
- 脚注 60
- Figueras-Aloy J、Manzoni P、Paes B 等人。确定无慢性肺病或 CHD 的早产儿严重呼吸道合胞病毒感染的风险以及相关的发病率和死亡率。感染 Dis Ther.2016 年 12 月;5(4):417-52.doi:10.1007/s40121-016-0130-1。
- 脚注 61
- Gouyon JB、Roze JC、Guillermet-Fromentin C 等人。无支气管肺发育不良的早产儿妊娠 <33 周因呼吸道合胞病毒毛细支气管炎住院:CASTOR 研究。流行病菌感染。2013 年 4 月;141(4):816-26.http://dx.doi.org/10.1017/S0950268812001069。
- 脚注 62
- Vu LD, Siefker D, Jones TL, et al. 患有严重呼吸道合胞病毒毛细支气管炎的人类婴儿 2 型呼吸道先天性淋巴细胞水平升高。Am J Respir Crit Care Med. 2019 年 11 月 27 日;200(11):1414-23.http://dx.doi.org/10.1164/rccm.201812-2366OC。
- 脚注 63
- Rodriguez-Gonzalez M, Perez-Reviriego AA, Castellano-Martinez A, et al. 左心室功能障碍和血浆 NT-Probnp 与呼吸道合胞病毒毛细支气管炎的不良进化有关。诊断。2019 年 7 月 27 日;9(3):85.doi:10.3390/diagnostics9030085。
- 脚注 64
- Simões EAF, Ambrose CS, Wu X, et al. 妊娠 32-35 周出生且未接受免疫预防的早产儿呼吸道合胞病毒感染的重症监护病房收治率与年龄的关系。儿科感染疾病杂志 2015 年 3 月;34(3):331.doi: 10.1097/INF.000000000000000566.
- 脚注 65
- Checchia PA、Paes B、Bont L 等人。定义先天性心脏病婴儿严重呼吸道合胞病毒感染的风险以及相关的发病率和死亡率。感染 Dis Ther.2017 年 3 月;6(1):37-56.doi:10.1007/s40121-016-0142-x。
- 脚注 66
- Szabo SM、Gooch KL、Bibby MM 等人。因严重呼吸道合胞病毒感染而住院的幼儿的死亡风险。Paediatr Respir Rev. 2013 年 1 月;13:增刊 2:S1-S8。doi: 10.1016/S1526-0542(12):00095-4.
- 脚注 67
- 加拿大统计局。表:13-10-0425-01 活产婴儿,按妊娠周数 https://doi.org/10.25318/1310042501-eng。
- 脚注 68
- Pignotti MS、Leo MC、Pugi A 等人关于呼吸道合胞病毒病 PVZ 预防适当性的共识会议。儿科肺病。2016 年 10 月;51(10):1088-96.doi:10.1002/ppul.23561。
- 脚注 69
- Hall CB、Weinberg GA、Iwane MK 等人。幼儿呼吸道合胞病毒感染的负担。N Engl J Med. 2009 年;360(6):588-98.doi: 10.1056/NEJMoa0804877
- 脚注 70
- Meissner HC、Bocchini JA、Brady MT 等人。免疫预防在减少呼吸道合胞病毒引起的疾病中的作用。小儿科。2009 年 12 月;124(6):1676-9.doi: 10.1542/peds.2009-2346.
- 脚注 71
- Figueras-Aloy J, Carbonell-Estrany X, Quero-Jimenez J, et al. Flip-2 研究:与胎龄 32 至 35 周在西班牙出生的早产儿需要住院治疗的呼吸道合胞病毒感染相关的危险因素。儿科感染疾病杂志 2008 年 9 月;27(9):788-93.doi: 10.1097/INF.0b013e3181710990.
- 脚注 72
- Paes B、Fauroux B、Figueras-Aloy J 等人。定义慢性肺病婴儿严重呼吸道合胞病毒感染的风险以及相关的发病率和死亡率。感染 Dis Ther.2016 年 12 月;5(4):453-471.doi:10.1007/s40121-016-0137-7。
- 脚注 73
- Winterstein AG、Choi Y、Meissner HC。年龄与慢性肺病早产儿呼吸道合胞病毒住院风险的相关性。美国医学会儿科医师。2018;172(2):154-60.doi:10.1001/jamapediatrics.2017.3792。
- 脚注 74
- Checchia PA、Nalysnyk L、Fernandes AW 等人。接受 PVZ 预防的严重呼吸道合胞病毒感染高危婴儿的死亡率和发病率:系统文献综述和荟萃分析。Crit Care Med. 2011 年 9 月;12(5):580-8.doi: 10.1097/PCC.0b013e3182070990
- 脚注 75
- Hama I、Takahashi S、Nakamura T 等人。先天性囊性肺病婴儿呼吸道合胞病毒感染的风险。儿科国际。2015 年 4 月;57(2):253-7.doi:10.1111/ped.12544。
- 脚注 76
- Drummond D、Thumerelle C、Reix P 等人。PVZ 对儿童间质性肺病儿童的有效性:法国经验。儿科肺病。2016 年 7 月;51(7):688-95.doi:10.1002/ppul.23354。
- 脚注 77
- Bjornson C, Chan P, Li A, et al. 囊性纤维化婴儿呼吸道合胞病毒的 PVZ 预防:有必要吗?Eur J Clin Microbiol Infect Dis. 2018 年 6 月;37(6):1113-8.doi:10.1007/s10096-018-3225-7。
- 脚注 78
- Groves HE、Jenkins L、Macfarlane M 等人。PVZ 预防北爱尔兰囊性纤维化婴儿呼吸道合胞病毒感染的疗效和长期结果。儿科肺病。2016 年 4 月;51(4):379-85.doi:10.1002/ppul.23376。
- 脚注 79
- Chu PY, Hornik CP, Li JS, et al. 1997-2012 年血流动力学显着心脏病儿童的呼吸道合胞病毒住院趋势。哈科尔·杨。2017 年 1 月;27(1):16-25.doi: 10.1017/S1047951116000470.
- 脚注 80
- Feltes TF, Cabalka AK, Meissner HC, et al. PVZ 预防可减少患有血流动力学显着先天性心脏病的幼儿因呼吸道合胞病毒而住院的人数。儿科杂志。2003 年 10 月;143(4):532-40.doi:10.1067/s0022-3476(03)00454-2。
- 脚注 81
- Chiu SN, Shao PL, Chen HC, et al.亚热带地区紫绀型先天性心脏病的呼吸道合胞病毒感染风险。儿科杂志。2016 年 4 月;171:25-30e1. doi: 10.1016/j.jpeds.2015.12.029.
- 脚注 82
- Resch B、Sommer C、Nuijten MJC 等人。PVZ 对高危儿童呼吸道合胞病毒感染的成本效益,基于奥地利的长期流行病学数据。儿科感染疾病杂志,2012 年 1 月;31(1):e1-8。doi: 10.1097/INF.0b013e318235455b.
- 脚注 83
- 贝克豪斯 AA,卡斯特罗-罗德里格斯 JA。唐氏综合症和严重 RSV 感染的风险:荟萃分析。小儿科。2018 年 9 月 1 日;142(3):e20180225。doi:10.1542/peds.2018-0225。
- 脚注 84
- Stagliano DR、Nylund CM、Eide MB 等人。患有唐氏综合症的儿童是严重呼吸道合胞病毒病的高危人群。儿科杂志。2015 年 3 月;166(3):703-9.doi:10.1016/j.jpeds.2014.11.058.
- 脚注 85
- Feldman AG、Sundaram SS、Beaty BL 等人。小儿肝移植后前 2 年因呼吸道合胞病毒和疫苗可预防感染住院。儿科杂志。2017 年 3 月;182:232,238.e1。doi:10.1016/j.jpeds.2016.12.021.
- 脚注 86
- 呼吸道合胞病毒和季节性流感在镰状细胞病儿童中引起类似的疾病。小儿血癌。2014 年 5 月;61(5):875-8.doi:10.1002/pbc.24887。
- 脚注 87
- El Saleeby CM, Somes GW, DeVincenzo JP, et al. 癌症儿童严重呼吸道合胞病毒病的危险因素:淋巴细胞减少症和年轻的重要性。小儿科。2008 年 2 月;121(2):235-243.doi:10.1542/peds.2007-1102。
- 脚注 88
- Kim YJ, Guthrie KA, Waghmare A, et al. 造血细胞移植受者的呼吸道合胞病毒:决定进展为下呼吸道疾病的因素。J Infect Dis. 2014 年 4 月 15 日;209(8):1195-204.doi:10.1093/infdis/jit832。
- 脚注 89
- O’Brien KL、Chandran A、Weatherholtz R 等人。Motavizumab 预防健康美洲原住民婴儿呼吸道合胞病毒病的疗效:一项 3 期随机双盲安慰剂对照试验。柳叶刀感染病学 2015 年 12 月;15(12):1398-408.doi: 10.1016/S1473-3099(15)00247-9.
- 脚注 90
- Gilca R、Billard MN、Zafack J 等人。PVZ 免疫预防预防加拿大魁北克省努纳维克极地地区健康足月<6 个月大婴儿呼吸道合胞病毒住院的有效性。Prev Med Rep. 2020 年 12 月;20:101180。doi:10.1016/j.pmedr.2020.101180.
- 脚注 91
- Banerji A、Lanctot KL、Paes BA 等人。加拿大因纽特婴儿呼吸道合胞病毒病住院费用与 PVZ 预防的比较。儿科感染疾病杂志 2009 年 8 月;28(8):702-6.doi: 10.1097/INF.0b013e31819df78e.
- 脚注 92
- Singleton R、Dooley L、Bruden D 等人。PVZ 预防对高危阿拉斯加土著婴儿呼吸道合胞病毒住院的影响。Pediatr Infect Dis J. 2003 年 6 月;22(6):540-5.http://dx.doi.org/10.1097/00006454-200306000-00010。
- 脚注 93
- Kim L, Rha B, Abramson JS, et al. 确定疫苗引入之前美国呼吸道合胞病毒病流行病学的差距。CID. 2017 年 9 月 15 日;65(6):1020-5.doi:10.1093/cid/cix432。
- 脚注 94
- Fauroux B、Simoes EAF、Checchia PA 等人。与儿童早期呼吸道合胞病毒感染相关的负担和长期呼吸道发病率。感染 Dis Ther.2017 年 6 月;6(2):173-97.doi:10.1007/s40121-017-0151-4.
- 脚注 95
- 呼吸道合胞病毒和哮喘起源:因果关系,还是共同易感性?。J Infect Dis. 2019 年 7 月 19 日;220(4):547-549.doi:10.1093/infdis/jiy672。
- 脚注 96
- Chawes BLK, Poorisrisak P, Johnston SL, et al. 新生儿支气管高反应性先于婴儿急性严重病毒性毛细支气管炎。J 过敏临床免疫学。2012 年 8 月;130(2):354-61.doi: 10.1016/j.jaci.2012.04.045.
- 脚注 97
- Bonnelykke K, Vissing NH, Sevelsted A, et al. 早期呼吸道感染与以后哮喘之间的关联与病毒类型无关。J 过敏临床免疫学。2015 年 7 月;136(1):81-6.doi: 10.1016/j.jaci.2015.02.024.
- 脚注 98
- Driscoll AJ、Arshad SH、Bont L 等人。早期呼吸道合胞病毒 下呼吸道疾病会导致儿童早期反复喘息和哮喘吗?对世界卫生组织赞助会议的证据和未来研究指南的批判性审查。疫苗。2020 年 3 月 4 日;38(11):2435-48.doi:10.1016/j.vaccine.2020.01.020.
- 脚注 99
- Backman K, Piippo-Savolainen E, Ollikainen H, et al. 成人在婴儿 RSV 毛细支气管炎后面临更高的哮喘风险,并且在 RSV 肺炎后呼吸健康相关的生活质量下降。儿科学报。2014 年 8 月;103(8):850-5.doi:10.1111/apa.12662。
- 脚注 100
- Backman K、Ollikainen H、Piippo-Savolainen E 等人。儿童早期病毒性喘息发作后成年期的哮喘和肺功能。Clin Exp 过敏。2018 年 2 月;48(2):138-46.doi:10.1111/cea.13062。
- 脚注 101
- 婴儿期 RSV 住院会增加无特应性易感性的晚期早产儿在 6 岁时发生喘息的风险。Eur J 儿科杂志。2019 年 4 月;178(4):455-62.doi:10.1007/s00431-018-03309-0.
- 脚注 102
- Mejias A、Wu B、Tandon N 等人。足月婴儿呼吸道合胞病毒感染后儿童喘息和哮喘的风险。儿科过敏免疫学。2020 年 1 月;31(1):47-56.doi: 10.1111/pai.13131.
- 脚注 103
- Henderson FW、Collier AM、Clyde WA Jr 等人。呼吸道合胞病毒感染、再感染和免疫。一项针对幼儿的前瞻性纵向研究。N Engl J Med. 1979 年 3 月 8 日;300(10):530-4.doi:10.1056/NEJM197903083001004。
- 脚注 104
- Glezen WP、Taber LH、Frank AL 等人。原发性感染和呼吸道合胞病毒再感染的风险。Am J Dis Child. 1986 年 6 月;140(6):543-6.doi: 10.1001/archpedi.1986.02140200053026.
- 脚注 105
- CB 厅。呼吸道合胞病毒和副流感病毒。N Engl J Med. 2001 年 6 月 21 日;344(25):1917-28.doi:10.1056/NEJM200106213442507。
- 脚注 106
- Pangesti KNA, Abd El Ghany M, Walsh MG, et al. 呼吸道合胞病毒的分子流行病学。Rev Med Virol.2018 年 3 月;28(2):1002/RMV.1968。doi:10.1002/rmv.1968。
- 脚注 107
- Groothuis JR、Gutierrez KM、Lauer BA。支气管肺发育不良儿童的呼吸道合胞病毒感染。小儿科。1988 年 8 月;82(2):199-203.[引用 2022 年 5 月 10 日]。可从:https://pubmed.ncbi.nlm.nih.gov/3399292/。
- 脚注 108
- Carbonell-Estrany X, Quero J, Bustos G, et al. 妊娠 33 周以下早产儿因呼吸道合胞病毒感染而再住院:一项前瞻性研究。Pediatr Infect Dis J. 2000 年 7 月;19(7):592-7.doi: 10.1097/00006454-200007000-00002.
- 脚注 109
- Carbonell-Estrany X,Quero J,IRIS 研究组。连续两个季节出生的早产儿呼吸道合胞病毒感染的住院率。儿科感染疾病杂志 2001 年 9 月;20(9):874-9.doi:10.1097/00006454-200109000-00010。
- 脚注 110
- Pedersen O、Herskind AM、Kamper J 等人。丹麦极低胎龄或出生体重婴儿呼吸道合胞病毒感染再住院。Acta Paediatr Jpn Overs Ed. 2003 年;92(2):240-2.doi: 10.1111/j.1651-2227.2003.tb00533.x.
- 脚注 111
- Blanken MO, Rovers MM, Molenaar JM, et al. 健康早产儿的呼吸道合胞病毒和复发性喘息。N Engl J Med. 2013 年 5 月 9;368:1791-9。doi: 10.1056/NEJMoa1211917.
- 脚注 112
- Yamaguchi M, Sano Y, Dapat IC, et al. 在日本连续八个流行季节中,由于人类呼吸道合胞病毒基因型的出现,儿童反复感染的频率很高。J 临床微生物学。2011 年 3 月;49(3):1034-40.doi:10.1128/JCM.02132-10。
- 脚注 113
- Okamoto M, Dapat CP, Sandagon AMD, et al. 菲律宾 B 亚组反复感染儿童呼吸道合胞病毒的分子特征。J Infect Dis. 2018 年 8 月 24 日;218(7):1045-53.doi:10.1093/infdis/jiy256。
- 脚注 114
- Simões EA、King SJ、Lehr MV 等人早产双胞胎和三胞胎。严重呼吸道合胞病毒感染的高危人群。Am J Dis Child. 1993 年 3 月;147(3):303-6.doi: 10.1001/archpedi.1993.02160270065020.
- 脚注 115
- Resch B、Pasnocht A、Gusenleitner W 等人。29-36 周胎龄早产儿呼吸系统疾病和呼吸道合胞病毒感染的再住院治疗。J 感染。2005 年 6 月;50(5):397-403.doi:10.1016/j.jinf.2004.06.015.
- 脚注 116
- Figueras-Aloy J, Carbonell-Estrany X, Quero J, et al. 西班牙胎龄 33-35 周出生的早产儿需要住院治疗的呼吸道合胞病毒感染相关危险因素的病例对照研究。儿科感染疾病杂志 2004 年 9 月;23(9):815-20.doi: 10.1097/01.inf.0000136869.21397.6b.
- 脚注 117
- Dotan M、Ashkenazi-Hoffnung L、Samra Z 等人。双胞胎因呼吸道合胞病毒毛细支气管炎住院和疾病严重程度。Isr Med Assoc J. 2013;15:701-4.[引用 2022 年 5 月 10 日]。可从:https://www.ima.org.il/MedicineIMAJ/viewarticle.aspx?year=2013&month=11&page=701。
- 脚注 118
- Groothuis J、Bauman J、Malinoski F 等人。预防 RSV 院内感染的策略。J 佩里纳托尔。2008 年 5 月;28(5):319-23.doi: 10.1038/jp.2008.37.
- 脚注 119
- Katz BZ, Sullivan C. 三级护理新生儿重症监护病房的呼吸道合胞病毒预防。Pediatr Infect Dis J. 2009 年 9 月;28(9):842,844.doi: 10.1097/INF.0b013e3181a0ad01.
- 脚注 120
- Ohler KH, Pham JT. 初始预防性 PVZ 给药对新生儿呼吸道合胞病毒住院治疗的时间比较。Am J Health Syst Pharm. 2013 年 8 月 1 日;70(15):1342-6.doi:10.2146/ajhp120526。
- 脚注 121
- Zembles TN、Gaertner KM、Gutzeit MF 等。在儿科医院实施美国儿科学会 PVZ 预防指南。Am J Health-Syst Pharm. 2016 年 3 月 15 日;73(6):405-8.doi:10.2146/ajhp150499.
- 脚注 122
- Harris RP、Helfand M、Woolf SH 等人。美国预防服务工作组的当前方法:流程回顾。美国预防医学杂志 2001 年 4 月;20:21-35。doi:10.1016/s0749-3797(01)00261-6。
- 脚注 123
- 英格兰公共卫生部。绿皮书第 2 部分:疾病、疫苗接种和疫苗。第 27a 章:呼吸道合胞病毒。2015. [引用 2022 年 5 月 10 日]。可从:https://assets.publishing.service.gov.uk/government/uploads/system/uploads/attachment_data/file/458469/Green_Book_Chapter_27a_v2_0W.PDF。
- 脚注 124
- Abadesso C、Almeida HI、Virella D 等人。使用 PVZ 控制新生儿重症监护病房合胞体呼吸道病毒的爆发。J Hosp 感染。2004 年 9 月;58(1):38-41.doi: 10.1016/j.jhin.2004.04.024.
- 脚注 125
- 新生儿重症监护病房呼吸道合胞病毒爆发:感染控制措施加 PVZ 使用的影响。抗微生物药物抵抗感染控制。2012 年 5 月 2;1:16。doi:10.1186/2047-2994-1-16.
- 脚注 126
- Hammoud MS、Al-Taiar A、Raina A 等人。使用 PVZ 与其他感染控制措施来控制新生儿监护病房的呼吸道合胞病毒爆发。J Trop 儿科杂志。2016 年 10 月;62(5):409-14.doi:10.1093/tropej/fmw025
- 脚注 127
- Silva DG、Almeida FJ、Arnoni MV 等人。在新生儿重症监护病房中,新型基因型 On-1 和 Na-2 连续两次呼吸道合胞病毒暴发的首次报告。儿科杂志。2020 年 3 月至 4 月;96(2):233-9.doi:10.1016/j.jped.2018.10.014.
- 脚注 128
- Dizdar EA, Aydemir C, Erdeve O, et al. 在新生儿重症监护病房中通过快速筛查定义的呼吸道合胞病毒暴发。J Hosp 感染。2010 年 8 月;75(4):292,294.doi: 10.1016/j.jhin.2010.01.013.
- 脚注 129
- 艾伯维公司。SYNAGIS 产品专著。2018. [引用 2022 年 5 月 10 日]。可从:https://www.abbvie.ca/content/dam/abbvie-dotcom/ca/en/documents/products/SYNAGIS_PM_EN.pdf。
- 脚注 130
- PVZ 预防:它对婴儿的生长发育有任何影响吗?Am J Perinatol。2014 年 9 月;31(8):667-72.doi:10.1055/s-0033-1356485。
- 脚注 131
- Wegner S, Vann JJ, Liu G, et al. 高危儿童队列中 PVZ 治疗的直接成本分析:来自北卡罗来纳州医疗补助计划的证据。小儿科。2004 年 12 月;114(6):1612-9.doi: 10.1542/peds.2004-0959.
- 脚注 132
- 超越随机对照试验:婴儿期呼吸道合胞病毒感染预防的“真实生活”体验,有和没有 PVZ。儿科肺病。2006 年 12 月;41(12):1167-74.doi:10.1002/ppul.20507。
- 脚注 133
- Anderson EJ、Carosone-Link P、Yogev R 等人。PVZ 在高危婴儿和儿童中的有效性:倾向评分加权回归分析。儿科感染疾病杂志 2017b 8 月;36(8):699-704.doi: 10.1097/INF.00000000000001533.
- 脚注 134
- Scheltema NM, Nibbelke EE, Pouw J, et al. 健康早产儿呼吸道合胞病毒预防和哮喘:一项随机对照试验。柳叶刀呼吸医学 2018 年 4 月;6(4):257-64.doi: 10.1016/S2213-2600%2818%2930055-9.
- 脚注 135
- Simões EAF、Carbonell-Estrany X、Rieger CHL 等人。呼吸道合胞病毒对特应性和非特应性儿童随后复发性喘息的影响。J 过敏临床免疫学。2010 年 8 月;126(2):256-62.doi: 10.1016/j.jaci.2010.05.026.
- 脚注 136
- Simões EA, Groothuis JR, Carbonell-Estrany X, et al. PVZ 预防、呼吸道合胞病毒和随后的复发性喘息。儿科杂志。2007 年 7 月;151(1):34,42.e1.doi:10.1016/j.jpeds.2007.02.032.
- 脚注 137
- Mochizuki H、Kusuda S、Okada K 等人。早产儿的 PVZ 预防和随后的复发性喘息:六年随访研究。Am J Respir Crit Care Med. 2017 年 7 月 1 日;196(1):29-38.doi: 10.1164/rccm.201609-1812OC.
- 脚注 138
- Yoshihara S、Kusuda S、Mochizuki H 等人。PVZ 预防对早产儿后续复发性喘息的影响。小儿科。2013 年 11 月;132(5):811-8.doi:10.1542/peds.2013-0982。
- 脚注 139
- Grimaldi M, Gouyon B, Michaut F, et al. 严重呼吸道合胞病毒毛细支气管炎:与患有支气管肺发育不良的严重早产儿 PVZ 启动相关的流行病学变异。儿科感染疾病杂志 2004 年 12 月;23:1081-5。doi: 10.1097/01.inf.0000145406.74341.c7.
- 脚注 140
- 罗宾逊 KA, 奥德洛拉 OA, 萨尔达尼亚 IJ.PVZ 用于预防囊性纤维化儿童呼吸道合胞病毒感染。Cochrane 数据库系统修订版 2016 年 7 月;2016(7):CD007743.doi: 10.1002/14651858.CD007743.pub6.
- 脚注 141
- 科恩 AH, 硼 ML, 丁吉万 C.Synagis (PVZ) 预防儿童囊性纤维化呼吸合胞病毒病安全性的 IV 期研究 [海报于 2005 年 5 月 20 日至 25 日在加利福尼亚州圣地亚哥举行的美国胸科学会国际会议上展示]。2005®
- 脚注 142
- Winterstein AG、Eworuke E、Xu D 等人。PVZ 免疫预防对囊性纤维化儿童的有效性。儿科肺病。2013 年 9 月;48(9):874-84.doi:10.1002/ppul.22711.
- 脚注 143
- Giebels K, Marcotte JE, Podoba J. 预防囊性纤维化幼儿的呼吸道合胞病毒。儿科肺病。2008 年 2 月;43(2):169-74.doi:10.1002/ppul.20751.
- 脚注 144
- Buchs C, Dalphin ML, Sanchez S. 囊性纤维化婴儿的 PVZ 预防不会延迟铜绿假单胞菌或金黄色葡萄球菌的首次分离。Eur J 儿科杂志。2017 年 5 月 16 日;176(7):891-7.doi:10.1007/s00431-017-2926-8。
- 脚注 145
- Fink AK、Graff G、Byington CL. PVZ 和囊性纤维化的长期结果。小儿科。2019 年 7 月;144(1):e20183495。doi:10.1542/peds.2018-3495。
- 脚注 146
- Chiu SN, Wang JN, Fu YC, et al.新型 PVZ 预防方案对先天性心脏病呼吸道合胞病毒感染的疗效:一项多中心研究。儿科杂志。2018;195:108,114.e1.doi:10.1016/j.jpeds.2017.11.044.
- 脚注 147
- Soraiz MG、Andrés SB、Castro SB 等人。阿根廷 1 岁以下患有血流动力学显着先天性心脏病的婴儿的 PVZ:与历史对照组的比较研究。年轻人的心脏病学:2017 年增刊 4。WCPCCS 2017:摘要 P2182 -S165-6.
- 脚注 148
- Harris KC、Anis AH、Crosby MC 等人。先天性心脏病儿童 PVZ 的经济评价:加拿大视角。Can J 心脏。2011;27:523.e11,523.e15.doi:10.1016/j.cjca.2010.12.064.
- 脚注 149
- Sanchez-Luna M、Medrano C、Lirio J 等人。唐氏综合症是呼吸道合胞病毒住院的危险因素:一项前瞻性多中心流行病学研究。流感 其他呼吸道病毒。2017 年 3 月;11(2):157-64.doi:10.1111/irv.12431。
- 脚注 150
- Yi H, Lanctôt KL, Bont L, et al. 唐氏综合征的呼吸道合胞病毒预防:一项前瞻性队列研究。小儿科。2014 年 6 月;133(6):1031-7.doi:10.1542/peds.2013-3916。
- 脚注 151
- Kimura T, Takeuchi M, Kawakami K. PVZ 对唐氏综合症儿童的利用和疗效。儿科国际 2020 年 1 月;62:677-82。doi:10.1111/ped.14157。
- 脚注 152
- Banerji A、Panzov V、Young M 等人。PVZ 对减少居住在努纳武特地区的婴儿因呼吸道合胞病毒而住院的实际效果。Can Respir J. 2014 年 5 月至 6 月;21:185-9。doi:10.1155/2014/941367.
- 脚注 153
- Grindeland CJ、Mauriello CT、Leedahl DD 等人。更新的基于指南的 PVZ 管理与呼吸道合胞病毒感染住院之间的关联。儿科感染疾病杂志 2016 年 7 月;35(7):728-32.doi: 10.1097/INF.00000000000001150.
- 脚注 154
- Zembles TN、Bushee GM、Willoughby RE 等人。美国儿科学会 PVZ 指南对胎龄 >=29 和 <35 周儿童的影响。儿科杂志。2019 年 6 月;209:125-9。doi:10.1016/j.jpeds.2019.02.020.
- 脚注 155
- Goldstein M, Krilov LR, Fergie J, et al. 美国呼吸道合胞病毒住院率。2014 年美国儿科学会免疫预防指南前后的早产儿与足月婴儿的比较:2012-2016 年。Am J Perinatol。2018 年 12 月;35(14):1433-42.doi:10.1055/s-0038-1660466。
- 脚注 156
- Kong AM、Krilov LR、Fergie J 等人。2014 年美国儿科学会 2014 年呼吸道合胞病毒免疫预防指南对在美国出生的早产儿的 2014-2015 年全国影响。Am J Perinatol。2018 年 1 月;35(2):192-200.doi:10.1055/s-0037-1606352。
- 脚注 157
- Walpert AS、Thomas ID、Lowe MC 等人先天性心脏病儿童的 RSV 预防指南变化和结果。先天性心脏病。2018 年 5 月;13(3):428-31.doi:10.1111/chd.12590。
- 脚注 158
- Belleudi V, Trotta F, Pinnarelli L, et al. 意大利 PVZ 新报销限制后的新生儿结局。Arch Dis Child. 2018 年 12 月;103(12):1163-7.doi:10.1136/archdischild-2018-315349。
- 脚注 159
- Capizzi A、Silvestri M、Orsi A 等人。PVZ 授权的最近 AAP 变化对 RSV 诱导的毛细支气管炎严重程度和发病率的影响。意大利语 J 儿科杂志。2017 年 8 月 14;43:71。https://doi.org/10.1186/s13052-017-0390-8
- 脚注 160
- Priante E、Tavella E、Girardi E 等人。限制性 PVZ 建议和对胎龄 > 29 周出生婴儿 RSV 住院的影响:一项意大利多中心研究。Am J Perinatol。2019 年 7 月;36(S 02):S77-82。doi:10.1055/s-0039-1691771。
- 脚注 161
- Johnson S、Oliver C、Prince GA 等人。开发一种针对呼吸道合胞病毒具有强效体外和体内活性的人源化单克隆抗体 (Medi-493)。J Infect Dis. 1997 年 11 月;176(5):1215-24.doi:10.1086/514115。
- 脚注 162
- Subramanian KN, Weisman LE, Rhodes T, et al. 早产儿和支气管肺发育不良婴儿呼吸道合胞病毒人源化单克隆抗体的安全性、耐受性和药代动力学。MEDI-493 研究组。儿科感染疾病杂志 1998 年 2 月;17(2):110-5.doi: 10.1097/00006454-199802000-00006.
- 脚注 163
- Robbie GJ, Zhao L, Mondick J, et al. PVZ(一种人源化抗呼吸道合胞病毒单克隆抗体)在成人和儿童中的群体药代动力学 [已发表的更正出现在抗菌剂 Chemother. 2012 年 10 月;56(10):5431].抗菌剂化疗。2012 年 9 月;56(9):4927-36.doi:10.1128/AAC.06446-11。
- 脚注 164
- PVZ:其用作严重呼吸道合胞病毒感染预防的综述。儿科药物。2004;6(3):177-97.doi:10.2165/00148581-200406030-00004。
- 脚注 165
- La Via WV、Notario GF、Yu X-Qiang 等人。三个月剂量的 PVZ 不足以实现 5 个月的保护:群体药代动力学分析。Pulm Pharmacol Ther.2013 年 12 月;26:666e-671. doi: 10.1016/j.pupt.2013.03.007.
- 脚注 166
- Gutfraind A、Galvani AP、Meyers LA 等人。PVZ 注射方案对呼吸道合胞病毒感染的疗效和优化。美国医学会儿科医师。2015 年 4 月;169(4):341-8.doi: 10.1001/jamapediatrics.2014.3804.
- 脚注 167
- Lavoie PM、Solimano A、Taylor R 等人。使用 PVZ 的简化给药方案对婴儿进行呼吸道合胞病毒免疫预防的结果。美国医学会儿科医师。2016 年 2 月;170(2):174-6.doi:10.1001/jamapediatrics.2015.3235。
- 脚注 168
- Claydon J, Popescu CR, Shaiba L, et al. 与先天性心脏病儿童采用简化 PVZ 方案的呼吸道合胞病毒相关的结果:描述性分析。CMAJ 开放。2019 年 2 月 18 日;7(1):E88-93。doi:10.9778/cmajo.20180167。
- 脚注 169
- Claydon J, Sur A, Callejas A, et al. 使用简化给药方案进行 PVZ 预防后婴儿的呼吸道合胞病毒中和血清抗体滴度。公共科学图书馆一号。2017 年 4 月 24 日;12(4):e0176152。doi:10.1371/journal.pone.0176152。
- 脚注 170
- Chen JJ, Chan P, Paes B, et al. 加拿大接受 PVZ (CARESS) 预防呼吸道合胞病毒的儿童登记处的严重不良事件。公共科学图书馆一号。2015 年 8 月 3 日;10(8):e0134711。doi:10.1371/journal.pone.0134711。
- 脚注 171
- Parnes C, Guillermin J, Habersang R, et al. 2000-2001 年呼吸道合胞病毒病的 PVZ 预防:PVZ 结果登记处的结果。儿科肺病。2003 年 6 月;35(6):484-9.doi:10.1002/ppul.10288。
- 脚注 172
- Forbes ML、Kumar VR、Yogev R 等人。血清 PVZ 水平与高危婴儿呼吸道合胞病毒病严重程度降低相关。人类疫苗和免疫疗法。2014;10(10):2789-94.doi:10.4161/hv.29635。
- 脚注 173
- Paes BA, Craig C, Pigott W, et al. 基于预定日期的季节性呼吸道合胞病毒预防与区域监测数据。儿科感染疾病杂志 2013 年 9 月;32(9):e360-4。doi: 10.1097/INF0b013e31829479d3.
- 脚注 174
- Weinberger DM, Warren JL, Steiner CA, et al. 基于当地数据的减剂量预防方案提供了针对呼吸道合胞病毒的近乎最佳的保护。Clin Infect Dis. 2015 年 8 月 15 日;61(4):506-14.doi:10.1093/cid/civ331。
- 脚注 175
- 关键免疫信息免疫剂的储存和处理:疫苗的处理:加拿大免疫指南,第 1 部分 [互联网]。渥太华(安大略省):加拿大公共卫生署;2021 年 6 月 11 日 [引用于 2022 年 5 月 10 日]。网址:https://www.canada.ca/en/public-health/services/publications/healthy-living/canadian-immunization-guide-part-1-key-immunization-information/page-9-storage-handling-immunizing-agents.html#p1c8a2。
- 脚注 176
- Mac S、Sumner A、Duchesne-Belanger S 等人。PVZ 对呼吸道合胞病毒的成本效益:系统评价。小儿科。2019 年 5 月;143(5):e20184064。doi:10.1542/peds.2018-4064。
- 脚注 177
- Blanken MO、Frederix GW、Nibbelke EE 等人。基于规则的免疫预防早产儿呼吸道合胞病毒感染的成本效益。Eur J 儿科杂志。2018 年 1 月;177(1):133-44.doi:10.1007/s00431-017-3046-1。
- 脚注 178
- Lofland JH, O’Connor JP, Chatterton ML, et al. PVZ 用于高危婴儿呼吸道合胞病毒预防:成本效益分析。克林·泰尔。2000 年 11 月;22(11):1357-69.doi:10.1016/s0149-2918(00)83032-5。
- 脚注 179
- Wang D, Cummins C, Bayliss S, et al. 儿童 PVZ 对呼吸道合胞病毒 (RSV) 的免疫预防:系统评价和经济评价。健康技术评估。2008 年 12 月;12(36):iii, ix-x, 1-86.doi:10.3310/HTA12360。
- 脚注 180
- Neovius K, Buesch K, Sandstrom K, et al. PVZ 作为瑞典早产儿呼吸道合胞病毒预防的成本效益分析。Acta Paediatr Int J Paediatr.2011 年 10 月;100(10):1306-14.doi: 10.1111/j.1651-2227.2011.02309.x.
- 脚注 181
- Nuijten MJC, Wittenberg W, Lebmeier M. PVZ 对高危儿童呼吸道合胞病毒预防的成本效益:英国分析。药物经济学。2007;25(1):55-71.doi: 10.2165/00019053-200725010-00006.
- 脚注 182
- Nuijten M, Lebmeier M, Wittenberg W. PVZ 预防荷兰高危儿童 RSV 的成本效益。J Med Econ. 2009a;12(4):291-300.doi: 10.3111/13696990903316961.
- 脚注 183
- Nuijten MJ, Wittenberg W. 西班牙 PVZ 的成本效益:使用观察数据的分析。Eur J Heal Econ. 2010 年 2 月;11(1):105-15.doi:10.1007/s10198-009-0206-x。
- 脚注 184
- Salinas-Escudero G, Martínez-Valverde S, Reyes-López A, et al. 使用 PVZ 预防墨西哥早产儿的成本效益分析。Salud Publica Mex. 2012 年 1 月至 2 月;54(1):47-59.[引用 2022 年 5 月 10 日]。可从:https://pubmed.ncbi.nlm.nih.gov/22286828/。
- 脚注 185
- Sanchez-Luna M, Burgos-Pol R, Oyagüez I, et al. PVZ 用于早产儿呼吸道合胞病毒感染预防的成本效用分析:基于西班牙临床证据的更新。BMC Infect Dis. 2017 年 10 月 17 日;17(1):1-11.doi:10.1186/s12879-017-2803-0.
- 脚注 186
- Smart KA, Paes BA, Lanctt KL. 不断变化的成本和对 RSV 预防的影响。J Med Econ. 2010 年;13(4):705-8.doi: 10.3111/13696998.2010.535577.
- 脚注 187
- 意大利 PVZ 的成本效用分析:高危早产儿呼吸道合胞病毒感染 (RSV) 预防模拟模型的结果。Ital J 儿科杂志。2009 年 2 月 25;35:1-12。doi:10.1186/1824-7288-35-4。
- 脚注 188
- Elhassan NO, Sorbero MES, Hall CB, et al. 无慢性肺病早产儿 PVZ 的成本效益分析。Arch Pediatr Adolesc Med. 2006 年 10 月;160(10):1070-6.doi:10.1001/archpedi.160.10.1070。
- 脚注 189
- McGirr AA、Schwartz KL、Allen U 等人。加拿大环境中 PVZ 在囊性纤维化婴儿中的成本效益:决策分析模型。Hum 疫苗免疫学。2017 年 3 月 4 日;13(3):599-606.doi: 10.1080/21645515.2016.1235670.
- 脚注 190
- Nuijten M, Lebmeier M, Wittenberg W. PVZ 在德国先天性心脏病儿童中的成本效益。J Med Econ. 2009b;12(4):301-8.doi: 10.3111/13696990903347172.
- 脚注 191
- Bentley A、Filipovic I、Gooch K 等人。英国婴儿呼吸道合胞病毒 (RSV) 预防的成本效益分析。健康经济修订版 2013;3:1-12 doi: 10.1136/thoraxjnl-2011-201054c.170.
- 脚注 192
- 先天性心脏病婴儿 PVZ 的经济分析。小儿科。2004 年 12 月;114(6):1606-11.doi:10.1542/peds.2004-0224。
- 脚注 193
- Weiner LB, Masaquel AS, Polak MJ, et al. 美国医疗补助覆盖的早产儿人群中 PVZ 的成本效益分析。J Med Econ. 2012 年;15(5):997-1018.doi: 10.3111/13696998.2012.672942.
- 脚注 194
- Mahadevia PJ, Masaquel AS, Polak MJ, et al. 美国早产儿 PVZ 预防的成本效用:国家政策视角。J Med Econ. 2012 年 5 月 10 日;15(5):987-96.doi: 10.3111/13696998.2012.690013.
- 脚注 195
- Schmidt R, Majer I, García Román N, et al. PVZ 预防先天性心脏病儿童严重呼吸道合胞病毒感染;一项反映西班牙循证临床路径的新型成本效用建模研究。健康经济修订版 2017 年 12 月 19;7:47。doi:10.1186/s13561-017-0181-3。
- 脚注 196
- Tam DY、Banerji A、Paes BA 等人。PVZ 在加拿大东部北极地区因纽特足月婴儿中的成本效益。J Med Econ. 2009 年;12(4):361-70.doi:10.3111/13696990903442155。
- 脚注 197
- Banerji A、Ng K、Moraes TJ 等人。PVZ 与无预防相比,对居住在加拿大北极地区的足月婴儿的成本效益。CMAJ 开放。2016 年 10 月至 12 月;4(4):E623-33。doi:10.9778/cmajo.20150052.
- 脚注 198
- Rietveld E, Steyerberg EW, Polder JJ, et al. 针对呼吸道合胞病毒的被动免疫:成本效益分析。Arch Dis Child. 2010 年 7 月;95(7):493-8.doi: 10.1136/adc.2008.155556
- 脚注 199
- Roeckl-Wiedmann I, Liese JG, Grill E, et al. 德国早产儿可能预防 RSV 相关住院的经济评估。Eur J 儿科杂志。2003 年 4 月;162(4):237-44.doi:10.1007/s00431-002-1106-6。
- 脚注 200
- Vogel AM、McKinlay MJ、Ashton T 等人。新西兰 PVZ 的成本效益。J 儿科儿童健康。2002 年 8 月;38(4):352-7.doi: 10.1046/j.1440-1754.2002.00790.x.
- 脚注 201
- Hampp C、Kauf TL、Saidi AS 等人。各种适应症中呼吸道合胞病毒预防的成本效益。Arch Pediatr Adolesc Med. 2011 年 6 月;165(6):498-505.doi: 10.1001/archpediatrics.2010.298.
- 脚注 202
- Hascoet JM、Fagnani F、Charlemagne A 等人。儿科经济评估的方法学方面:法国环境中 RSV 感染预防的说明。拱儿科。2008 年 12 月;15(12):1739-48.doi:10.1016/j.arcped.2008.09.024.
- 脚注 203
- Seeler RA, Schatz B. PVZ (Synagis)–将婴儿分组以减少浪费。小儿科。1999 年 11 月;104(5 第 1 部分):1170-1。doi:10.1542/peds.104.5.1170。
- 脚注 204
- CADTH 方法和指南。卫生技术经济评估指南:加拿大第 4 版 [Internet]。渥太华(安大略省):CADTH;2017 年 5 月;1-76 [引用于 2022 年 5 月 10 日]。可从:https://www.cadth.ca/sites/default/files/pdf/guidelines_for_the_economic_evaluation_of_health_technologies_canada_4th_ed.pdf。
- 脚注 205
- Mossialos E, Wenzl M, London School of Economics and Political Science, et al. 2015 年医疗保健系统国际概况:2016 年 1 月 [互联网]。纽约 (NY):联邦基金;2016 年 1 月;1-180 [引用于 2022 年 5 月 10 日]。可从:https://www.commonwealthfund.org/publications/fund-reports/2016/jan/international-profiles-health-care-systems-2015。
- 脚注 206
- Gilca R. 魁北克国家公共卫生研究所。个人通信。
- 脚注 207
- Lorcy A、Gilca R、Dubé E 等人。可行性和伦理问题:医护人员对魁北克努纳维克新 RSV 预防计划的经验和担忧。国际极地健康杂志。2020 年 12 月;79(1):1742564.doi: 10.1080/22423982.2020.1742564.
- 脚注 208
- Hui C, Paes B, Papenburg J, et al. 加拿大原住民儿童的 PVZ 依从性和结果。儿科感染疾病杂志 2016 年 11 月;35(11):1187-93.doi: 10.1097/INF.0000000000001282.
- 脚注 209
- Wong S.K., Li A., Lanctot K.L., et al.依从性和结果:PVZ 利用率的系统评价。专家 Rev Respir Med. 2018 年 1 月;12(1):27-42.doi: 10.1080/17476348.2018.1401926.
- 脚注 210
- 加拿大警戒计划 [互联网]。渥太华(安大略省):加拿大卫生部;2018 年 7 月 12 日[引用于 2019 年 4 月 5 日]。可从:https://www.canada.ca/en/health-canada/services/drugs-health-products/medeffect-canada/canada-vigilance-program.html。
- 脚注 211
- Wegzyn C、Toh LK、Notario G 等人。PVZ 在呼吸道合胞病毒感染导致严重疾病高危儿童中的安全性和有效性:一项系统评价。感染 Dis Ther.2014 年 12 月;3(2):133-58.doi:10.1007/s40121-014-0046-6。
- 脚注 212
- Makari D, Jensen KM, Harris B, et al. 液体与冻干 PVZ 制剂在早产儿和患有慢性肺病的儿童中的安全性的随机、双盲研究。感染 Dis Ther.2014 年 12 月;3(2):339-47.doi:10.1007/s40121-014-0033-y.
- 脚注 213
- Robbie GJ、Makari D、Harris B. PVZ 液体制剂与冻干制剂相比的药代动力学和安全性的随机、双盲研究。感染 Dis Ther.2014 年 12 月;3(2):203-14.doi:10.1007/s40121-014-0042-x。
- 脚注 214
- Carbonell-Estrany X、Simões EAF、Dagan R 等人。Motavizumab 预防高危儿童呼吸道合胞病毒:一项非劣效性试验。小儿科。2010 年 1 月;125(1):e35-51。doi:10.1542/peds.2008-1036。
- 脚注 215
- Fernandez P、Trenholme A、Abarca K 等人。在同一季节使用 Motavizumab 和 PVZ 预防呼吸道合胞病毒 (RSV) 的 2 期、随机、双盲安全性和药代动力学评估。BMC 儿科。2010 年 6 月 3;10:38。doi:10.1186/1471-2431-10-38。
- 脚注 216
- Feltes TF, Sondheimer HM, Tulloh RM, et al. Motavizumab 与 PVZ 预防血流动力学显着先天性心脏病儿童严重呼吸道合胞病毒病的随机对照试验。儿科研究 2011 年 8 月;70(2):186-91.doi: 10.1203/PDR.0b013e318220a553.
- 脚注 217
- Haerskjold A, Linder M, Henriksen L, et al. PVZ 暴露和自身免疫性疾病的风险:一项跨国队列研究。儿科药物。2016 年 12 月;18(6):435-41.doi:10.1007/s40272-016-0191-3。
- 脚注 218
- Haerskjold A, Stokholm L, Linder M, et al. PVZ 暴露和特应性皮炎、哮喘和过敏性鼻结膜炎的风险:一项跨国、基于人群的队列研究。儿科药物。2017 年 4 月;19(2):155-64.doi:10.1007/s40272-017-0215-7。
- 脚注 219
- Mitchell I, Paes BA, Li A, et al. CARESS:PVZ 的加拿大登记处。儿科感染疾病杂志 2011 年 2 月;30:651-5。doi: 10.1097/INF.0b013e31821146f7.
- 脚注 220
- Paes B, Mitchell I, Li A, et al. 特殊人群的呼吸系统住院和呼吸道合胞病毒预防。Eur J 儿科杂志。2012 年 5 月;171(5):833-41.doi:10.1007/s00431-011-1654-8。
- 脚注 221
- Manzoni P、Paes B、Lanctôt KL 等人。加拿大和意大利接受 PVZ 预防呼吸道合胞病毒的婴儿结果:一项国际前瞻性队列研究。儿科感染疾病杂志 2017 年 1 月;36(1):2-8.doi: 10.1097/INF.00000000000001340.
- 脚注 222
- Simon A, Nowak H, Sterz R. 德国 PVZ 的使用:2002-2007 年的数据。克林·帕迪亚特。2011 年 9 月;223(5):292-8.doi:10.1055/s-0030-1270515。
- 脚注 223
- Simon A、Gehrmann S、Wagenpfeil G 等人。PVZ 在德国的使用 – 德国 SynagisTM 登记处 2009 – 2016 年报告。克林·帕迪亚特。2018 年 9 月;230(5):263-9.doi:10.1055/a-0595-7771。
- 脚注 224
- Groothuis JR. 北半球一项大型试验中 PVZ 给药的安全性和耐受性。北半球扩展访问研究组。Pediatr Infect Dis J. 2001 年 6 月;20(6):628-30.doi: 10.1097/00006454-200106000-00018.
- 脚注 225
- Groothuis Jr. PVZ 在 29 至 32 周胎龄无慢性肺病早产儿中预防严重呼吸道合胞病毒感染的安全性。Eur J Clin Microbiol Infect Dis. 2003 年 7 月;22(7):414-7.doi:10.1007/s10096-003-0961-z。
- 脚注 226
- 卡斯蒂略 LM、布加林 G、阿里亚斯 JC。拉丁美洲有呼吸道合胞病毒感染风险婴儿 PVZ 预防的一年观察性研究。Eur J Clin Microbiol Infect Dis. 2017 年 9 月至 10 月;93(5):467-74.doi: 10.1016/j.jped.2016.11.006.
- 脚注 227
- Lacaze-Masmonteil T, Roze JC, Fauroux B. 高危儿童呼吸道合胞病毒相关住院的发生率:接受 PVZ 作为 RSV 预防治疗的全国婴儿队列的随访。儿科肺病。2002 年 9 月;34(3):181-8.doi:10.1002/ppul.10175。
- 脚注 228
- Pinquier D、Gouyon JB、Fauroux B 等人。Modalités d’Utilisation, Tolérance et Benefice du PVZ dans la Prévention des Infections à VRS en France : Saison 2005–2006 [PVZ 免疫预防:法国临床实践中的使用、安全性和有益效果]。拱儿科。2009 年 11 月;16(11):1443-52.doi:10.1016/j.arcped.2009.08.008.
- 脚注 229
- Kashiwagi T, Okada Y, Nomoto K. 免疫功能低下或唐氏综合症儿童呼吸道合胞病毒感染的 PVZ 预防:日本的一项多中心上市后监测。儿科药物。2018 年 2 月;20(1):97-104.doi:10.1007/s40272-017-0264-y。
- 脚注 230
- Al-Alaiyan S、Pollack P、Notario GF。沙特阿拉伯婴儿和儿童长期使用 PVZ 的安全性和药代动力学。药物背景。2015 年 2 月 27;4:212270。doi:10.7573/dic.212270。
- 脚注 231
- Lacaze-Masmonteil T、Seidenberg J、Mitchell I 等人。PVZ 在有严重呼吸道合胞病毒感染风险的幼儿暴露第二季的安全性评估。药物安全2003;26(4):283-91.doi: 10.2165/00002018-200326040-00005.
- 脚注 232
- Null D Jr、Pollara B、Dennehy PH 等人。PVZ (Synagis) 给药两个季节的安全性和免疫原性。Pediatr Infect Dis J. 2005 年 11 月;24(11):1021-3.doi: 10.1097/01.inf.0000183938.33484.bd.
- 脚注 233
- Turti TV、Baibarina EN、Degtiareva EA 等。俄罗斯联邦严重呼吸道合胞病毒病高危儿童 PVZ 预防的前瞻性、开放标签、非比较研究。BMC Res 笔记。2012 年 9 月 4;5:484。doi:10.1186/1756-0500-5-484。
- 脚注 234
- Mori M、Onodera M、Morimoto A 等人。PVZ 在日本免疫功能低下婴儿和儿童中的使用。儿科感染疾病杂志 2014 年 11 月;33(11):1183-5.doi: 10.1097/INF.00000000000000392.
- 脚注 235
- Sáez-Llorens X、Castaño E、Null D 等人。早产儿和支气管肺发育不良婴儿肌内人源化呼吸道合胞病毒单克隆抗体的安全性和药代动力学。MEDI-493 研究组。Pediatr Infect Dis J. 1998 年 9 月;17(9):787-91.doi: 10.1097/00006454-199809000-00007.
- 脚注 236
- Borecka R, Lauterbach R, Helwich E. 与呼吸道合胞病毒 (RSV) 感染 PVZ 预防依从性相关的因素 – 来自波兰的数据。Med Wieku Rozwoj.2016;20(3):181-90.[引用 2022 年 5 月 10 日]。可从:https://pubmed.ncbi.nlm.nih。gov/27941187/。
- 脚注 237
- Abushahin A, Janahi I, Tuffaha A. 卡塔尔早产儿 PVZ 免疫预防对呼吸道合胞病毒病的有效性。国际通用医学杂志 2018 年 1 月 31;11:41-6。doi: 10.2147/IJGM.S156078。
- 脚注 238
- 张SG, Park MS, Yu JE.2005 年至 2009 年韩国一家医院 PVZ 预防支气管肺发育不良早产儿呼吸道合胞病毒感染的结果。J Korean Med Sci. 2010 年 2 月;25(2):251-6.doi:10.3346/jkms.2010.25.2.251.
- 脚注 239
- 萨维茨 J、吉尼 C、班克斯 TA。一例 PVZ 过敏反应。Ann Allergy 哮喘免疫学。2014 年 8 月;113(2):236-7.doi:10.1016/j.anai.2014.06.006.
- 脚注 240
- Resch B. 用于预防呼吸道合胞病毒感染的单克隆抗体 PVZ 的产品评论。Hum Vaccin 免疫剂。2017 年 9 月 2 日;13(9):2138-49.doi: 10.1080/21645515.2017.1337614.
- 脚注 241
- Tenenbaum T, Drechsel-Bäuerle U, Oberle D. PVZ 单克隆抗体预防后的心肺事件。儿科感染疾病杂志 2018 年 11 月;37(11):e281-2。doi: 10.1097/INF.000000000000002017.
- 脚注 242
- Pérez-De-Lis M、Retamozo S、Flores-Chávez A 等人。由生物制剂诱导的自身免疫性疾病。对 12,731 例的审查(BIOGEAS 登记处)。专家 Opin 药物 Saf。2017 年 11 月;16(11):1255-71.doi:10.1080/14740338.2017.1372421。
- 脚注 243
- Saji T, Nakazawa M, Harada K. 先天性心脏病儿童 PVZ 预防的安全性和有效性。儿科国际。2005 年 8 月;47(4):397-403.doi: 10.1111/j.1442-200x.2005.02089.x.
- 脚注 244
- Simon A, Gehrmann S, Wagenpfeil G, et al. PVZ 在唐氏综合症婴儿中的应用 – 来自德国 SynagisTM 登记处的报告 2009-2016。Eur J 儿科杂志。2018 年 6 月;177(6):903-11.doi:10.1007/s00431-018-3142-x.
页面详细信息
修改日期:
Hits: 34
- 心脏病成人的疫苗接种指南
- 用于检测治疗性蛋白制品的免疫原性的检测法开发和验证行业指南
- 肺部疾病成人的疫苗接种指南
- 快速响应:截至 2024 年 12 月在非大流行背景下人类接种禽流感疫苗的初步指南
- 糖尿病成人的疫苗接种指南
- 慢性肝病或慢性肝脏感染成人的疫苗接种指南
- 人类免疫缺陷病毒(HIV)感染者成人疫苗接种指南
- 65 岁及以上成人流感疫苗接种补充指南
- 2013 年美国感染病学会(IDSA)免疫功能低下人群疫苗接种临床实践指南
- 针对公共卫生紧急情况的猴痘检测政策
- 卫生保健机构手部卫生指南
- 环境感染控制指南 保健设施
- 2025 年 4 月 30 日的 NACI 声明摘要:关于 2025-2026 年季节性流感疫苗的声明
- 更新了老年人呼吸道合胞病毒 (RSV) 疫苗指南,包括扩大 RSVPreF3 在 50-59 岁人群中的使用以及使用新的 mRNA-1345 疫苗
- 孕期梅毒感染筛查:美国预防服务工作组重申建议声明
- 2025 年 5 月 14 日的 NACI 声明摘要:关于免疫功能低下成人带状疱疹疫苗接种的最新建议
- 2022 美国动物卫生协会犬类疫苗接种指南(2024年更新)
- 2020 年 AAHA/AAFP 猫科动物疫苗接种指南
- 2025 年 5 月 15 日的 NACI 声明摘要:关于使用 Imvamune 预防 mpox 的更新指南的快速响应
- 2025 年 2 月 13 日 NACI 声明摘要:关于麻疹暴露后预防的更新建议
- 从 2025 年 7 月 1 日起完成常规免疫接种计划(英国)
- 2025 年 1 月 10 日的 NACI 声明摘要:2025 年至 2026 年夏季 COVID-19 疫苗使用指南
- 麻疹暴露后预防更新建议的增编
- 使用 Imvamune 预防猴痘的更新指南
- 免疫功能低下成人带状疱疹疫苗接种的最新建议
- 推荐使用帕利珠单抗减少婴儿呼吸道合胞病毒感染的并发症
- 登革热防控方案(2025年版)
- 关于防止节肢动物叮咬的个人防护措施的声明 – 更新
- CATMAT 关于在 65 岁或以上人群中使用基孔肯雅热减毒活疫苗 (IXCHIQ) 的指南
- 关于在授权旅行者使用 QDENGA(登革热疫苗)的司法管辖区使用的建议
- 基于暴露的干预措施,用于管理整个生命周期中高度针头恐惧的个体:临床实践指南,呼吁进一步研究
- mRNA COVID-19 疫苗接种后患有心肌炎和心包炎的青少年的临床指南
- 归国国际旅客发热初步评估指南
- NACI 快速响应:在持续的猴痘疫情背景下更新了关于 Imvamune 的临时指南
- 关于管理耐多药沙门氏菌感染的临时指南
- 家长免疫接种指南
- 英国旅行者接种基孔肯雅热疫苗:JCVI 建议
- 针对 80 岁及以上成年人的呼吸道合胞病毒 (RSV) 免疫计划:JCVI 建议,2025 年 7 月 16 日
- JCVI 关于 2026年秋季和 2027 年春季 COVID-19 疫苗接种的声明
- CATMAT 关于播散性类圆线虫病的声明
- 成人免疫接种指南
- 针对呼吸道合胞病毒感染住院高风险婴幼儿的帕利珠单抗预防更新指南
- 针对呼吸道合胞病毒感染住院高风险婴幼儿的帕利珠单抗预防
- JCVI 关于 2026 年至 2027 年流感疫苗的声明
- 有关打算探亲访友的国际旅客的声明摘要
- 青少年疫苗接种指南
- 免疫接种状态不确定或不完全的个人疫苗接种:2025 年 7 月 1 日起
- 从 2025 年 7 月 1 日起进行常规儿童免疫接种(2024 年 7 月 1 日出生的婴儿)
- 加拿大关于在疫苗短缺期间使用分次剂量黄热病疫苗的临时建议
- 寨卡病毒预防和治疗建议
- 带状疱疹免疫接种计划:医护人员资讯
- 带状疱疹疫苗接种指南
- 儿童和青少年接种COVID-19疫苗
- 印度旅行疫苗接种:2025 年循证健康指南
- 旅行者疟疾预防和治疗指南
- 登革热:给明智旅行者与移居者的详尽旅行指南
- 旅行者伤寒:预防和保护完整指南
- 美国儿科学会 2025 年 8 月 19 日发布的推荐18 岁及以下儿童与青少年免疫接种程序
- 隐藏的敌人:旅行者立克次体感染完整指南
- 心脏病发作症状:旅行者的基本医疗指南
- 真菌性皮肤感染:类型、治疗和预防完整指南
- 热带医学和旅行咨询委员会 (CATMAT) 关于国际旅行者和伤寒的声明
- 2025 年简明临床指南:ACC 关于成人免疫接种作为心血管护理一部分的专家共识声明:美国心脏病学会解决方案集监督委员会的报告
- 产科-妇科护理中的 COVID-19 疫苗接种注意事项
- 妊娠期流感:预防和治疗
- 母体呼吸道合胞病毒疫苗接种
- 疫苗预防和控制季节性流感:免疫实践咨询委员会的建议——美国,2025-26 年流感季节
- 用Clesrovimab预防婴儿严重呼吸道合胞病毒相关下呼吸道感染:免疫实践咨询委员会的建议 — 美国,2025年
- 健康怀孕指南
- 关于预防婴幼儿呼吸道合胞病毒感染的建议:政策声明
- 过敏反应定义、概述和临床支持工具:2024 年共识报告 – GA2LEN项目
- 人狂犬病免疫球蛋白(human rabies immunoglobulin, HRIG)使用临时建议
- 如何与我们的心脏病患者讨论成人疫苗接种
- 2025 年秋季疫苗指南
- 疫苗佐剂非临床研究技术指导原则
- 完整的常规免疫接种计划 英国 2025年9月1日期
- 2025 年至 2026 年国家流感免疫接种计划信函
- 恰加斯病:基本旅行指南
- 创新型疫苗临床试验申请申报资料要求
- 远离结核病的旅行者指南
- 更顺畅的免疫接种体验指南
- 您的免疫预约指南:充满信心地完成整个过程
- 联合疫苗临床前和临床研究技术指导原则
- 疫苗接种预约指南:预期事项与准备方法
- 旅行时如何保护儿童免受水痘侵害:专家指南
- 家长互联网免疫接种信息指南
- 您的无缝免疫接种与健康服务指南
- 2025年病毒爆发与旅行警告:专家友好指南
- 结合疫苗质量控制和临床研究技术指导原则
- 预防用含铝佐剂疫苗技术指导原则
- 生物制品稳定性研究技术指导原则(试行)
- 常见传染病的暴露后预防
- 无缝接种预约指南
- 开发用于预防全球传染病的疫苗的一般原则
- 关于预防性疾病的联合疫苗评估:生产、测试和临床研究
- 关于组合疫苗及免疫学兽用药品(IVMPs)联合使用的指导原则
- 世界卫生组织关于疫苗非临床评价的指南
- 确保基于DT的组合疫苗的质量、安全和有效性的建议
- 沙特 疫苗生产和质量控制指南
- 疫苗接种预约指南:流程与准备事项
- 儿童与青少年疫苗接种时间指南
- 聚焦预防 | 美国心脏病学会简化心血管疾病免疫接种建议
- 精通疫苗接种诊所:提高效率与优化患者护理的内部指南
- 临床医生呼吸道疫苗共同临床决策指南
- 你的疫苗接种顺利体验指南
- 美国传染病学会关于A组链球菌性咽炎的临床实践指南更新
- 更顺畅疫苗接种体验终极指南
- 婴幼儿和青少年COVID-19疫苗接种建议:政策声明
- IDSA 2025年关于在免疫功能低下患者中使用疫苗预防季节性新冠病毒、流感和呼吸道合胞病毒感染的指南
- 无脾成人的疫苗接种指南
- 花生过敏预防的积极趋势:预防指南的实际影响
- 2025–2026年儿童流感预防与控制建议:技术报告
- 您的疫苗诊所指南:像专业人士一样导航系统
- 带状疱疹疫苗临床试验技术指导原则
- PIDS/IDSA 2023年儿童急性细菌性关节炎诊断和管理指南
- 预防节肢动物叮咬的个人防护措施声明
- 异维甲酸与疫苗诊所:保持防护的内部指南
- IDSA 2024年抗微生物药物耐药革兰氏阴性菌感染治疗指南
- 重组糖蛋白激素类产品药学研究与评价技术指导原则
- 流感病毒疫苗临床试验技术指导原则(征求意见稿)
- 重组表达单克隆抗体类生物制品制造及检定规程撰写指南(征求意见稿)
- 归国国际旅行者发热初始评估指南
- 中国流感疫苗预防接种技术指南(2025—2026)
- 成人癌症相关免疫抑制患者抗菌药物预防临床实践指南:ASCO/IDSA更新版
- 免疫功能低下旅行者
- 全国镰状细胞中心联盟关于镰状细胞病健康维护的共识建议共识声明
- 多联疫苗临床试验技术指导原则
- 曲霉病诊断和管理临床实践指南:IDSA 2016年更新版
- 养老院感染预防与控制多学会指南
- 关于跨国收养的声明
- 美国传染病学会 (IDSA) 发布的《念珠菌病管理临床实践指南:2016 年更新版》
- 流感疫苗完全指南
- IWGDF/IDSA糖尿病相关足部感染诊疗指南
- 热带病与旅行咨询委员会:老年旅行者声明
- 疫苗临床试验不良事件分级标准指导原则(修订版)
- ATS/CDC/IDSA临床实践指南:成人和儿童结核病的诊断
- 用于人乳头瘤病毒检测的自行收集阴道标本及筛查终止指南:美国癌症协会宫颈癌筛查指南更新
- 热带医学与旅行咨询委员会关于儿童旅行者的声明
- 成人导管相关性尿路感染的诊断、预防和治疗:美国传染病学会2009年国际临床实践指南
- HIVMA/IDSA 2014年更新版:HIV感染患者慢性肾病管理临床实践指南
- 对免疫状况不明或未完成的人员进行疫苗接种:自2026年1月1日起
- SHEA/IDSA 发布的《成人艰难梭菌感染管理临床实践指南:2021 年更新》
- 加拿大传染病报告:孕期旅行声明
- 成人和儿童艰难梭菌感染临床实践指南:美国医疗保健流行病学学会/美国感染病学会2017年更新版
- 关于旅行者与狂犬病疫苗的声明
- IDSA 2016 年球孢子菌病治疗临床实践指南
- 免疫接种者袖珍指南:孕期与哺乳期
- 成人社区获得性肺炎的诊断和治疗:美国胸科学会和美国传染病学会官方临床实践指南
- CATMAT 关于播散性粪类圆线虫病的声明:预防、评估和管理指南
- 3个月以上婴幼儿社区获得性肺炎的管理:儿科传染病学会和美国传染病学会临床实践指南
- 复杂性尿路感染(cUTI):治疗和管理临床指南
- 自行采集阴道标本用于人乳头瘤病毒检测及筛查退出指南:美国癌症协会宫颈癌筛查指南更新
- 旅行者结核病风险评估与预防
- IDSA 新型冠状病毒肺炎患者治疗和管理指南
- 热带病与旅行咨询委员会(CATMAT) 致旅行者及关于黄热病的声明
- 预防用疫苗佐剂药学研究技术指导原则(试行 )
- 隐球菌病治疗临床实践指南: 美国感染病学会2010年更新
- 儿童常规免疫接种计划
- ASM/ECMM/ISHAM 隐球菌病诊断和治疗全球指南
- 加拿大各省及地区婴幼儿常规(及补种)疫苗接种时间表(截至2025年12月)
- 美国儿科学会推荐的青少年及年轻成人疫苗
- IDSA 脑炎管理指南
- 加拿大各省和地区针对健康且先前已接种疫苗的成年人的常规疫苗接种计划
- 美国2026年儿童和青少年免疫接种计划建议
- 美国心脏协会成人感染性心内膜炎指南:诊断、抗菌治疗和并发症处理
- IDSA 2008 年老年长期护理机构居民发热和感染评估临床实践指南更新
- 癌症成人患者的疫苗接种:ASCO指南
- 癌症患者治疗前的乙型肝炎病毒筛查与管理:美国临床肿瘤学会临时临床意见更新
- CEPI 生物安全政策
- IDSA 关于 A 组链球菌(GAS)咽炎的临床实践指南更新
- 2026 年美国 18 岁及以下儿童和青少年推荐免疫接种程序
- 2025-2030 年美国人膳食指南
- AASLD/IDSA 2023 年丙型肝炎病毒感染检测、管理和治疗临床实践指南更新
- 关于接受度普利尤单抗治疗的患者使用疫苗的系统评价和专家德尔菲共识建议:美国过敏、哮喘和免疫学会立场文件
- 常规推荐的孕产妇疫苗接种汇总
- SHEA/APIC/IDSA/PIDS 多学会联合立场文件:提高标准——有效医疗机构感染预防和控制计划所需的资源和结构
- 美国医疗机构中感染乙型肝炎、丙型肝炎或人类免疫缺陷病毒的医护人员管理办法
- 医护人员疫苗接种咨询四步法指南
- IDSA 2017 年医疗相关性脑室炎和脑膜炎临床实践指南
- AASLD ISDA 慢性乙型肝炎治疗实践指南
- 美国传染病学会 2025 年组织胞浆菌病临床实践指南更新:成人、儿童和孕妇无症状组织 胞浆菌肺结节(组织胞浆菌瘤)及轻度或中度急性肺组织胞浆菌病的治疗
- 呼吸中心:您的 GoodRx 指南
- 2017 年 HIVMA/IDSA 艾滋病毒感染者慢性疼痛管理临床实践指南
- 人乳头瘤病毒疫苗临床试验技术指导原则 (修订版)
- 流感病毒疫苗临床试验技术指导原则(试行)
- 美国传染病学会和美国胸科学会2016年临床实践指南:成人医院获得性肺炎和呼吸机相关性肺炎的管理
- 美国内科医师学会免费提供的 2025-2026 年成人新冠疫苗接种快速实践指南(适用于非孕妇或免疫功能低下成人)
- 美国传染病学会发布的《婴幼儿、儿童、青少年和成人免疫接种计划:临床实践指南》
- SHEA/IDSA 实施抗菌药物管理计划的临床实践指南
- IDSA 2017 年感染性腹泻诊断和治疗临床实践指南
- IDSA 2018 年季节性流感诊断、治疗、化学预防和机构暴发管理临床实践指南更新
- IDSA 2024 年指南更新:成人、儿童和孕妇复杂性腹腔内感染的风险评估、影像诊断和微生物学评估

