Contents
Cost-Effectiveness of Nirsevimab and Maternal RSVpreF Immunization Strategies in Low-Risk Infants
共同第一作者,贡献相同
2023 年,免疫实践咨询委员会(ACIP)建议,对 8 个月以下婴儿使用尼塞维单抗,对妊娠 32 至 36 周的孕妇接种 RSVpreF 疫苗,以预防婴儿呼吸道合胞病毒(RSV)相关的下呼吸道感染。我们比较了 ACIP 推荐的尼塞维单抗联合 RSVpreF 疫苗策略与仅使用尼塞维单抗策略在美国健康低风险婴儿中的成本效益。
我们使用嵌套马尔可夫模型构建决策树,比较了三种针对健康低风险婴儿的免疫策略:不免疫、根据美国免疫实践咨询委员会 (ACIP) 指南采用 RSVpreF 和尼塞维单抗的混合策略,以及所有婴儿仅使用尼塞维单抗。我们使用质量调整生命年 (QALY) 评估了健康和社会结局,并从医疗保健部门(即直接医疗成本)和社会角度(即照护者生产力损失等因素)评估了成本。我们使用增量成本效益比 (ICER) 评估了成本效益,并以 15 万美元/QALY 的支付意愿阈值作为成本效益基准,同时进行了敏感性分析。
从医疗保健行业的角度来看,根据 15 万美元/质量调整生命年(QALY)的阈值,混合策略和单独使用奈塞维单抗的策略与不接种疫苗相比均不具有成本效益。从社会角度来看,混合策略与不接种疫苗相比具有成本效益(117,848 美元/QALY)。由于产品成本较高,单独使用奈塞维单抗与混合策略相比不具有成本效益(347,821 美元/QALY)。然而,如果 RSVpreF 疫苗不可行,则单独使用奈塞维单抗的策略与不接种疫苗相比具有成本效益(134,391 美元/QALY)。结果对产品成本和疗效的假设较为敏感。
儿科医生和妇产科医生应共同推荐 RSV 疫苗接种,因为 ACIP 推荐的混合 RSVpreF 和 nirsevimab 策略是一种对社会具有成本效益的保护婴儿的方法。
政策影响概述:
儿科医生和妇产科医生应携手合作,通过为婴儿接种尼塞维单抗或为孕妇接种 RSVpreF 疫苗来扩大呼吸道合胞病毒(RSV)的保护范围。尽管 RSVpreF 的临床疗效较低,但结合两种干预措施的混合策略是最具成本效益的方法。降低尼塞维单抗价格的政策不仅可以提高其可及性,还能使其成为预防 RSV 相关疾病最具成本效益和临床疗效的策略。
介绍
呼吸道合胞病毒 (RSV) 是美国婴幼儿最常见的致病因素之一,也是导致婴幼儿住院的主要原因之一。 1-4 此前,单克隆抗体帕利珠单抗是儿童唯一的免疫选择,但其价格昂贵,需要每月注射,且仅推荐用于高危婴儿。 5,6 2023 年 8 月,免疫实践咨询委员会 (ACIP) 推荐使用一种新的单剂量单克隆抗体尼塞维单抗,用于所有 8 个月以下的婴儿以及进入第二个 RSV 流行季的 8 至 19 个月大的儿童,这些儿童罹患严重 RSV 的风险较高。 5,7 2023 年 9 月,ACIP 推荐在 9 月至次年 1 月期间,为妊娠 32 至 36 周的孕妇接种 RSVpreF 疫苗,这是一种基于蛋白质的 RSV 疫苗。 8,9
随着 nirsevimab 和 RSVpreF 的获批,其成本效益问题也随之出现。在私营医疗机构,RSVpreF 的定价为 306.80 美元,而 nirsevimab 的定价为 556.13 美元。 10 尽管临床试验结果令人鼓舞,但高昂的免疫接种成本仍然令医疗服务提供者和保险公司感到担忧。 11-13 美国疾病控制与预防中心(CDC)在 2024 年对儿科医生和妇产科医生进行的一项调查显示,RSV 免疫接种面临的主要挑战包括:采购产品库存带来的经济负担、保险报销问题以及 RSVpreF 和 nirsevimab 之间缺乏优先推荐。 13 美国免疫实践咨询委员会(ACIP)引用的两项近期美国研究分别考察了这些免疫产品的成本效益。其中,nirsevimab 的研究发现,与不接种疫苗相比,季节性地为婴幼儿接种疫苗可能具有社会成本效益。 14 RSVpreF 研究发现,在呼吸道合胞病毒 (RSV) 流行季之前或早期给孕妇接种疫苗可能具有成本效益 。15 一项加拿大研究报告称,采用混合策略,即为孕妇接种疫苗并仅对高危婴儿进行免疫接种,其成本效益为:nirsevimab 为 290 美元,RSVpreF 为 195 美元 。16 随着美国免疫实践咨询委员会 (ACIP) 发布报告,建议使用 nirsevimab 和 RSVpreF 来扩大对所有婴儿(包括之前不符合 palivizumab 接种条件的婴儿)的保护范围,了解这些产品在所有 8 个月以下婴儿中的成本效益对于确定最佳免疫接种策略至关重要。 由于尼塞维单抗基本取代了帕利珠单抗用于符合条件的高危患者,我们的分析重点转向了首个呼吸道合胞病毒(RSV)流行季的“低危”婴儿,因为这些新产品扩大了 RSV 防护的覆盖范围。 6,17 虽然我们将足月儿和晚期早产儿(无慢性疾病)称为“低危”,但所有婴儿都有罹患严重 RSV 的风险,使用“低危”一词是为了将他们与患有慢性肺病或先天性心脏病等疾病的高危婴儿区分开来。5 6
本研究旨在对美国人群中的三种免疫策略进行成本效益分析:不进行免疫接种、根据 ACIP 指南采用 RSVpreF 和 nirsevimab 的混合策略,以及仅使用 nirsevimab 进行 RSV 预防。我们从医疗保健系统和社会角度构建了 RSV 感染结局在晚期早产儿和足月健康婴儿中的模拟模型。
方法
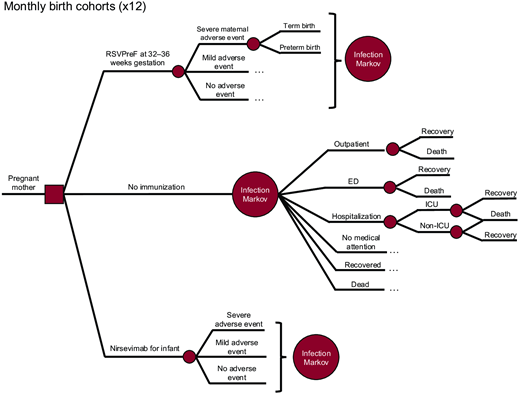
带有嵌套马尔可夫模型的决策树( 图 1 )估算了 3 种针对健康、低风险婴儿在出生第一年的免疫策略的成本和收益:
未接种疫苗
ACIP 推荐的混合策略是使用 RSVpreF 和 nirsevimab 18 :对妊娠 32 至 36 周的孕妇进行季节性 RSVpreF 接种,对拒绝接种 RSVpreF 的母亲所生的婴儿进行 nirsevimab 接种,并对在季节性接种窗口期之外出生的婴儿进行 nirsevimab 补种。
在呼吸道合胞病毒(RSV)流行季节,所有新生儿出生时均需接种尼塞维单抗;对于在流行季节之外出生的婴儿,则需进行补种免疫接种。
在 2023-2024 年呼吸道合胞病毒(RSV)流行季的初期推广阶段,56%的婴儿通过两种疫苗接种获得了保护。 13,19 然而,随着临床医生意识的提高和后勤挑战的解决,预计接种率将会上升。 13,19-23 使用 nirsevimab 时,10 月至次年 3 月出生的婴儿在其出生月份接种疫苗,而 8 个月以下且出生在流行季接种窗口期之外的婴儿,则可在 10 月或 11 月的常规儿童保健检查时(即 2、4 或 6 个月大时)进行补种。根据美国疾病控制与预防中心(CDC)近期发布的免疫接种和调查数据, 19,20,22-24 在基线情景下,我们假设仅使用 nirsevimab 的策略接种率为 70%。我们没有纳入仅使用 RSVpreF 的策略,因为在妊娠 32 至 36 周进行季节性接种无法保护在 RSV 流行季之外出生的婴儿。即使全年服用 RSVpreF,母体抗体保护期也只有大约 6 个月,因此 RSV 流行季节期间许多婴儿将得不到保护,因此 ACIP 不建议仅采用 RSVpreF 策略。
对于混合策略,我们考虑了 RSVpreF 或 nirsevimab 的合理组合。RSVpreF 的接种时间为 9 月至次年 1 月,我们假设 10 月至次年 3 月出生的婴儿中,40%将通过母体接种获得免疫,而另外 30%的婴儿将在出生时接种 nirsevimab。 16 21 23 24 其他月份出生的婴儿则接种 nirsevimab 进行补种,同样假设接种率为 70%。在两种策略中,我们都假设获得 RSV 保护的婴儿总比例相同。
我们考虑了呼吸道合胞病毒(RSV)感染风险的季节性和年龄模式、免疫接种效力、保护持续时间、不良反应、免疫接种成本以及 RSV 相关的发病率和死亡率。成本效益采用增量成本效益比(ICER)进行评估。健康和经济结果则从医疗保健系统和社会角度,以质量调整生命年(QALY)进行评估。
模型描述
该模型追踪了每 12 个月出生队列,并在婴儿出生后的第一年内每月监测呼吸道合胞病毒(RSV)相关结局。我们的模型重点关注健康的足月儿和晚期早产儿,并未单独对高危婴儿进行建模。我们考虑了以下几种就诊情况下发生的 RSV 相关下呼吸道感染(MA RSV LRTI):门诊就诊、急诊就诊、非重症监护室(ICU)住院以及 ICU 住院。在医疗保健视角分析中,我们纳入了 RSV 相关的医疗费用和婴儿质量调整生命年(QALY)损失,以及背景死亡率和存活婴儿预期产生的终生医疗保健费用。在社会视角分析中,我们考虑了每例 MA RSV LRTI 病例导致的照护者生产力损失和效用损失,以及每例婴儿死亡导致的折现终生生产力损失和照护者丧亲之痛。
鉴于呼吸道合胞病毒(RSV)的极高流行率,且缺乏证据表明目前的 RSV 疫苗能够预防传播,我们选择不直接模拟传播过程,而是估算每月中重度呼吸道合胞病毒(RSV)下呼吸道感染(LRTI)病例的风险。 1,25 我们保守地假设每个婴儿最多发生 1 次呼吸道合胞病毒(RSV)下呼吸道感染,并且没有纳入 RSV 上呼吸道感染的发病率。我们没有模拟婴儿在不同医疗机构之间的转诊,而是假设婴儿直接转诊至病情最严重的医疗机构。我们假设,一旦进入某种疾病状态,婴儿要么在经历一个病程后完全康复,要么死亡。
根据出生月份和婴儿年龄调整了进入各 RSV 状态的月风险。 26,27 此外,还考虑了与免疫接种相关的不良事件,包括理论上可能因 RSVpreF 而增加的早产风险。 28-30 表 1 列出了所使用的 RSV 和免疫接种相关的成本和生活质量下降情况。
| 范围 | 价值 | 范围 | 来源 |
|---|---|---|---|
| MA RSV LRTI 门诊就诊的季节性发病率 | |||
| 0-5个月龄,足月 | 0.0826 | 0.0311–0.1323 | Gantenberg 等人 2022 年, 42 Hall 等人 2009 年, 3 Keisler-Starkey 等人 2023 年 43 |
| 6-11个月龄,足月 | 0.1105 | 0.0311–0.1770 | |
| 0-5个月龄,晚期早产儿 | 0.0934 | 0.0343–0.1323 | |
| 6-11个月大,晚期早产儿 | 0.1250 | 0.0343–0.1770 | |
| MA RSV LRTI 的季节性发病率及急诊就诊比例 | |||
| 0-5个月龄,足月 | 0.0336 | 0.0145–0.0543 | Gantenberg 等人 2022 年, 42 Hall 等人 2009 年, 3 Keisler-Starkey 等人 2023 年 43 |
| 6~11个月龄,足月 | 0.0350 | 0.0145–0.0567 | |
| 0-5个月龄,晚期早产儿 | 0.0428 | 0.0170–0.0543 | |
| 6-11个月大,晚期早产儿 | 0.0446 | 0.0170–0.0567 | |
| MA RSV LRTI 住院治疗的季节性发病率 | |||
| 0-5个月龄,足月 | 0.0195 | 0.0099–0.0195 | Gantenberg 等人 2022 年, 42 Hall 等人 2009 年, 3 Keisler-Starkey 等人 2023 年 43 |
| 6~11个月龄,足月 | 0.0061 | 0.0051–0.0128 | |
| 0-5个月龄,晚期早产儿 | 0.0426 | 0.0203–0.0426 | |
| 6-11个月大,晚期早产儿 | 0.0133 | 0.0051–0.0280 | |
| 因呼吸道合胞病毒(RSV)下呼吸道感染住院并转入重症监护室的比例 | |||
| 0-2个月龄,足月 | 0.1100 | 0.1100–0.3534 | McLaurin 等人 2016 年, 44 Arriola 等人 2019 年, 45 (上限) |
| 3~11个月龄,足月 | 0.0767 | 0.0767–0.2849 | |
| 0-2个月龄,晚期早产儿 | 0.2100 | 0.1988–0.3534 | McLaurin 等人 2016 年, 44; Arriola 等人 2019 年, 45 (上限);Rha 等人 2020 年, 46 (下限) |
| 3-11个月大,晚期早产儿 | 0.1233 | 0.1233–0.2849 | McLaurin 等人 2016 年, 44 Arriola 等人 2019 年, 45 (上限) |
| 免疫接种引起不良事件的概率 | |||
| Nirsevimab,婴儿严重不良事件(过敏反应) | 0.000005 | Chen 等人 2015 33 b | |
| 尼尔塞维单抗,婴儿轻度不良事件(全身反应) | 0.005 | Hutton 等人 2024 年 14 | |
| RSVpreF,母体严重不良事件(GBS) c | 0.0000015 | FDA 安全通讯, 30 Sejvar 等人 2011,47 Schonberger 等人 1979 48 | |
| RSVpreF,母体轻度不良事件(全身反应) | 0.011 | Kim DeLuca 等人 2023 49 天 | |
| RSVpreF,因轻微不良事件而进行门诊就诊 | 0.03 | ||
| 晚期早产的概率 | |||
| 研究人群中晚期早产儿的比例 | 0.0828 | Helfrich 等人 2015 年 50 | |
| RSVpreF 导致晚期早产的相对风险 | 1 | 1–1.03 | Kampmann 等人 2023 年第 29 页 |
| 医疗保健行业成本,美元 | |||
| 每月背景医疗保健费用 | 236 | 医疗支出小组调查 36 | |
| 门诊就诊 | 171 | 49–171 | Choi 和 Finelli 2023, 51 Bowser 等人 2022 52 (下限) |
| 急诊就诊 | 804 | 568–804 | Clopper 等人 2024, 35 Choi 和 Finelli 2023 51 (下限) |
| 未入住 ICU 的住院治疗,期限 | 12 456 | 9478–12456 | McLaurin 等人 2016,44 Choi 和 Finelli 2023 51 (下限) |
| 未入住重症监护室的住院治疗,晚期早产 | 18 081 | 9478–18081 | |
| 入住 ICU 的住院治疗,期限 | 47 128 | 29 282–47 128 | |
| 因重症监护室入院治疗,晚期早产 | 55 200 | 29 282–55 200 | |
| Nirsevimab 产品成本 | 485.441 | 50–600 | 美国疾病控制与预防中心疫苗价格表, 10 Hutton 等人 2024 14 (范围) |
| RSVpreF 产品成本 | 268.445 | 50–500 | 美国疾病控制与预防中心疫苗价格表, 10 Hutton 等人 2024 15 (范围) |
| 免疫接种 | 21.81 | CMS 医师收费标准 53 | |
| 尼尔塞维单抗,婴儿严重不良事件(需要住院治疗的过敏反应) | 8453.42 | Hutton 等人 2024 年 14 | |
| Nirsevimab,婴儿轻微不良反应(门诊就诊) | 93.63 | Prosser 等人 2023 年第 54 页 | |
| RSVpreF,母体严重不良事件(GBS) | 39 651.19 | Prosser 等人 2006 年 55 | |
| RSVpreF,孕妇轻微不良事件(例如,门诊就诊) | 93.63 | Prosser 等人 2023 年第 54 页 | |
| 定期交付 | 2863.96 | Speer 等人 2021 年第 56 页 | |
| 晚期早产 | 12 497.27 | ||
| 终身背景医疗保健费用折扣 | 163 519 | 医疗支出小组调查 48 | |
| 社会成本 | |||
| 照护者每日生产力损失成本,$ | 256.24 | 社会保障署全国平均工资指数 57 | |
| 每次门诊或急诊就诊导致照护者生产力损失的天数 | 2.5 | 0–7 | Glaser 等人 2022 年第 37 页 |
| 每次住院导致的照护者生产力损失天数 | 7.4 | 0-14 | |
| 每例婴儿死亡造成的终身生产力损失折现值,$ | 1 970 126.74 | Grosse 等人 2019, 58 Hutton 等人 2024 14 15 | |
| 5 个月免疫接种有效率,% | |||
| 奈塞维单抗,门诊/ 急诊 | 76.4 | 62.3–85.2 | Muller 等人 2023 年第 32 页 |
| 奈塞来昔布,无需入住 ICU 的住院治疗 | 76.8 | 49.4–89.4 | |
| 奈塞维单抗,入住 ICU e f | 78.6 | 48.8–91.0 | |
| RSVpreF,门诊/急诊科 | 52.5 | 28.7–68.9 | Kampmann 等人 2023 年第 29 页 |
| RSVpreF,无需入住 ICU 的住院治疗 | 56.4 | 5.2–81.5 | |
| RSVpreF,入住 ICU g h | 70.9 | 44.5–85.9 | |
| MA RSV LRTI 病例死亡率风险(按医疗机构划分) | |||
| 门诊 | 0.00128 | Reichert 等人 2022, 59 Hansen 等人 2022 60 | |
| ED | 0.00357 | ||
| 住院治疗 | 0.09807 | ||
| 每次呼吸道合胞病毒感染或免疫接种不良事件造成的质量调整生命年损失 | |||
| 婴儿效用损失,门诊 | 0.0085 | 0.0047–0.0455 | Glaser 等人 2022, 37 Hutton 等人 2024 14 15 (基本情况和上限),Shoukat 等人 2023 16 (下限) |
| 婴儿效用损失,ED | 0.0134 | 0.0079–0.0455 | |
| 婴儿效用损失,住院治疗 | 0.0170 | 0.0110–0.0726 | |
| 门诊照护者效用损失 | 0.0041 | 0–0.0249 | Glaser 等人 2022, 37 Hutton 等人 2024 14 15 (基准情况和上限) |
| 照护者效用损失,ED | 0.0068 | 0–0.0249 | |
| 照护者效用降低,住院治疗 | 0.0066 | 0–0.0373 | |
| 照护者效用损失,婴儿死亡(丧亲之痛) | 1.09 | Camacho 等人 2024 年 61 | |
| Nirsevimab,每例婴儿严重不良事件(需要住院治疗的过敏反应)的效用损失 | 0.0137 | 0.0137–0.02 | Kim DeLuca 等人 2023,49 d Prosser 等人 2006 55 (上限) |
| Nirsevimab,每例婴儿轻度不良事件的效用损失 | 0.0059 | Kim DeLuca 等人 2023 49 天 | |
| RSVpreF,每例孕产妇严重不良事件(GBS)的效用损失 | 0.0198 | 0.0198–0.141 | Kim DeLuca 2023, 49 d Prosser et al 2006 55 (上限) |
| RSVpreF,每例孕妇轻度不良事件的效用损失 | 0.0012 | Kim DeLuca 等人 2023 49 天 | |
| 其他生活质量因素 | |||
| 对晚期早产儿的健康效用 | 0.97 | 0.94–1 | Varley-Campbell 等人 2019 62 |
| 折扣后的终身质量调整生命年 | 28.50 | Lee 等人 2022 年第 38 页 | |
缩写:ED,急诊科;FDA,食品药品监督管理局;GBS,格林-巴利综合征;ICU,重症监护室;MA RSV LRTI,接受医疗救治的呼吸道合胞病毒相关下呼吸道感染;QALY,质量调整生命年。
各医疗机构中,6 个月平均季节性呼吸道合胞病毒(RSV)下呼吸道感染(LRTI)发病率可解释为 RSV 流行季(10 月至次年 3 月)期间预期发生该疾病的婴儿比例。模型中使用的月度发病率由季节性发病率计算得出,并根据各月出生队列的 RSV 季节性模式进行加权( 补充材料 1 )。
由于缺乏尼塞维单抗治疗过敏反应的发生率数据,因此使用帕利珠单抗上市后监测数据作为过敏反应发生率的替代指标。
在接种 RSVpreF 疫苗的老年患者中检测到了格林-巴利综合征(GBS)病例增多。美国食品药品监督管理局(FDA)已委托开展一项研究,旨在检测孕妇中 GBS 病例的增多情况。在我们的模型中,我们假设疫苗导致的 GBS 相对风险在孕妇和老年患者中相同。在相对风险相同的情况下,由于孕妇 GBS 的基线风险较低,因此孕妇中 GBS 病例的增多数量也会较少。因此,我们估计孕妇 GBS 的增多风险为每百万剂 RSVpreF 疫苗 1.5 例( 见补充表 3 )。
由于不良事件数据有限,因此以流感疫苗接种不良事件为依据的估计值被用作 RSVpreF 引起轻微全身反应和门诊就诊概率的替代指标,并用于估计每次不良事件的效用损失。
有关 nirsevimab 的完整疗效假设的详细信息,请参见补充图 1 。
据报道,Nirsevimab 对“非常严重的”MA RSV LRTI 的疗效被用作其预防住院和入住 ICU 疗效的替代指标。
有关 RSVpreF 的完整功效假设的详细信息,请参见补充图 2 。
据报道,RSVpreF 对“严重”MA RSV LRTI 的疗效被用作其预防住院和入住 ICU 的疗效的替代指标。
有关病死率风险计算的详细信息,请参阅补充材料 2 。
模型输入
流行病学投入
各地区每月 MA RSV 下呼吸道感染的发病率均来自文献中报道的季节性发病率和 RSV 季节性估计值( 表 1 )。尽管每个 RSV 流行季的时间和持续时间各不相同,但截至 2024-2025 流行季,其模式似乎已恢复到疫情前的基线水平。 26,27 因此,我们基于美国疾病控制与预防中心(CDC)国家呼吸道和肠道病毒监测系统(NRVS)的疫情前月度数据,计算了 RSV 传播的季节性轨迹。 26 补充图 3 解释了如何计算和应用代表季节性的月度权重。
RSV 相关死亡风险的计算基于各场景下的死亡比例估计值和 RSV 总体死亡率( 补充材料 2,补充表 1 )。在条件允许的情况下,参数值按早产程度(足月儿与晚期早产儿)和年龄进行分层。我们未考虑与 RSV 相关的任何长期后遗症。我们纳入了基于美国疾病控制与预防中心国家生命统计系统 31 数据计算的月度背景死亡率( 补充表 2 )。
免疫接种效力投入
Nirsevimab 和 RSVpreF 的疗效数据直接来源于各自 3 期临床试验的 5 个月终点。 29,32 对于这两种产品,我们假设给药后前 5 个月疗效完全且稳定,随后呈线性下降,至 10 个月时疗效降至 0%( 补充图 1 和 2 )。 16 我们考虑了轻度和重度不良事件( 表 1 )。上市后数据显示,RSVpreF 疫苗接种会增加格林-巴利综合征的风险,因此将其纳入重度不良事件。 30 虽然在 nirsevimab 试验中未观察到过敏性休克事件,但根据 palivizumab 观察到的风险,我们假设其风险较低。 33
成本投入
鉴于约有一半的美国儿童符合联邦政府资助的儿童疫苗计划 (VFC) 的资格,我们采用私营部门每剂疫苗价格与 VFC 每剂疫苗价格(RSVpreF 为 268.45 美元,nirsevimab 为 485.44 美元)的平均值计算了免疫接种成本 10 14 15 34 ,并额外加上了 21.81 美元的管理费用( 表 1 ) 35 。门诊、急诊、非重症监护室住院和重症监护室住院相关的医疗费用;免疫接种相关不良事件的费用;因呼吸道合胞病毒 (RSV) 下呼吸道感染导致的照护者生产力损失;以及因婴儿死亡导致的终生生产力损失(折现值)均根据文献估算( 表 1 )。此外,我们还纳入了基于医疗支出调查 (Medical Expenditure Panel Survey) 的每月背景医疗保健费用 36 。所有费用均已调整为 2024 年美元。
生活质量投入
我们考虑了因呼吸道合胞病毒(RSV)感染导致的婴儿质量调整生命年(QALY)损失,参数值来源于一项关于 RSV 对生活质量影响的系统评价。 37 在我们的社会视角分析中,我们考虑了因照护者溢出效应导致的 QALY 损失( 表 1 )。婴儿死亡导致的 QALY 损失则使用预期折现终生 QALY 进行估算。 38
分析
免疫接种的结果和影响
我们模拟了婴儿呼吸道合胞病毒(RSV)下呼吸道感染(LRTI)的门诊就诊、急诊就诊和住院(包括 ICU 和非 ICU)情况,分析周期为 1 年,并结合预期终生结局,估算了平均医疗保健成本、生产力损失以及每名婴儿的质量调整生命年(QALY)损失。我们通过将经历每种 RSV 相关结局的婴儿比例乘以 2024 年美国足月和晚期早产儿出生队列的规模,计算了每种情况下 MA RSV LRTI 病例数和死亡人数作为中间结局。39 未来预期终生成本和 QALY 均按 3%的年贴现率进行折现。
基准案例分析
我们进行了增量成本效益分析,将每种策略与次优策略进行比较。增量成本效益比(ICER)以美元/质量调整生命年(QALY)为单位,分别从医疗保健部门和社会角度进行评估。我们考虑了 15 万美元/QALY 的支付意愿阈值,这是评估新干预措施成本效益的常用基准。 40 作为一项次要分析,我们考虑了仅使用尼塞维单抗作为唯一可行的免疫策略的情况,例如,当 RSVpreF 疫苗不可用或因指南变更而被排除在外时。
敏感性分析
我们进行了大量的单因素和双因素敏感性分析,以识别社会视角分析中的影响变量。鉴于尼塞维单抗(nirsevimab)因其高昂的价格而备受诟病,我们尤其关注产品成本。 12,13 此外,考虑到这些免疫产品的疗效尚不明确,且近期研究结果表明尼塞维单抗的实际疗效似乎高于临床试验得出的疗效, 41 我们认为有必要研究模型结果对免疫疗效的敏感性。最后,RSVpreF 临床试验提示可能与早产风险增加有关,但这种关联并不具有统计学意义。 29,63 另一项类似的基于蛋白质的呼吸道合胞病毒疫苗(RSVPreF 3 -Mat)的试验因安全性问题而提前终止,因为疫苗组的早产率显著高于安慰剂组。 63 64 在我们的基本情况下,我们假设 RSVpreF 不会增加早产的风险,但我们在敏感性分析中测试了晚期早产儿出生率增加的影响。
我们的社会视角分析结果与医疗保健行业分析结果存在显著差异。因此,我们对每例婴儿死亡导致的照护者质量调整生命年(QALY)损失、生产力损失和终身生产力损失进行了单因素和双因素敏感性分析,以评估它们对模型结果的影响。
结果
免疫接种的健康结果和影响
混合治疗策略可避免 134,859 例门诊就诊、48,215 例急诊就诊、21,743 例住院(包括 2,389 例 ICU 住院)和 25 例死亡( 表 2 )。对于预计因 RSV 感染需要住院治疗的婴儿,该策略可使质量调整生命年 (QALY) 增加 21 个。相反,仅使用尼塞维单抗的治疗策略可避免 144,575 例门诊就诊、52,131 例急诊就诊、23,663 例住院(包括 2,475 例 ICU 住院)和 27 例死亡;对于预计因 RSV 感染需要住院治疗的婴儿,该策略可使质量调整生命年 (QALY) 增加 22 个。
免疫接种人数及免疫策略对呼吸道合胞病毒感染结果的影响
| 免疫策略 | 接种疫苗的婴儿人数 | RSV 治疗结果 | |||||||
|---|---|---|---|---|---|---|---|---|---|
| RSVpreF | 尼尔塞维单抗 | 全部的 | 门诊就诊 | 急诊就诊 | 住院人数 | 重症监护室住院 | 死亡人数 | ||
| 未接种疫苗 | 全部的 | 0 | 0 | 0 | 365 322 | 128 011 | 51 593 | 5205 | 60 |
| RSVpreF 和 nirsevimab | 全部的 | 704 827 | 1 749 122 | 2 453 949 | 230 463 | 79 796 | 29 850 | 2817 | 35 |
| 避免的案例 | 134 859 | 48 215 | 21 743 | 2389 | 25 | ||||
| 仅使用尼塞维单抗 | 全部的 | 0 | 2 453 949 | 2 453 949 | 220 746 | 75 880 | 27 930 | 2730 | 33 |
| 避免的案例 | 144 575 | 52 131 | 23 663 | 2475 | 27 | ||||
美国足月儿和晚期早产儿人群中免疫接种剂量、呼吸道合胞病毒(RSV)感染病例和死亡人数的统计数据。由于四舍五入,估计计数可能略有出入。
缩写:ED,急诊科;ICU,重症监护室;RSV,呼吸道合胞病毒。
基准案例分析
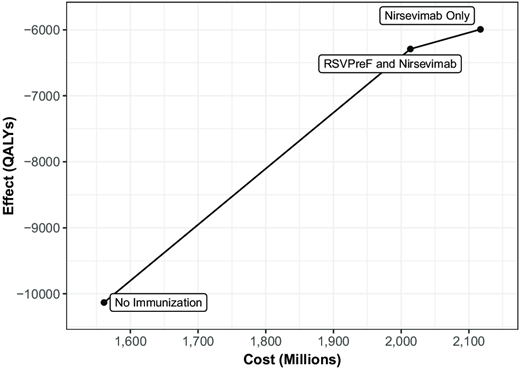
在医疗保健领域分析中,基于当前平均产品价格和呼吸道合胞病毒(RSV)发病率估计值,两种干预策略的增量成本效益比(ICER)均大于 15 万美元/质量调整生命年(QALY)(表 3 )。在社会视角分析中,混合策略将导致 10.93 亿美元的免疫接种成本、5.96 亿美元的 RSV 相关医疗保健成本以及 3.24 亿美元的生产力损失成本,总计 20.14 亿美元——高于不进行免疫接种的成本( 表 4 )。然而,混合策略可带来 2789 个 QALY 的净收益,因此具有成本效益,其 ICER 为 117848 美元/QALY( 表 3 , 表 5 )。与混合策略相比,仅使用尼塞维单抗的策略成本高出 1.03 亿美元,但可额外获得 298 个 QALY;该策略不具有增量成本效益,其增量成本效益比为 347,821 美元/质量调整生命年( 图 2 , 表 3 )。如果将 RSVpreF 从考虑范围中移除,则仅使用 nirsevimab 的策略与不进行免疫接种相比具有成本效益,其增量成本效益比为 134,391 美元/质量调整生命年。
成本效益
| 战略 | 成本(百万美元) | QALY 损失 | 增量成本(百万美元) | 增量质量调整生命年 (QALY) 增益 | ICER,$/QALY |
|---|---|---|---|---|---|
| 医疗保健行业视角下的成本效益结果 | |||||
| 未接种疫苗 | 1029 | 7357 | |||
| RSVpreF 和 nirsevimab | 1689 | 4568 | 660 | 2789 | 236 582 |
| 仅使用尼塞维单抗 | 1809 | 4352 | 120 | 216 | 555 637 |
| 社会视角下的成本效益结果 | |||||
| 未接种疫苗 | 1561 | 10 132 | |||
| RSVpreF 和 nirsevimab | 2014 | 6291 | 453 | 3840 | 117 848 |
| 仅使用尼塞维单抗 | 2117 | 5994 | 103 | 298 | 347 821 |
缩写:ICER,增量成本效益比;QALY,质量调整生命年。
美国足月和晚期早产婴儿人群中呼吸道合胞病毒 (RSV) 及 RSV 免疫接种相关成本细分(百万美元)
| 医疗保健成本 | Productivity Costs | Total Cost | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 干涉 | 门诊 | ED | 医院,无重症监护室 | 医院,重症监护室 | RSV 死亡率 | RSV 总成本 | 医疗保健总成本 | Outpatient | ED | Hospital, No ICU | Hospital, ICU | RSV Mortality | Total | ||
| 未接种疫苗 | 0 | 62 | 103 | 618 | 256 | -10 | 1029 | 1029 | 234 | 82 | 88 | 10 | 118 | 532 | 1561 |
| RSVpreF 和 nirsevimab 总 | 1093 | 39 | 64 | 360 | 139 | -6 | 596 | 1689 | 148 | 51 | 51 | 5 | 69 | 324 | 2014 |
| RSVpreF 和 nirsevimab 的区别 | 1093 | −23 | −39 | −258 | −118 | 4 | −433 | 660 | −86 | −31 | −37 | −5 | −49 | −207 | 453 |
| 仅使用 Nirsevimab 的总 | 1246 | 38 | 61 | 336 | 134 | -5 | 563 | 1809 | 141 | 49 | 48 | 5 | 65 | 308 | 2117 |
| 仅使用奈塞维单抗的差异 | 1246 | −25 | −42 | −282 | −122 | -9 | −466 | 766 | −93 | −33 | −40 | −5 | −53 | −224 | 542 |
我们报告了每种策略的详细成本构成,以及每种干预策略与不进行免疫接种之间的成本差异。负数表示节省。干预成本包括免疫接种产品成本、接种管理成本以及与免疫接种不良事件相关的成本。RSV 导致的死亡可节省医疗保健成本,因为婴儿死亡无需支付预期的终身医疗保健支出。表中未包含非 RSV 背景死亡相关的成本。
缩写:ED,急诊科;ICU,重症监护室;QALY,质量调整生命年;RSV,呼吸道合胞病毒。
针对足月和晚期早产儿,分析每种策略下呼吸道合胞病毒(RSV)感染和 RSV 免疫接种导致的美国婴儿质量调整生命年(QALY)损失,以及每种策略与不接种疫苗相比的 QALY 损失差异。
| 婴儿质量调整生命年损失 | 照护者质量调整生命年损失 | Total QALYs | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 干涉 | 门诊 | ED | 医院,无重症监护室 | 医院,重症监护室 | RSV 死亡率 | 全部的 | 门诊 | ED | Hospital, No ICU | Hospital, ICU | RSV Mortality | Total | ||
| 未接种疫苗 | 0 | 3095 | 1713 | 784 | 88 | 1677 | 7357 | 1497 | 874 | 304 | 34 | 65 | 2774 | 10 132 |
| RSVpreF 和 nirsevimab 总 | 61 | 1952 | 1068 | 457 | 47 | 982 | 4568 | 945 | 545 | 177 | 18 | 38 | 1723 | 6291 |
| RSVpreF 和 nirsevimab 的区别 | 61 | −1142 | −645 | −327 | −40 | −695 | −2789 | −553 | −329 | −127 | −16 | −27 | −1051 | −3840 |
| 仅使用 Nirsevimab 的总 | 73 | 1870 | 1016 | 426 | 46 | 921 | 4352 | 905 | 518 | 165 | 18 | 36 | 1642 | 5994 |
| 仅使用奈塞维单抗的差异 | 73 | −1225 | −698 | −358 | −42 | −756 | −3005 | −593 | −356 | −139 | −16 | −29 | −1133 | −4138 |
干预措施导致的质量调整生命年(QALY)损失包括免疫接种引起的不良事件。表中未包含因背景死亡率导致的 QALY 损失。
缩写:ED,急诊科;ICU,重症监护室;QALY,质量调整生命年;RSV,呼吸道合胞病毒。
敏感性分析
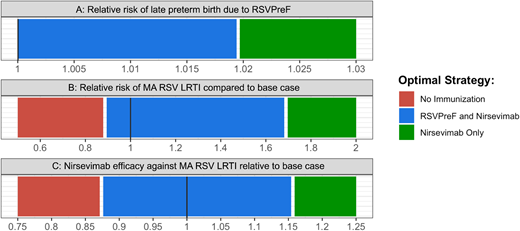
研究结果对 RSVpreF 可能导致的晚期早产风险增加较为敏感。如果 RSVpreF 导致晚期早产风险相对增加 2%或以上,则优先选择仅使用 nirsevimab 的策略( 图 3A )。此外,RSV 风险估计值的范围较广,表明存在高度不确定性。 3,31 例如,如果每月因 MA RSV 下呼吸道感染住院的发生率增加到敏感性范围的上限,则与不进行免疫接种相比,混合策略的增量成本效益比(ICER)将为 4277 美元/质量调整生命年(QALY)。如果发生率下降到下限,则两种策略均不具有成本效益,ICER 将超过 150000 美元/QALY( 图 4 )。总体而言,如果所有情况下 MA RSV 下呼吸道感染的每月绝对发生率均比基线情况高出 69%,则优先选择仅使用 nirsevimab 的策略。相反,如果每月发病率降低 11%,则两种策略均不具有成本效益( 图 3B )。
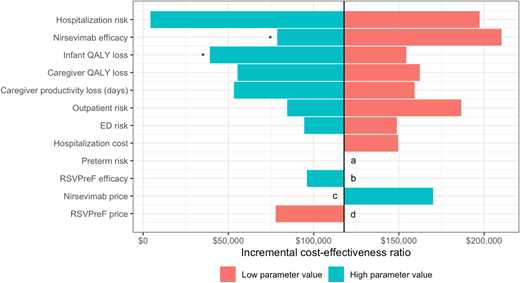
单因素敏感性分析显示了混合使用 RSVpreF 和 nirsevimab 策略与不干预相比的增量成本效益比(ICER)。彩色条形图显示了在高低参数值假设下的 ICER。该图以基线情景的 ICER 为中心,因此条形图的长度表示参数值高低变化时 ICER 的变化。如果对于给定的参数值假设,ICER 与基线情景相比没有变化,则不显示条形图。如果在给定的参数值假设下,混合策略被单独使用 nirsevimab 策略强劣或弱劣,则不显示条形图。如果混合策略被强劣,则意味着其疗效低于单独使用 nirsevimab 策略,但成本更高。如果混合策略被弱劣,则意味着单独使用 nirsevimab 策略成本更高、疗效更高、ICER 更低。
*如果尼塞维单抗的疗效或婴儿质量调整生命年损失较高,则与混合策略相比,仅使用尼塞维单抗的策略更可取。
a 如果 RSVpreF 导致早产的风险较高,则混合策略略逊于仅使用 nirsevimab 的策略。
b 如果 RSVpreF 的疗效较低,则混合策略将完全被仅使用 nirsevimab 的策略所压制。
c 如果每剂 nirsevimab 的成本降至 50 美元,则仅使用 nirsevimab 的策略可以节省成本,而混合策略则明显处于劣势。
d 如果 RSVpreF 每剂的成本上升到 500 美元,那么混合策略就完全被仅使用 nirsevimab 的策略所支配。
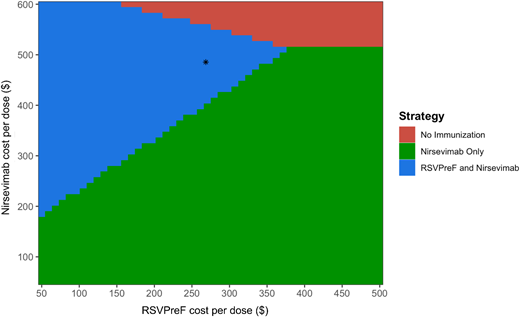
我们的模型对两种产品的疗效都非常敏感。当 nirsevimab 的疗效达到上限时,单用 nirsevimab 的策略更优( 图 4 )。具体而言,如果 nirsevimab 在所有医疗环境中的疗效提高 16%,则单用 nirsevimab 的策略更优( 图 3C )。相反,如果 RSVpreF 的疗效设定为上限,则混合策略更优,其增量成本效益比(ICER)为 96101 美元/质量调整生命年(QALY)。然而,如果 RSVpreF 的疗效比基线情况降低 22%,则单用 nirsevimab 的策略更优。最后,如果 nirsevimab 的价格降至 401.89 美元,则单用 nirsevimab 的策略更优( 图 5 )。
在比较社会视角和医疗保健视角分析的差异时,若将照护者损失纳入考量,而忽略婴儿死亡造成的终身生产力损失,则混合策略的增量成本效益比(ICER)为 130,551 美元/质量调整生命年(QALY)。如果所有照护者的生产力损失和效用损失均降低 39%或更多,则两种策略均不具备成本效益。
讨论
概述
我们的分析表明,从社会角度(即考虑照护者生产力损失等因素)来看,在美国,对于低风险足月儿和晚期早产儿,采用 RSVpreF 疫苗和 nirsevimab 联合免疫策略预防 MA RSV 下呼吸道感染具有成本效益,其成本为 117,848 美元/QALY(以 150,000 美元/QALY 的支付意愿阈值计算)。然而,假设 nirsevimab 的临床疗效高于 RSVpreF 疫苗,则仅使用 nirsevimab 进行免疫接种可以避免更多 MA RSV 下呼吸道感染事件的发生。从医疗保健的角度来看(即,仅考虑医疗成本),如果两种产品的成本降低 23%(RSVpreF,205.90 美元;nirsevimab,372.33 美元),混合免疫策略仍然具有成本效益,ICER 低于 150,000 美元/QALY。
据我们所知,目前尚无其他已发表的成本效益研究比较这两种新型呼吸道合胞病毒(RSV)防护产品在美国婴幼儿中的联合应用。然而,免疫实践咨询委员会(ACIP)在其建议中分别对每种产品进行了成本效益分析。 14,15 鉴于 ACIP 决定同时推荐这两种产品,我们的研究结果强调,儿科医生和产科医生共同为各自的患者接种疫苗是预防婴幼儿 RSV 相关下呼吸道感染最具成本效益的方法。这种混合策略也为临床医生和家庭提供了灵活性,他们可以根据个人偏好、临床考虑以及每种方法的相对优势,选择是为母亲接种疫苗还是为婴儿接种疫苗。 65
首选免疫策略的成本效益受多种因素影响。如果将尼塞维单抗的平均单剂成本降低至 401.89 美元,则基于成本效益标准及其在降低呼吸道合胞病毒 (RSV) 相关下呼吸道感染 (LRTI) 事件方面的临床影响,单用尼塞维单抗的策略将更具优势。同样,如果尼塞维单抗在真实世界中的有效性比临床试验中观察到的有效性高出 16%,则单用尼塞维单抗的策略也更受青睐。这一发现意义重大,因为目前针对孕妇 RSVpreF 的真实世界有效性研究有限,而 2023-2024 年呼吸道合胞病毒流行季尼塞维单抗的真实世界有效性早期估计值已显示,其对 RSV 相关急性呼吸道感染的有效率为 89%,对 RSV 相关住院的有效率为 93%。 62 66
每种产品的免疫接种率也是我们分析中的一个重要因素。尽管由于供应链问题,2023-2024 年的免疫接种率可能显著降低,但这些问题在 2024-2025 年已基本得到解决,早期数据显示接种率有所提高。 22-24 作者也意识到,新的免疫接种措施的实施可能并不完美,每种产品免疫接种率的变化可能会影响两种免疫策略的呼吸道合胞病毒 (RSV) 防治效果。
局限性
本研究存在一些局限性。由于这些产品由不同的制药公司研发,临床试验方法上的差异可能导致产品难以直接比较。虽然呼吸道合胞病毒(RSV)感染导致重症或并发症的风险随年龄增长而降低,但鉴于现有文献有限,我们无法按月对风险进行分层。然而,我们尝试将风险分为两个年龄组:0 至 5 个月和 6 至 11 个月。同样,我们分析中的参数也仅限于已发表的、区分足月儿和晚期早产儿的数据。对于以下参数,我们对两组均采用了相同的值:RSV 感染相关的质量调整生命年(QALY)损失、RSV 死亡率以及门诊和急诊就诊费用。最后,我们的模型没有考虑人际传播 RSV;考虑到 RSV 感染的高发病率和高风险,纳入这些数据将使这些策略更具成本效益。
政策启示
本研究旨在评估 ACIP 目前关于在呼吸道疾病流行季节为母亲或婴儿接种疫苗以预防儿童呼吸道合胞病毒(RSV)感染的建议的成本效益。鉴于尼塞维单抗(nirsevimab)的单剂成本较高,仅依靠儿科医生为婴儿接种疫苗似乎并非最具成本效益的方案。因此,从社会角度来看,与产科合作伙伴携手实施最佳实践,尽可能多地为婴儿接种疫苗,才是最具成本效益的方案。目前儿科医生在实施过程中面临的障碍包括难以确定母亲的 RSV 疫苗接种情况,而这对于确定婴儿是否符合尼塞维单抗的接种条件至关重要。 13 同样,由于尼塞维单抗成本较高,降低其价格的机制(例如,通过协商、减少自付费用)可能使其成为从社会和医疗保健部门角度来看更具成本效益的策略,同时,由于其疗效优于 RSVpreF 疫苗,还能更好地保护婴儿。
结论
美国免疫实践咨询委员会 (ACIP) 建议,为母亲接种 RSVpreF 疫苗或为婴儿注射尼塞维单抗,以预防美国低风险婴儿发生呼吸道合胞病毒 (RSV) 相关下呼吸道感染 (LRTI),这是一种具有成本效益的策略。儿科医生和产科医生应合作推荐 RSV 疫苗接种,因为这是一种具有社会成本效益的婴儿保护方法。同时,他们还应倡导降低尼塞维单抗的单剂成本,使其作为单一策略,从社会角度来看比联合用药更具成本效益。
曾先生和曾先生构思并设计了本研究,收集数据,进行数据分析,撰写了初稿,并对稿件进行了审阅和修改。Shah 先生和陈博士构思并设计了本研究,收集数据,撰写了初稿,并对稿件进行了审阅和修改。Asch 博士、Salomon 博士和 Owens 博士构思并设计了本研究,并对稿件进行了审阅和修改。所有作者均已审阅并同意最终提交的稿件,并对本研究的各个方面负责。
利益冲突声明: 作者声明不存在任何利益冲突。
资金来源: 本研究未获得任何资金支持。
| 英文缩写 | 英文全称 | 中文译名 |
|---|---|---|
| ACIP | Advisory Committee on Immunization Practices | 免疫实践咨询委员会 |
| CDC | Centers for Disease Control and Prevention | 疾病控制与预防中心 |
| ED | emergency department | 急诊科 |
| ICER | incremental cost-effectiveness ratio | 增量成本效果比 |
| ICU | intensive care unit | 重症监护室 |
| MA RSV LRTI | medically attended respiratory syncytial virus–associated lower respiratory tract infection | 需就医治疗的呼吸道合胞病毒相关下呼吸道感染 |
| QALY | quality-adjusted life-year | 质量调整生命年 |
| RSV | respiratory syncytial virus | 呼吸道合胞病毒 |
| VFC | Vaccines for Children | 儿童疫苗计划 |
参考
Hits: 17
相关文章:
- 尼尔塞维单抗与 RSVpreF 疫苗治疗新生儿呼吸道合胞病毒相关住院的比较
- RSVpreF 疫苗在成人中耐受性良好,显示出良好的安全性
- 妊娠期 RSVpreF 疫苗接种的中期安全性
- Nirsevimab 项目在两个流行季内降低了 RSV 住院率
- 母亲呼吸道合胞病毒疫苗接种和小于8个月的婴儿接受呼吸道合胞病毒抗体(Nirsevimab)——美国,2024年4月
- Nirsevimab 可能有助于预防婴幼儿除呼吸道合胞病毒 (RSV) 以外的严重呼吸道疾病
- 分析表明,nirsevimab 可将婴儿呼吸道合胞病毒 (RSV) 住院率降低 83%
- 两项法国研究证明了 nirsevimab 保护婴儿的有效性
- RSV 单克隆抗体 nirsevimab 对婴儿的有效性为 83%
- Nirsevimab 对婴儿 RSV 显示出很强的真实世界有效性
- 住院婴儿呼吸道感染因 nirsevimab RSV 抗体而暴跌
- Nirsevimab 给药
- Nirsevimab 在健康足月儿中对 RSV 表现出高效
- Nirsevimab(Beyfortus®、赛诺菲和阿斯利康)VIS
- 3 项研究:Nirsevimab 对婴儿重症呼吸道合胞病毒感染疗效显著;干预措施可提高其使用率
Powered by YARPP.