Effectiveness of COVID-19 Vaccination and Prior Infections to Reduce Long COVID Risk During the Pre-Omicron and Omicron Periods
摘要
我们根据接种剂量和既往感染史,估算了 Omicron 疫苗接种前和接种 Omicron 疫苗期间针对 COVID-19 和长 COVID 的疫苗有效性 (VE)。
我们结合了来自加拿大魁北克省一组医护人员的调查信息、免疫登记数据和实验室管理数据。我们将 COVID-19 病例定义为有症状且经实验室确诊的感染,将长期 COVID 定义为持续 ≥12 周的自我报告症状。我们采用检测阴性设计,根据感染史分层评估了疫苗对 COVID-19 和长期 COVID 的有效性。在 Omicron 疫苗接种前,我们将接种疫苗的参与者与未接种疫苗的参与者进行比较;在 Omicron 疫苗接种期间,我们将接种疫苗的参与者与在实验室检测前 ≥6 个月接种过两次疫苗的参与者进行比较。
分析纳入了 8230 名 COVID-19 患者和 43361 份检测样本。在 Omicron 疫苗应用前,单剂和双剂疫苗对 COVID-19 的疫苗有效率分别为 75%(95% CI:64–83)和 95%(95% CI:84–98),对长期 COVID 的疫苗有效率分别为 91%(95% CI:79–96)和 87%(95% CI:22–98)。在 Omicron 疫苗应用期间,加强剂疫苗对 COVID-19 的疫苗有效率为 41%(95% CI:34–47),对长期 COVID 的疫苗有效率为 57%(95% CI:46–66),并在 6 个月后逐渐下降。接种疫苗且先前感染过的个体的混合疫苗效力范围为 81%(95% CI:38-94)至 92%(95% CI:87-95),无论接种剂量、先前感染的变异株或距上次免疫事件的中位时间(最长 9 个月)如何。
在 Omicron 疫苗接种计划实施前,新冠疫苗可以预防新冠后遗症;在 Omicron 疫苗接种计划实施后,新冠后遗症的风险降低了一半以上。鉴于目前大部分人口已经接种疫苗并感染了病毒,重复接种加强针可能对预防新冠后遗症的额外益处有限。这一观察结果对公共卫生、免疫规划和成本控制都具有重要意义。
长新冠是一种慢性感染后疾病,通常会影响日常生活,可能影响全球超过 4 亿人 [ 1 , 2 ]。
大多数评估疫苗对新冠长期症状风险保护作用的研究仅针对新冠病例进行评估,而忽略了通过预防严重急性呼吸综合征冠状病毒 2 (SARS-CoV-2) 感染(包括重症新冠)来降低早期(上游)风险的作用[ 3 , 4 ]。自奥密克戎疫苗问世以来,疫苗对感染的有效性似乎降低且持续时间缩短[ 5 ]。虽然少数将新冠长期症状视为重症新冠后遗症的研究发现,疫苗对新冠长期症状的保护作用较低至中等,但关于混合免疫(疫苗加感染诱导的免疫)有效性的数据仍然匮乏[ 6-8 ]。
在加拿大,与其他地区一样,新冠疫苗接种计划的目标是预防重症,并且由于疫苗保护期较短,需要每 6-12 个月接种一次加强针[ 9 , 10 ]。在目前新的 Omicron 亚型持续传播和高频率再感染的情况下,评估加强针对预防新冠长期症状的持续保护作用仍然至关重要。
2023 年春季,我们对魁北克省的一组医护人员进行了一项在线调查,以评估新冠长期症状的发生率、风险因素和保护因素[ 11 ]。我们将调查数据与行政登记数据相结合,根据接种剂量(1-5 剂)、既往感染史和流行的 SARS-CoV-2 毒株,估算了疫苗对 COVID-19 和新冠长期症状的有效性。为了与其他研究进行比较,我们还测量了疫苗接种对 COVID-19 病例风险降低的影响。
方法
研究设计
我们采用检测阴性设计 (TND) 评估了疫苗对 COVID-19 的有效性,并采用回顾性队列设计 (RCD) 估计了疫苗与 COVID-19 长期风险降低相关的效果。
人口
居住在加拿大魁北克省的成年医护人员,如果在疫情期间在公共医疗和社会服务网络中工作,和/或已在医生、护士、护理助理、呼吸治疗师、药剂师或助产士等专业机构注册,并且能够用法语或英语交流,则受邀参与一项在线调查。研究人群包括在 2021 年 1 月 3 日(魁北克疫苗接种活动启动 3 周后)至 2023 年 2 月 20 日期间(允许进行 12 周的随访以确定长期新冠病例)接受过 SARS-CoV-2 核酸扩增检测(NAAT)的调查参与者。我们排除了以下 COVID-19 患者:(1)如果其首次自我报告的 COVID-19 病例未在实验室登记中得到 NAAT 阳性结果的确认(允许自我报告日期与实验室检测日期之间有 60 天的滞后);(2)如果调查回复无法识别长期新冠或将其归因于 COVID-19 感染。 (3) 如果接种疫苗超过 5 剂,或最后一剂并非 mRNA 疫苗,或两次接种间隔不足 3 个月。对于混合免疫分析,如果参与者第二次自述的 COVID-19 感染未通过实验室登记的核酸扩增检测 (NAAT) 阳性结果确认,或在首次感染后报告出现新冠长期症状,则也被排除在外。
程序
2023 年 5 月 16 日至 2023 年 6 月 15 日期间,参与者自行报告了社会人口学和临床数据。问题包括 COVID-19 发作的次数、日期、实验室确诊情况和严重程度,以及 COVID-19 感染后 12 周以上是否仍存在至少一种症状[ 11 ]。利用唯一标识符,调查数据与省级卫生行政数据库关联,包括:免疫接种登记系统;魁北克省综合慢性病监测系统(QICDSS),其中包含基于人群的合并症信息[ 12 ];以及包含自疫情爆发以来所有 SARS-CoV-2 核酸扩增检测(NAAT)及其检测原因的实验室登记系统。在魁北克省,医护人员在疫情爆发的第一年接受了广泛的 NAAT 检测,并且在 Omicron 系统运行期间,他们仍然可以便捷地获得 NAAT 检测。
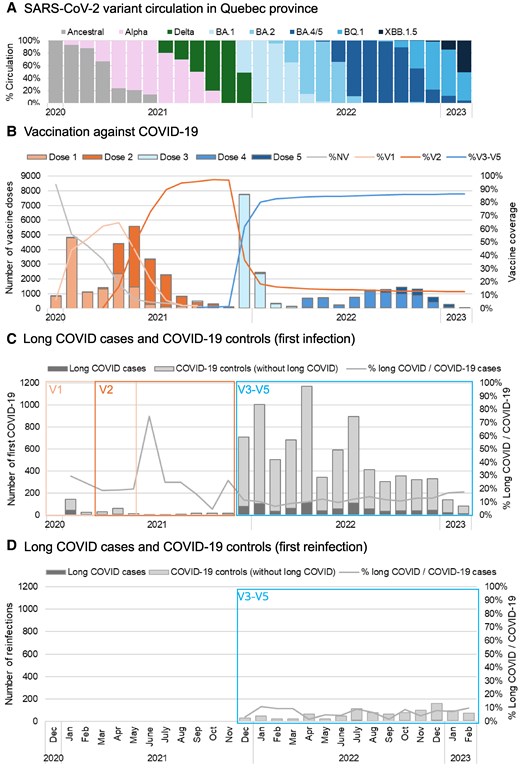
根据魁北克病毒基因监测数据,将 Omicron 毒株的主要流行期分为 Omicron 毒株出现前(2021 年 1 月 3 日至 2021 年 12 月 18 日)和 Omicron 毒株流行期(2021 年 12 月 19 日至 2023 年 2 月 20 日),具体方法已在其他文献中描述[ 13 ]。研究期间,主要的 Omicron 毒株亚型为 BA.1、BA.2、BA.4/5、BQ.1 和 XBB.1.5( 图 1 )。
暴露和结果定义
疫苗接种状态的定义以样本采集日期为准。若受试者(或检测对象)在核酸扩增检测(NAAT)日期前≥14 天(V1)或≥7 天(V2-V5)接种过一剂 mRNA 疫苗(辉瑞-BioNTech 公司的 BNT-162b2 或 Moderna 公司的 mRNA-1273),则视为接种了 1 至 5 剂疫苗(V1 至 V5);若未接种任何 COVID-19 疫苗,则视为未接种疫苗(NV)。混合免疫的定义基于接种的疫苗剂次(V2-V5)以及既往经 NAAT 确诊的 Omicron 病毒感染(感染前或感染 Omicron 病毒),且无 COVID-19 长期症状。
新冠病毒感染病例为医护人员在接受新冠病毒症状核酸扩增检测(NAAT)时呈阳性,检测结果以记录为准。首次再感染定义为在首次 NAAT 检测呈阳性后≥90 天再次进行 NAAT 检测呈阳性。所有分析中的长新冠病例均定义为自我报告持续存在新冠病毒感染后症状(共 21 种症状)的个体,这些症状归因于新冠病毒感染(首次感染或首次再感染),且经实验室登记的 NAAT 检测证实。中度或重度长新冠病例定义为存在≥1 种持续存在的中度或重度症状。
为了评估疫苗对 COVID-19 和长 COVID 的有效性 (VE),符合条件的阴性对照组为在首次(如有)核酸扩增检测 (NAAT) 呈阳性之前出现症状但 NAAT 检测结果为阴性的参与者。在首次感染后 ≥90 天且在首次(如有)再次感染之前进行的阴性检测也符合混合保护评估的条件。为了评估疫苗在 COVID-19 病例中降低风险的有效性 (RCD),对照组为感染 SARS-CoV-2(首次感染或首次再次感染)但未出现长 COVID 症状的个体(COVID-19 对照组)。方法概述见补充图 1 。
统计分析
根据疫苗接种剂量和变异株演变情况,我们在 Omicron 疫苗上市前评估了单剂和双剂疫苗的疫苗有效性 (VE),并在 Omicron 疫苗上市期间评估了加强针的疫苗有效性,具体评估依据各剂次疫苗的供应情况( 图 1 )[ 14 , 15 ]。我们使用 2021 年 1 月 3 日(流行病学周 W2021-01)至 2021 年 6 月 12 日(W2021-23)期间检测的样本评估了 V1(针对诺如病毒),此时原始毒株和 Alpha 变异株仍在流行。我们使用 2021 年 3 月 28 日(W2021-13)至 2021 年 12 月 11 日(W2021-49)期间检测的样本评估了 V2(针对诺如病毒),此时原始毒株、Alpha 和 Delta 变异株仍在流行。我们使用 2021 年 12 月 19 日(W2021-51)至 2023 年 2 月 20 日(W2023-08)期间(奥密克戎疫苗流行期间)检测的样本,评估了加强剂量(V3-V5)和混合免疫(与 V2 组相比,V2 组接种时间距检测日期≥6 个月,且无既往感染记录或自我报告)。由于在奥密克戎疫苗流行期间未接种疫苗的参与者数量稀少,且接种疫苗后 6 个月内对奥密克戎疫苗的保护作用减弱[ 16 ],因此选择 V2 组作为加强剂量评估的对照组。我们通过将每次加强剂量与检测日期≥6 个月前接种的前一次剂量进行比较,来评估连续加强剂量的保护作用。这些亚组分析包括自 W2021-51(V3)、W2022-14(V4)和 W2022-35(V5)以来进行的检测。我们还按距上次加强疫苗接种的时间,以 2 个月为间隔进行分层。
为了评估 TND 疫苗的有效性[ 17 ],我们采用发病率密度抽样法,在每个两周时间段内,每个病例随机选择 10 个检测阴性对照(V1 和 V2 分析)或最多 5 个检测阴性对照(V3-V5 分析)。通过日历时间匹配,控制了研究期间病例和对照分布变化以及 COVID-19 疫苗接种可能造成的混杂因素[ 18 ]。我们采用条件 logistic 回归分析,比较检测阳性 COVID-19 病例和长 COVID 病例与检测阴性对照,并调整性别、年龄组、居住地区、职业、工作场所、物质和社会剥夺指数以及既往合并症数量等因素,估计比值比(OR)和 95%置信区间(95% CI)。对于 RCD 估计长 COVID 风险降低 [ 19 , 20 ],通过逻辑回归模型比较长 COVID 病例和 COVID-19 对照组(即未出现长 COVID 的 COVID-19 病例),并调整上述相同变量和 4 周时间段,估计 OR 和 95% CI。绝对 VE(V1 和 V2 与 NV 相比)和相对 VE(V3-V5 与 V2 相比)和风险降低的计算公式为:(1-OR adjusted )*100。
伦理考量
本研究是在魁北克省公共卫生局局长依据《公共卫生法》的法律授权下进行的,并得到了魁北克大学附属医院-拉瓦尔大学研究伦理委员会的批准。
结果
在受邀的 400,222 名魁北克省医护人员中,有 22,496 人(5.6%)完成了调查。其中,10,281 名(45.7%)SARS-CoV-2 感染者与实验室登记册中相应的核酸扩增检测(NAAT)结果相关联,7,679 名(34.1%)未关联,4,536 名(20.2%)为未感染者( 见补充图 2 )。排除上述人员后,分别有 43,361 份和 38,653 份 NAAT 结果符合 TND 分析 COVID-19 和长 COVID-19 疫苗效力分析的条件;另有 8,230 名首次感染者和 923 名首次再感染者被纳入 RCD 风险降低分析。
在所有分析中,病例组和对照组的特征总体相似,大多数参与者为白人中年女性( 表 1 , 补充表 1 )。在检测结果为阴性的对照组中,分别有 45.1%和 43.0%的人在 Omicron 疫苗接种前后至少患有一种合并症;而在长期新冠病例组中,相应比例分别为 45.3%和 48.6%( 表 1 )。按疫苗接种情况划分,观察到类似比例( 补充表 2 )。
| 奥密克戎前体 | 奥米克戎 | |||||
|---|---|---|---|---|---|---|
| 新冠病毒检测呈阳性病例 | 新冠后遗症 | 检测阴性对照 a | 新冠病毒检测呈阳性病例 | 新冠后遗症 | 检测阴性对照 a | |
| N | 310 | 95 | 16 663 | 5306 | 849 | 20 414 |
| 特征 | 氮(%) | 氮(%) | 氮(%) | 氮(%) | 氮(%) | 氮(%) |
| 性别 | ||||||
| 女性 | 270 (87.1) | 81 (85.3) | 14 295 (85.8) | 4537 (85.5) | 743 (87.5) | 17 734 (86.9) |
| 男性 | 40 (12.9) | 14 (14.7) | 2368 (14.2) | 769 (14.5) | 106 (12.5) | 2680 (13.1) |
| 年龄(岁) | ||||||
| 中位数(四分位距) | 43(35–50) | 45(36–53) | 42(35–51) | 44(36–52) | 45(38–53) | 43(36–52) |
| 18–39 | 129 (41.6) | 34 (35.8) | 6806 (40.9) | 2018 (38.0) | 252 (29.7) | 8271 (40.5) |
| 40–49 | 98 (31.6) | 30 (31.6) | 5316 (31.9) | 1716 (32.3) | 298 (35.1) | 6120 (30.0) |
| 50–59 | 59 (19.0) | 20 (21.1) | 3173 (19.0) | 1130 (21.3) | 216 (25.4) | 4435 (21.7) |
| ≥60 | 24 (7.7) | 11 (11.6) | 1366 (8.2) | 442 (8.3) | 83 (9.8) | 1588 (7.8) |
| 种族/民族 | ||||||
| 白色的 | 246 (79.4) | 73 (76.8) | 14 658 (88.0) | 4706 (88.7) | 730 (86.0) | 18 406 (90.2) |
| 黑色的 | 24 (7.7) | 7 (7.4) | 682 (4.1) | 168 (3.2) | 34 (4.0) | 753 (3.7) |
| 亚洲 | 12 (3.9) | 1 (1.1) | 314 (1.9) | 129 (2.4) | 23 (2.7) | 336 (1.6) |
| 西班牙裔 | 9 (2.9) | 4 (4.2) | 714 (4.3) | 84 (1.6) | 18 (2.1) | 237 (1.2) |
| 其他/未报告 | 19 (6.1) | 10 (10.5) | 295 (1.7) | 219 (4.1) | 44 (5.2) | 682 (3.3) |
| 合并症 b | ||||||
| 没有任何 | 171 (55.2) | 52 (54.7) | 9142 (54.9) | 3094 (58.3) | 436 (51.4) | 11 630 (57.0) |
| 一 | 71 (22.9) | 20 (21.1) | 4326 (26.0) | 1305 (24.6) | 222 (26.1) | 5019 (24.6) |
| 两个或两个以上 | 68 (21.9) | 23 (24.2) | 3195 (19.2) | 907 (17.1) | 191 (22.5) | 3765 (18.4) |
| 职业 | ||||||
| 护理人员、医生和其他卫生专业人员 | 181 (58.4) | 48 (50.5) | 10 893 (65.4) | 3341 (63.0) | 481 (56.7) | 14 082 (60.9) |
| 健康辅助职业 | 72 (23.2) | 30 (31.6) | 3704 (22.2) | 994 (18.7) | 208 (24.5) | 4150 (20.3) |
| 管理和行政人员 | 57 (18.4) | 17 (17.9) | 2066 (12.4) | 971 (18.3) | 160 (18.8) | 2182 (10.7) |
| 工作场所 | ||||||
| 医院 | 133 (42.9) | 50 (52.6) | 8736 (52.4) | 2602 (49.0) | 384 (45.2) | 12 434 (60.9) |
| LTCF | 58 (18.7) | 13 (13.7) | 3021 (18.1) | 589 (11.1) | 133 (15.7) | 3140 (15.4) |
| 诊所 | 37 (11.9) | 11 (11.6) | 1865 (11.2) | 813 (15.3) | 123 (14.5) | 1862 (9.1) |
| 其他 c | 82 (26.5) | 21 (22.1) | 3041 (18.3) | 1302 (24.5) | 209 (24.6) | 2978 (14.6) |
| 感染变种 | ||||||
| 祖先 | 125 (40.3) | 43 (45.3) | NA | NA | NA | NA |
| 阿尔法 | 133 (42.9) | 38 (40.0) | NA | NA | NA | NA |
| 三角洲 | 52 (16.8) | 14 (14.7) | NA | NA | NA | NA |
| 奥密克戎 BA.1 | NA | NA | NA | 1811 (34.1) | 231 (27.2) | NA |
| 奥密克戎 BA.2 | NA | NA | NA | 1580 (29.8) | 231 (27.2) | NA |
| 奥密克戎 BA.4/5 | NA | NA | NA | 1475 (27.8) | 288 (33.9) | NA |
| 奥密克戎 BQ.1 | NA | NA | NA | 411 (7.7) | 91 (10.7) | NA |
| Omicron XBB.1.5 | NA | NA | NA | 29 (0.5) | 8 (0.9) | NA |
| 最后一剂 mRNA 疫苗的类型 | ||||||
| 一价 | 123 (39.7) | 29 (30.5) | 12 557 (75.4) | 5086 (95.9) | 810 (95.4) | 19 928 (97.6) |
| 二价 | 0 (0.0) | 0 (0.0) | 0 (0.0) | 197 (3.7) | 37 (4.4) | 445 (2.2) |
缩写:IQR,四分位距;LTCF,长期护理机构;NA,不适用。
a 符合密度抽样条件的阴性对照试验与 COVID-19 检测阳性或新冠长期病例相匹配。
b 合并症包括:抑郁症、酒精和药物滥用、高血压、慢性肺病、甲状腺功能减退症、肾病、体液和电解质紊乱、外周血管疾病、肥胖症、痴呆症、脑血管疾病、神经系统疾病、肝病、精神病、肺循环障碍、类风湿性关节炎、凝血功能障碍、体重减轻、瘫痪、溃疡性疾病、艾滋病/HIV、贫血、心血管疾病、糖尿病、免疫系统问题、癌症。
c 康复中心、患者家中、远程办公、其他。
疫苗接种情况随时间变化( 图 1 )。2021 年 12 月,96.9% 的参与者接种了两剂疫苗,3%~1% 的参与者未接种疫苗。到 2022 年 2 月,加强疫苗接种率达到 82.2%,13.7% 的医护人员在研究期间未接种任何加强剂。总体而言,大多数首发感染是由 Omicron 疫苗引起的,包括长期 COVID 病例(849 例 [89.0%])和 COVID-19 检测阳性病例(5306 例 [93.7%]; 图 1 )。在 Omicron 疫苗接种期间,分别有 18 例(2.1%)和 43 例(5.1%)长期 COVID 病例在 Omicron 疫苗接种前和接种期间有核酸扩增检测 (NAAT) 确诊的既往感染,而 COVID-19 对照组的相应比例分别为 267 例(3.6%)和 589 例(8.0%)( 补充表 3 )。
在 Omicron 疫苗上市前,根据 TND 估计的单剂疫苗对 COVID-19 的绝对疫苗有效率 (VE) 为 75%(95% CI:64–83),对 COVID-19 长期症状的疫苗有效率增至 91%(95% CI:79–96),RCD 估计 COVID-19 感染的医护人员发生 COVID-19 长期症状的风险降低了 77%(95% CI:38–82)( 表 2 )。根据 TND 估计的两剂疫苗对 COVID-19 的疫苗有效率 (VE) 为 95%(95% CI:84–98),对 COVID-19 长期症状的疫苗有效率 (VE) 为 87%(95% CI:27–98),在 7 个月的随访期间未见疫苗效力减弱的迹象( 补充表 4 和 5 )。RCD 未发现接种两剂疫苗的感染医护人员发生 COVID-19 长期症状的风险降低。
| 参与者 | ||||
|---|---|---|---|---|
| 案例 | 控制 | 接种疫苗后的月数(中位数(四分位距)) | 调整后的 VE(%)或风险降低(%)(95% CI) a,b | |
| COVID-19 VE 分析,TND | ||||
| 病例对照定义 | 2019冠状病毒病病例 | 检测结果为阴性 | … | … |
| NV(Omicron 前时期) c | 180 (80.4) | 1254 (56.0) | NA | 参考 |
| V1 | 44 (19.6) | 986 (44.0) | 1.6 (0.8–2.8) | 75%(64–83) |
| NV(Omicron 前时期) d | 44 (36.7) | 299 (24.9) | NA | 参考 |
| V2 | 76 (63.3) | 901 (75.1) | 5.4 (3.8–6.8) | 95%(84–98) |
| V2_6m(奥密克戎周期) e | 702 (14.3) | 1190 (11.3) | 7.9 (7.0–9.5) | 参考 |
| V3-V5 | 4219 (85.7) | 9376 (88.7) | 2.7 (1.1–4.4) | 41%(34–47) |
| 长期新冠疫苗有效性分析,TND | ||||
| 病例对照定义 | 新冠长期症状 | 检测结果为阴性 | … | … |
| NV(Omicron 前时期) c | 65 (89.0) | 426 (58.4) | NA | 参考 |
| V1 | 8 (11.0) | 304 (41.6) | 1.6 (0.8–2.7) | 91%(79-96) |
| NV(Omicron 前时期) d | 14 (40.0) | 109 (31.1) | NA | 参考 |
| V2 | 21 (60.0) | 241 (68.9) | 5.4 (3.6–6.9) | 87%(27-98) |
| V2_6m(奥密克戎周期) e | 138 (17.5) | 369 (9.4) | 9.0 (7.5–12.5) | 参考 |
| V3-V5 | 652 (82.5) | 3559 (90.6) | 3.7 (2.0–6.4) | 57%(46-66) |
| 长期新冠风险降低分析,RCD | ||||
| 病例对照定义 | 新冠长期症状 | 新冠肺炎疫情防控 | … | … |
| NV(Omicron 前时期) c | 65 (89.0) | 158 (73.8) | NA | 参考 |
| V1 | 8 (11.0) | 56 (26.2) | 2.5 (1.4–3.0) | 77%(38–92) |
| NV(Omicron 前时期) d | 14 (40.0) | 42 (38.5) | NA | 参考 |
| V2 | 21 (60.0) | 67 (61.5) | 5.6 (4.2–6.9) | −122% (−2119–78) |
| V2_6m(奥密克戎周期) e | 138 (17.5) | 773 (11.9) | 8.0 (6.9–10.5) | 参考 |
| V3-V5 | 652 (82.5) | 5747 (88.1) | 3.7 (2.0–6.2) | 47%(33–57) |
缩写:CI,置信区间;IQR,四分位距;NA,不适用;NV,未接种疫苗;RCD,回顾性队列设计;RR,风险降低;TND,检测阴性设计;V1-V5,接种 1 至 5 剂疫苗;V2_6m,在检测日期前 ≥6 个月接种 2 剂疫苗;VE,疫苗有效性;W,流行病学周。
a 逻辑回归模型以两周为周期,比较了接种疫苗且之前未感染的参与者与未接种疫苗的参与者(Omicron 疫苗接种前时期)或在测试前 6 个月或更长时间接种 2 剂疫苗的参与者(Omicron 疫苗接种时期),并根据年龄组、性别、居住地区、职业、工作场所、物质和社会剥夺指数、合并症数量进行了调整。
b 疫苗有效性和风险降低计算公式为(1—调整后的 OR)×100。
c W2021-01 至 2021-23。
d W2021-13 至 2021-49。
e W2021-51 至 2023-08。
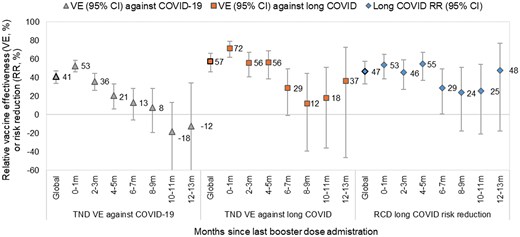
在 Omicron 疫苗接种期间,根据 TND 检测,加强剂量疫苗的疫苗有效率(V3-V5 相对于 V2)为:针对首次感染 COVID-19 为 41%(95% CI:34–47),针对首次感染后长期 COVID 为 57%(95% CI:46–63)( 表 2 )。接种后 2 个月内,疫苗有效率更高,针对 COVID-19 为 53%(95% CI:46–58),针对长期 COVID 为 72%(95% CI:62–79)( 补充表 4 和 5 )。然而,与 Omicron 疫苗接种前 V1 和 V2 的疫苗有效率不同,加强剂量疫苗的疫苗有效率随时间推移持续下降,在接种后 6 个月时降至较低且无统计学意义(针对 COVID-19 为 13% [95% CI:-6 至 28],针对长期 COVID 为 29% [95% CI:-1 至 50])( 图 2 )。接种 Omicron 疫苗前感染与针对 COVID-19 再感染的混合疫苗效力 (VE) 为 60% (95% CI: 51–67) 相关;接种 Omicron 疫苗前感染的混合疫苗效力范围为 76% (95% CI: 69–81) 至 79% (95% CI: 75–83)( 图 3 , 补充表 6 )。接种 Omicron 疫苗前感染与针对长 COVID 的混合疫苗效力相似,接种两剂疫苗者为 87% (95% CI: 72–94),接种加强剂者为 85% (95% CI: 73–91) 至 92% (95% CI: 87–95)( 图 3 , 补充表 7 )。对于不同的既往感染和疫苗剂量组合,再感染后长 COVID 的风险降低幅度在 65% 至 79% 之间,置信区间较大( 图 3 , 补充表 8 )。
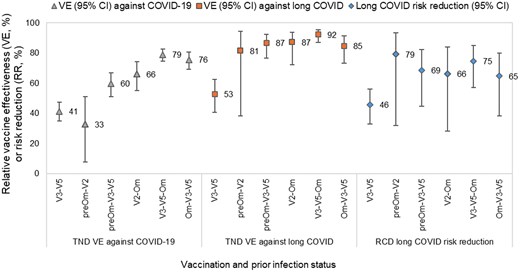
在奥密克戎疫苗接种期间,接种疫苗和既往感染与 COVID-19 和长 COVID 的保护作用相关。采用逻辑回归模型比较了接种疫苗且既往感染或未感染的参与者与接种两剂疫苗(接种时间距检测时间≥6 个月)且无既往感染记录或自我报告的参与者。缩写:CI,置信区间;PreOm-V2,接种两剂疫苗前在奥密克戎疫苗接种期间发生过感染;PreOm-V3-V5,接种三至五剂疫苗前在奥密克戎疫苗接种期间发生过感染;RCD,回顾性队列研究设计;RR,风险降低;TND,检测阴性设计;V2-Om,接种两剂疫苗后在奥密克戎疫苗接种期间发生过感染;V3-V5,接种三至五剂疫苗且无既往感染;V3-V5-Om,接种三至五剂疫苗后在奥密克戎疫苗接种期间发生过感染;Om-V3-V5,接种三至五剂疫苗前在奥密克戎疫苗接种期间发生过感染;VE,疫苗有效性。
尽管再次感染后出现长期 COVID 病例的数量太少,无法按上次免疫事件发生的时间进行分层,但无论上次接种疫苗的中位时间如何(范围从 2 个月到 9 个月不等),VE 估计值都相似( 补充表 3 )。
在所有情况下,针对中度或重度症状的长期 COVID 的估计 VE 与针对长期 COVID 的总体保护相似( 补充表 9 )。
讨论
本研究分析了疫苗对新冠长期症状的保护作用,结合了超过 14000 名医护人员的调查数据(这些医护人员均有登记确认的疫苗接种记录和 SARS-CoV-2 感染记录),进一步揭示了预防 COVID-19 感染的重要益处。虽然在量化疫苗对新冠长期症状的益处时,预防感染似乎显而易见,但大多数先前的分析都忽略了这一关键方面,仅考虑了预防已感染者出现新冠长期症状。在 Omicron 疫苗接种前,我们发现新冠疫苗可将新冠长期症状的风险降低约 90%,这主要是通过降低 COVID-19 疾病的风险实现的。在 Omicron 疫苗接种期间,首次感染后接种加强针预防新冠长期症状的有效率约为 60%,并在接种后 6 个月开始下降。相反,既往感染后接种 2-5 剂疫苗的混合疫苗预防新冠长期症状的有效率达到 80%至 90%,并且在接种剂量、既往感染毒株或接种后中位时间(长达 9 个月)方面没有进一步变化。
尽管已有超过 80 项研究探讨了疫苗接种对新冠长期症状的影响 [ 3 ],但大多数研究仅纳入了 SARS-CoV-2 感染者,并且报告了突破性感染后新冠长期症状风险的降低,而这些降低不能被解读为疫苗的总体有效性 [ 4 , 21 , 22 ]。我们的研究不仅报告了新冠病例中疫苗对新冠长期症状的疗效,还报告了相对于非病例的疗效,从而更全面地反映了疫苗的益处。此外,我们还计算了疫苗对新冠本身的有效性,以便更好地理解风险降低的估计结果。
在 Omicron 疫苗问世之前,两项涵盖四个欧洲国家的研究估计,单剂疫苗对新冠长期症状的有效率为 35% 至 58%,远低于我们 91% 的估计值 [ 7 , 8 ]。这些研究利用行政健康记录,将新冠长期症状定义为存在 ≥1 种核心新冠长期症状,但并未明确归因于 COVID-19。此前一项使用相同数据来源的英国研究报告称,单剂疫苗对 COVID-19 的有效率为 57% 至 75% [ 23 ]。与针对 COVID-19 的有效率相比,针对新冠长期症状的有效率反而更低,这表明针对新冠长期症状的有效率可能被低估了。报告单剂疫苗可降低 COVID-19 患者中新冠长期症状风险的研究并未观察到疫苗保护作用,估计值范围为 -4% 至 4% [ 24-26 ]。大多数评估第二剂疫苗对新冠肺炎患者额外保护作用的研究报告显示,长期新冠风险降低了 3%至 50%,范围从 22%到 49%不等[ 21 , 24 , 26-28 ]。相反,我们观察到,对于在奥密克戎疫苗接种前已发生突破性感染的患者,接种一剂疫苗可使长期新冠风险降低 77%,但没有证据表明接种两剂疫苗的感染患者在预防长期新冠方面有额外获益。这一结果必须结合魁北克省第二剂疫苗接种的延迟以及两剂疫苗对新冠肺炎的极高疫苗效力来解读,因为接种两剂疫苗后仍感染的个体数量较少,难以评估其对新冠肺炎病例预防长期新冠的额外保护作用[ 29 ]。
在奥密克戎疫苗接种期间,一项基于捷克行政数据和医生诊断的长期新冠病例的全国性研究报告称,加强针对长期新冠的有效率仅为 20%,而其对重症新冠肺炎的有效率估计为 50%至 80%,且在接种后 10 个月的随访期内呈下降趋势[ 6 ]。我们观察到,在接种疫苗后的前两个月,长期新冠的有效率为 72%,新冠肺炎的有效率为 53%,但其随时间推移呈下降趋势。在奥密克戎疫苗感染病例中,加强针接种使长期新冠风险降低了一半,但在接种后 6 至 11 个月,风险降至 24%至 29%。这与大多数已发表的研究结果一致,这些研究报告称,加强针可使长期新冠风险降低 15%至 70%[ 19 , 30-32 ],而其他一些研究则报告称没有保护作用[ 20 , 26 , 28 ]。
鉴于大多数人已经感染过 SARS-CoV-2,混合免疫提供的保护目前最为重要。在我们的研究中,混合免疫与在接种 Omicron 疫苗后再次感染时预防长期 COVID-19 的高有效性(3%~80%)相关,且与疫苗接种剂量和先前感染的可能毒株无关。这一结果高于 Czeck 研究的估计值[ 6 ]。另一项研究也表明,在调整疫苗接种情况和流行毒株后,先前感染与长期 COVID-19 风险降低 86%相关[ 33 ]。我们的研究克服了以往研究的重要局限性,例如排除了疫苗接种前的时期[ 34-37 ]、准确确定了疫苗接种相对于感染的时间[ 38-40 ]以及采用了更具体的长期 COVID-19 定义(例如,将 COVID-19 后出现的症状归因于实验室确诊的 COVID-19)[ 7 ]。纳入疫苗接种前的时期会高估疫苗有效性,因为已知疫苗接种前时期的毒株与较高的长期 COVID-19 风险相关[ 33 ]。大多数基于行政数据的研究使用非特异性定义,很少使用 ICD-10 代码诊断新冠长期症状[ 41 ]。那些使用特定医生诊断的研究也可能受到就医行为的干扰,后者与接种疫苗和新冠长期症状的诊断可能性均相关[ 6,42 ]。
像我们这样的基于队列调查的研究也存在局限性。为了减少因自我报告的 COVID-19 持续症状而导致的分类错误,我们仅纳入了调查时已确诊的病例,以减少回忆偏差,并纳入实验室确诊的 COVID-19 病例。此外,我们还针对中度或重度 COVID-19 长期症状进行了二次分析,从而提高了结果的特异性。调查参与率低可能导致结果代表性不足(例如,重度 COVID-19 长期症状患者可能更愿意参与),但针对中度/重度 COVID-19 长期症状的保护率与总体估计值相似。在 Omicron 疫苗接种期间,未接种疫苗的参与者人数不足,无法测量绝对疫苗效力。根据其他研究,上次接种疫苗时间距今 ≥6 个月的个体可能未获得保护,因此构成了一个有效的对照组 [ 16 , 43 ],但这限制了我们在 Omicron 疫苗接种期间测量两剂疫苗效力的能力。未记录的既往感染可能低估疫苗有效性[ 44 ],但医护人员在 Omicron 疫苗接种前时期享有不受限制的检测权限并接受了系统性检测;我们也排除了那些自述既往感染但缺乏核酸扩增检测(NAAT)确认的人员。医护人员仅被询问了首次出现新冠长期症状的情况。因此,只有在首次感染后未出现新冠长期症状的人员才符合混合免疫评估的条件。宿主对新冠长期症状的易感性降低,而非疫苗或既往感染诱导的免疫力,可能部分解释了观察到的与混合免疫相关的保护作用。 我们的医护人员群体在人口统计学特征和合并症方面与其他已报道的医护人员群体相似[ 17,45 ] ,但是我们的研究结果可能无法推广到更广泛的人群,包括儿童或老年人。
总体而言,我们的研究结果有力地证实了新冠疫苗接种能够预防新冠后遗症,并增强对新冠疾病的保护作用。接种疫苗并同时感染过新冠病毒(Omicron 病毒)可对感染 Omicron 病毒后的新冠后遗症提供最高的保护。我们的研究证实了新冠疫苗接种计划在降低新冠后遗症风险方面的重要作用,尤其是在 Omicron 病毒出现之前,但自 Omicron 病毒出现以来也发挥了一定的作用,鉴于 Omicron 病毒的后代仍在传播,其意义依然存在。然而,在当前疫苗接种率和感染率都很高的背景下,我们发现无论加强针的剂量或接种疫苗后的时间长短,对新冠后遗症的混合保护效果都相似,这表明重复接种疫苗不太可能带来显著的额外益处。鉴于其对公共卫生、疫苗接种计划和成本的重要影响,这一观察结果值得其他研究者进一步调查和证实。
补充数据
补充材料可在以下网址获取: 《临床传染病》 在线版。本刊所载数据由作者提供,旨在帮助读者。由于所发布材料未经编辑,作者对其内容负全部责任,因此如有任何疑问或评论,请联系通讯作者。
笔记
致谢。 作者感谢 Stéphanie Grenier 和 Josiane Rivard(魁北克大学附属医院研究中心)协调和实施新冠长期症状调查的工作,以及 Aissatou Fall 博士(加拿大公共卫生署)对研究方案讨论和初步结果的贡献。最后,我们感谢所有慷慨参与调查的医护人员。
作者贡献。 所有作者均可完全访问研究中的所有数据,并对数据的完整性和数据分析的准确性负责。概念和设计:SC、GDS、DMS、CS 和 DT。数据采集、分析或解释:所有作者。撰写初稿:SC。对稿件的重要知识内容进行审阅和修改:所有作者。统计分析:JP、MO 和 SC。监督:GDS 和 SC。
数据可用性。 本研究中使用的数据库属于魁北克省卫生和社会服务部 (Ministère de la Santé et des Services sociaux du Québec) 所有,并根据魁北克省公共卫生局局长依据《公共卫生法》的法律授权与研究人员共享,因此不得与第三方共享数据。汇总数据可在正文和补充材料中找到。用于统计分析的 SAS 代码已在 GitHub 代码库 ( https://github.com/JoPhi-immun/VE-against-Long-COVID ) 中共享。
资金支持。 本研究由加拿大公共卫生署资助。长期新冠调查由魁北克省卫生和社会服务部资助。本研究还获得了魁北克研究基金会(FRQ)通过研究中心拨款的资助。
潜在利益冲突。SC 、JP、MO 和 KG 报告称,加拿大公共卫生署和魁北克省卫生和社会服务部为其所在机构开展此项研究提供了资助。DMS 报告称,其所在机构获得了加拿大公共卫生署、太平洋公共卫生基金会、加拿大卫生研究院和迈克尔·史密斯健康研究基金会的资助,但与目前的研究工作无关。DT 获得魁北克研究基金会 (FRQ) 研究职业奖的资助。其他作者均声明无利益冲突。
所有作者均已提交 ICMJE 利益冲突披露表。编辑认为与稿件内容相关的利益冲突均已披露。
数据可用性
本研究使用的数据库属于魁北克省卫生和社会服务部所有,并根据魁北克省公共卫生局局长依据《公共卫生法》的法律授权与研究人员共享,因此不得与第三方共享数据。汇总数据可在正文及补充材料中找到。
参考
Hits: 31
相关文章:
- 新冠与流感严重程度相似,但 Omicron BA.5 患者更容易死亡
- 原始单价 mRNA 疫苗对儿童和青少年 COVID-19 Omicron 相关住院治疗的有效性的持久性——美国,2021-2023 年
- COVID-19 疫苗在 delta 和 omicron 期间对儿童和青少年非常有效
- 新型冠状病毒变异体的基因组监测:Omicron XBB和JN.1谱系的循环——美国,2023年5月至2024年9月
- SARS-CoV-2 Omicron 感染后免疫力可能比之前毒株后更快地减弱
- COVID 和流感联合疫苗的结果看起来很有希望——以下是它如何有益于公众健康
- 研究确定女性、心脏病是长期 COVID 危险因素,疫苗接种是保护性因素
- 涉及近 185,000 名患者的新研究建议增强癌症患者对 COVID-19 的免疫力
- 癌症患者应及时接种 COVID-19 加强针
- 与《人民之声》的标题相反,COVID-19疫苗并没有“杀死数百万人”,而是防止了死亡
- 接种 COVID 疫苗的孩子哮喘症状的发生率可能较低
- 接种疫苗可以预防严重冠状病毒肺炎后的精神问题
- CDC 研究表明,接种疫苗的儿童患长期 COVID 的风险降低 57% 至 73%
- 最新研究表明,新冠病毒仍会导致重症,但最新的疫苗是有效的
- 新冠肺炎指南,第二部分:感染预防
Powered by YARPP.

孟博士您好,关于我的接种想问问您。感谢您可以回复我
我的接种是一个跨度很长的全程,我不知道这是否有效果。
我曾经在2024年6月发生了第一次暴露,被猫抓但是没流血,不过我还是在2024年7.1,7.4接种了五针法的前两针疫苗。
然后在2025年的4月份再老家又发生了一次暴露,当时没有让我引起足够的重视。回老家发现当时和我玩闹的那只狗其实没多久就死掉了。后来我就在2025年的9.4,9.11,9.25顺着去年7.1,7.4接种了剩下三针。
以下是我的问题。
您看像我这样,24年7.1,7.4,25年9.4,9.11,9.25。这样五针可以算一个中间间隔14个月的全程吗,这样的接种是否足够帮我排除风险呢?我现在很纠结要不要重新接种一个全程。
今天我暴露刚好过去一年了,一般来说潜伏期一年的概率大吗?
1.是全程
2.如果再次暴露只需要加强