Fetal tissue use in vaccines [Imported Post from 03/09/2021]
为了帮助促进此博客及其内容向 substack 的迁移,我导入了这篇文章以回应最近对此事的担忧。
以下文章最初发表于 2021 年 3 月 9 日的 deplatformdisease.com。为了适应当前的上下文,它已进行了轻微修改。
您可能听说过疫苗在生产过程中利用胎儿组织,这可能会引发一些问题。我在下面详细阐述了以下所有内容,但这里有一些背景可以帮助您解决问题:
- 从中获得这些细胞的堕胎发生在几十年前,而这些细胞本身与那些原始胎儿相差许多代。
- 无论这些细胞随后是否用于疫苗生产,都会发生给我们这些细胞的选择性流产。换句话说,这不是在将细胞用于生物医学研究和保留怀孕之间做出选择,而是在利用堕胎对我们的生物学和医学知识做出积极贡献之间做出选择。
- 这些堕胎已经能够为这些疫苗的生产提供足够的材料,它们已经持续了几十年并继续为我们服务。疫苗行业并没有为了制造而积极地从堕胎中采购组织。它不需要。
- 来自这些胎儿细胞株的疫苗已经预防了数十亿种疾病,挽救了数百万人的生命。没有疫苗含有实际的胎儿细胞或组织。细胞的唯一目的是作为工厂制造疫苗抗原,然后将这些抗原纯化出来。这些细胞的 DNA 在制造过程中通过核酸酶处理而被破坏。
- 疫苗的历史告诉我们,通常,用于制造人类疫苗的最佳细胞是人类细胞,理想情况下,那些没有机会被其他病毒污染的细胞,使胎儿细胞成为理想的候选者(历史见下文)。
- 多个宗教权威已经就这个问题发表了意见,他们并不认为疫苗在道德上受到了损害,以至于服用借助胎儿细胞制造的疫苗是不道德的,其中包括天主教会(尽管许多人认为,如果没有该技术生产的替代品可用,则应改用这些替代品)。
- 然而,我确实认识到,一个人的宗教信仰可能不被宗教学者的团体所代表,他们就这个问题发表了自己的想法,所以我在这里把重点放在了使用这些细胞的事实上,而不是道德上,我觉得我在这里没有资格对这些方面发表意见,因为我不是一个宗教学者。未来,我们可能会有替代使用胎儿组织进行疫苗生产的方法,但目前这些技术还没有完全准备好成为标准。
- 我非常强烈地认为,不应利用对胎儿细胞使用的担忧来拒绝只能通过接种疫苗获得的基本保护。我只会鼓励努力寻求替代技术,这些技术可以生产出与今天通过人类细胞株生产的疫苗一样安全、有效和廉价的疫苗,但截至目前,该技术对于生产拯救生命的疫苗仍然至关重要。
对于任何可能对使用胎儿组织生产疫苗的历史有浓厚兴趣的人来说,梅雷迪思·瓦德曼 (Meredith Wadman) 的《疫苗竞赛》是一本了解更多信息的好书。
在医学研究中使用胎儿细胞通常会引起许多热情洋溢的意见,因为这个话题必然与人们对堕胎的看法有关,而堕胎是人们深深持有的、真诚的信念,这些信念影响着他们的思考。为了保持一个集中的范围,我不会在这里讨论堕胎,除非承认所讨论的胎儿细胞最初来自堕胎。
原则上,我将在这里集中解释(以我能做到的最冷静和客观的方式):
- 为什么首先使用胎儿细胞
- 为什么(目前)还没有合适的替代方案来替代它们的使用(但将来可能会出现哪些替代方案)
- 与特定 COVID-19 疫苗的相关性
基本原理
首先,针对病毒的疫苗需要大量生产这些病毒,但病毒不能自行繁殖(这是病毒定义的一部分)——它们需要一个宿主细胞来提供它们,以便它们可以复制。此外,理想情况下,该细胞应具有显著的分裂能力(根据病毒,复制过程可能导致细胞死亡,因此该细胞不能再用于进一步培养)。
这些细胞的使用类似于使用土壤种植蔬菜。这是必不可少的,但到了收获和食用的时候,我们会彻底清洗蔬菜以去除杂质。
在这一点上,你可能会想,为什么我们不能简单地使用动物细胞来规避使用胎儿细胞的明显道德困境。在许多情况下,我们可以——但会出现一些问题。许多病毒对它们感染的细胞类型非常具有特异性。细胞必须既易感(意味着它表达病毒能够进入内部所需的受体)又允许(意味着它必须能够支持病毒代谢复制),任何病毒才能在其内部繁殖。不幸的是,这意味着一些病毒不会在非人类细胞中有效生长,即使你让它们变得敏感,弄清楚如何在易感的基础上让它们变得宽松是具有挑战性和昂贵的。转向使用胎儿细胞培养病毒还有一个重要的历史原因:SV40。SV40(猿猴病毒 40)是一种存在于猴肾细胞中的病毒,已被用于培养病毒;在 1950 年代,在这些猴子肾细胞中培养 4 型和 7 型腺病毒用于疫苗生产,后来表明疫苗也受到了 SV40 的污染。这些细胞还用于生产灭活脊髓灰质炎疫苗的病毒。众所周知,SV40 能够在啮齿动物中致癌,因此在发现它存在于人类疫苗中时,问题就变成了该病毒是否也可能导致人类癌症。普洛特金的疫苗很好地总结了证据(强调是我的):
尽管人们担心 SV40 对疫苗接种者及其后代的潜在致癌性,但长期随访研究并不支持这种关联。 572,573 1997 年在美国国立卫生研究院召开的一次会议重新审查了现有证据,并得出结论:“在暴露于 SV40 污染的脊髓灰质炎疫苗的人类中,没有发生可测量的肿瘤疾病增加。574 随后,一份报告评估了可能暴露于 SV40 的出生队列的癌症风险,并得出结论,这些队列的癌症结果风险没有显着增加。575 然而,SV40 暴露是否会增加癌症风险的问题仍在争论。 576,577 免疫安全委员会(在医学研究所的主持下)在 2002 年的一项审查得出结论,由于流行病学研究存在足够的缺陷,因此证据不足以得出 SV40 污染的脊髓灰质炎疫苗是否会导致癌症的结论。 578 随后的几项队列和病例对照研究使用更科学严谨的方法未能支持 SV40 与癌症之间的关系。 579、580、581、582 目前用于 OPV 生产的细胞系来自在无 SV40 的菌落中饲养的猴子或来自特征明确的连续细胞系(Vero 细胞)。此外,必须对 OPV 进行已知病毒筛查;因此,SV40 不存在于当前批次的 OPV 疫苗中。
换句话说,值得庆幸的是,对证据的审查并未表明脊髓灰质炎疫苗中的 SV40 导致癌症发病率上升,或者在我们的流行病学方法检测此类信号的范围内,该病毒可能对人类有害。这个问题有许多人为的发现确实表明了这种联系,但这些可以通过试剂的已知问题来解释,例如,用于识别患者肿瘤中 SV40 的抗体可以与已知能够感染人类并可能导致癌症的相关病毒发生交叉反应。IARC(您可以免费下载 PDF)为任何感兴趣的人提供了关于 SV40 的详细专著。然而,这引发了关于哪些细胞应该用于疫苗生产的重要问题。
在其自然历史中,细胞将不可避免地暴露在病毒中,当您尝试大量制造病毒时,例如用于疫苗,避免污染物至关重要——尽管我们无法证明 SV40 污染物的存在对人类健康有害,但疫苗中可能存在替代污染物并对人类健康有害。因此,解决方案是:使用没有机会感染病毒的细胞——胎儿细胞。
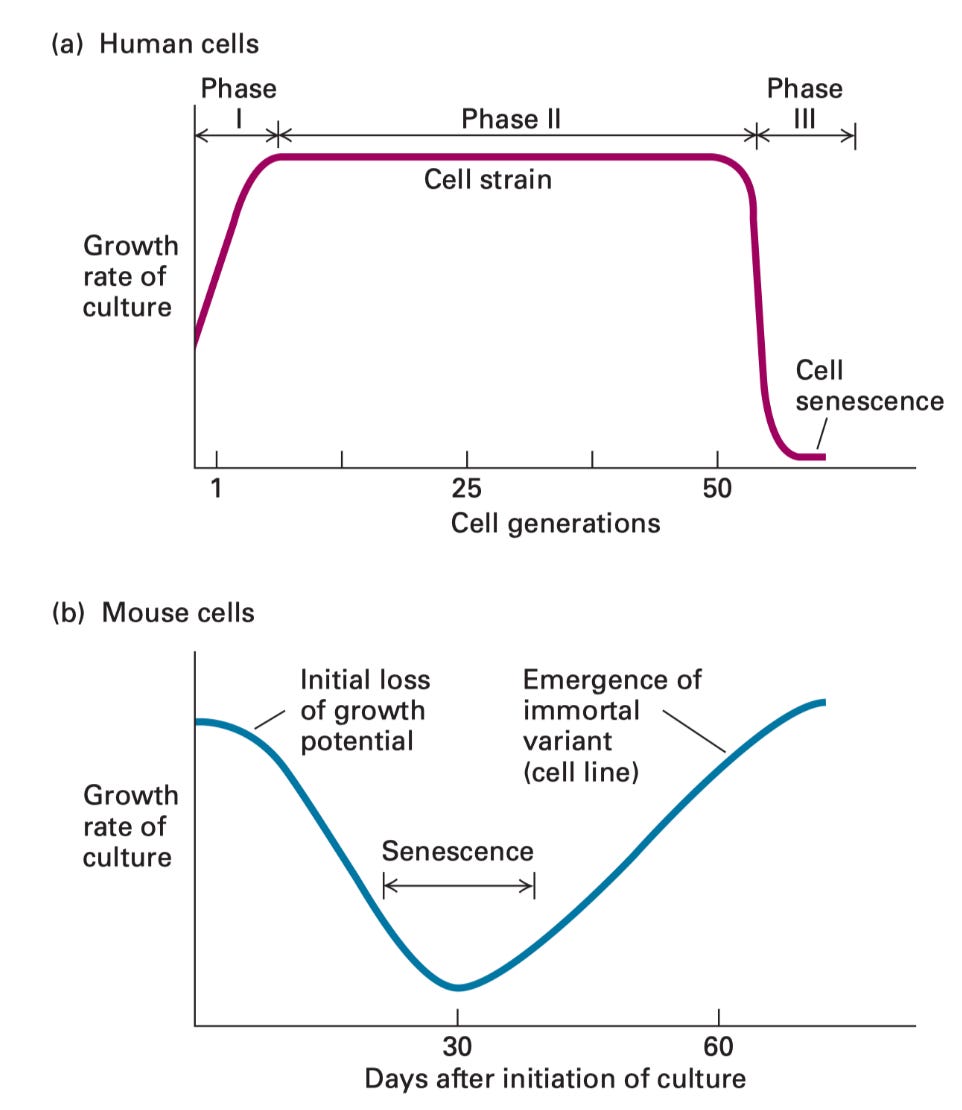
不过,首先需要简短地绕道来澄清一些重要的术语。在讨论这个话题时,人们通常会使用“细胞系”一词来表示用于制造这些疫苗的特定细胞类型,但这是不正确的。从人体组织中分离的细胞会经历可预测的变化。首先,它们中的很大一部分死亡,但剩余的细胞可以被收获和稀释,并在培养皿中重复重新铺板约 50 次细胞分裂,然后它们达到称为细胞衰老的阶段,在该阶段它们停止分裂(达到此阶段所需的分裂次数称为 Hayflick 极限)。稳态生长期(图 4.1a 中的阶段 II)是一种细胞品系。另一方面,当这种情况发生时,一些细胞可能会获得突变,使它们永生且无法衰老。这被称为细胞系。癌细胞表现出这种特性,您可能听说过 HeLa 细胞,这些细胞是在未经 Henrietta Lacks 同意的情况下以不道德的方式从 Henrietta Lacks 那里获得的,用于在生物学和医学方面取得重大进步。细胞株(而不是细胞系)用于制造疫苗,Hayflick 的努力确保了这些细胞株可以持续几十年来生产疫苗。
对于儿童计划的疫苗,使用了两种胎儿细胞株:MRC-5 和 WI-38,用于制造水痘、风疹、甲型肝炎疫苗和一种狂犬病疫苗;均来自 1960 年代欧洲妇女的选择性堕胎。在它们的使用历史中,从未发现过病毒污染物的证据。我认为在这里需要注意的是,这些不是 为了获得用于疫苗制造的病毒生产材料而进行的堕胎:它们无论如何都会发生,但这样一来,至少胎儿组织可以用来积极改变人类健康。正如 Hayflick 和 Olshansky 所解释的那样:
结果表明,使用 WI-38 相关疫苗预防或治疗的脊髓灰质炎、麻疹、腮腺炎、风疹、水痘、腺病毒、狂犬病和甲型肝炎病例总数在美国为 1.98 亿,全球为 45 亿(非洲为 7.2 亿,拉丁美洲和加勒比地区为 3.87 亿,亚洲为 27 亿,欧洲为 4.55 亿)。在美国,避免了大约45万例相同疾病的死亡总数,全球约有1030万例(非洲为160万例,拉丁美洲和加勒比地区为88.6万例,亚洲为620万例,欧洲为100万例)。
无论一个人对堕胎的个人看法如何,都不能忽视的是,无论一个人对这些细胞的采购有什么看法,它们都对公共卫生产生了巨大的积极影响。 多个宗教权威表示,尽管他们在道德上反对堕胎和普遍使用胎儿细胞,但他们并不认为疫苗接受者接受这些细胞内产生的疫苗在道德上是妥协的。 该主题的著名生物伦理学家通常不同意堕胎会使疫苗在道德上败坏。
每。C6 也是属于 Janssen 的与疫苗生产相关的细胞系(不是细胞株),Janssen 是一种来自 1985 年流产胎儿的视网膜细胞。生物医学研究中另一种非常常见的细胞系是 HEK.293 细胞系,它来自 1972 年流产的胎儿。这两种细胞是生产复制缺陷型腺病毒的理想选择,mRNA 疫苗在临床前在 HEK.293 细胞中进行了测试,但它们未用于疫苗的生产。复制缺陷型腺病毒对于载体疫苗的生产非常有用,并且由于它们无法复制(它们所需的必需基因缺失),因此甚至可以安全地给予免疫功能低下的人。细胞表达对反式病毒复制所必需的基因 (这意味着这些基因不是病毒基因组的一部分,而是由细胞表达),但最终产物缺乏制造它们的指令,产生了复制缺陷的腺病毒载体。
作为 质量控制过程的一部分,细胞中残留的 DNA 都会被称为核酸酶的酶破坏,抗原被纯化出来,以排除残留的痕量培养基以外的任何东西。
选择
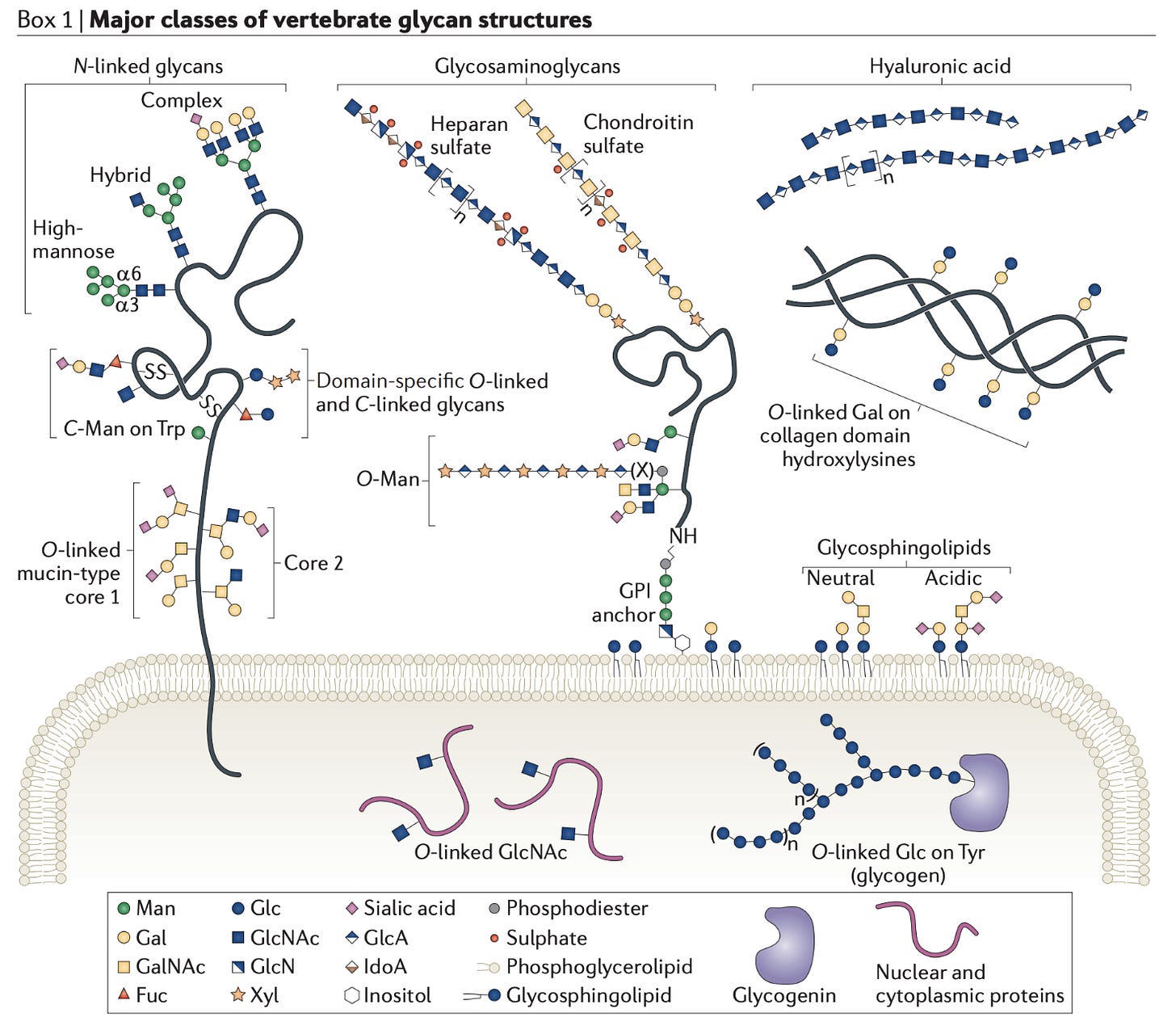
mRNA 疫苗的惊人之处之一是它们可以完全不使用细胞制造1。你只需要一个你想要的 RNA 的 DNA 序列、一个 RNA 聚合酶和一堆核糖核苷酸,你自己就有一个疫苗生产容器(当然,这并不那么简单,因为必须编辑 RNA 以控制它产生的免疫反应有多强,并且必须包装成非常特殊配方的脂质纳米颗粒)。这里的问题主要是双重的。首先,相对于其他类型的 mRNA 疫苗,mRNA 疫苗的制造成本更高,并且更难储存,这限制了它们在高收入国家以外的使用可行性。mRNA 疫苗在处理非病毒病原体时也可能遇到困难。注定要在细胞外分泌的蛋白质在称为糖基化的过程中被称为聚糖的糖树修饰。感染人类的病毒在人类细胞中执行此作,因此 mRNA 疫苗中病毒蛋白的糖基化在重现实际感染中发生的情况方面做得非常出色。然而,对于寄生虫或细菌等物质,它们糖基化的方式可能与人类细胞可能做的事情截然不同,这可能是免疫系统识别抗原的一个严重问题。
近年来,另一种更具吸引力的选择是植物性疫苗。这是疫苗抗原的制造地,字面意思是在工厂内。这有很多好处:
与细菌、酵母、昆虫或哺乳动物系统相比,植物表达系统在速度、成本、可扩展性和安全性方面具有几个内在优势[5,6]。此外,植物具有执行翻译后变化的能力,这些变化在蛋白质折叠、运输、稳定性和生物活性中很重要 [7, 8]。已经开发了植物源性抗体 (PDAb) 来防止不同的病原体,包括病毒、细菌和真菌 [9, 10]。
在某些情况下,甚至可以进一步制造可食用疫苗,这对于中低收入国家 (LMIC) 来说是一个绝佳的解决方案,其中植物实际上含有疫苗抗原,人们食用植物,这可能代表了对感染消化道的病原体(如脊髓灰质炎病毒或轮状病毒)获得免疫力的可行途径。也有人尝试制造植物性流感疫苗,这些疫苗可能很快就会取得成果。但是,这种方法也有局限性。一方面,疫苗抗原基于人类或动物病原体,因此找到一种能够可靠地产生它们的植物根本不是一项简单的任务。此外,组织选择也很重要:例如,叶子的蛋白酶表达量很高,并且总体蛋白质的含量通常很差,这意味着它们可能会破坏它们产生的抗原。实现一致的剂量也可能是一个挑战(事实上,这个问题臭名昭著地延伸到草药)。还有人担心如何确保患者对抗原产生良好的免疫反应,而不是学会耐受它们。此外,人们更普遍地担心使用非人类细胞也会如何影响糖基化(蛋白质在分泌前用糖装饰,作为其质量控制措施的一部分,但这样做的方式非常具体),因为这可能会影响免疫系统识别和响应它们的能力——尤其是植物不会产生唾液酸残基,而唾液酸残基在哺乳动物中非常常见,对免疫至关重要识别,并且它们会产生人类根本不产生的糖,这可能会引发免疫系统的反应。Medicago 生产了一种植物性 COVID-19 疫苗。
还有基于昆虫细胞载体的方法。这实际上就是 Novavax 所做的。这里的潜在缺点与使用植物相似,特别是在糖基化方面。相对于人类,昆虫的蛋白质上的糖基化模式往往不那么复杂、修剪过,这对于免疫系统识别它们的能力可能有意义。然而,这也被认为是一个优势,因为这意味着更多的蛋白质暴露在免疫系统中。它们还表达一些糖类,如植物,这些糖类在人类中没有,因此会引发免疫反应。然而,最近的工作已经能够在昆虫细胞内产生更人源化的糖基化系统。
这并不是说这些替代方法不起作用(毕竟,脊髓灰质炎疫苗是用猴肾细胞制成的,在疫苗接种活动中取得了巨大成功),尤其是有可能产生人源化糖基化系统,事实上,我们拥有的大多数需要基于细胞的表达系统的药物都不使用人体细胞, 但是在处理免疫系统时,重要的是要尽可能精确(例如,考虑到 A 型和 B 型血仅一个乙酰基不同,但免疫系统对不匹配的血型会产生非常有效的反应),并且这些其他药物的设计目的通常不像疫苗那样以引起免疫系统的反应为目的(事实上,通常会小心尝试以防止这种情况发生)。目前,使用人类细胞的基于细胞株的方法仍然是标准,但随着技术的发展,这将值得进一步研究。我对使用替代技术没有任何疑虑,只要它被证明是 AS 或更安全有效的。
引用
- Lodish H、Berk A、Kaiser CA 等人。 分子细胞生物学。第 8 版 W.H. Freeman;2016 年。
- 查罗 RA。胎儿组织脱落。N Engl J Med. 2015 年;373(10):890-891。
- 亨丽埃塔·拉克斯(Henrietta Lacks):科学必须纠正历史错误。 自然。2020;585(7823):7。
- 奥尔尚斯基 SJ,海弗里克 L.WI-38 细胞株在挽救生命和降低发病率中的作用。AIMS 公共卫生。2017 年;4(2):127-138。
- 病毒学讲座 2021 #2 – 传染周期。发布时间:2021 年 1 月 15 日。2021 年 3 月 8 日访问。
- 猿猴病毒 40。Who.int. 2021 年 3 月 8 日访问。https://monographs.iarc.who.int/wp-content/uploads/2018/06/mono104-002.pdf
- 费城儿童医院。疫苗成分 – SV40。Chop.edu。2021 年 3 月 8 日访问。https://www.chop.edu/centers-programs/vaccine-education-center/vaccine-ingredients/sv40
- 疫苗开发中的人类细胞株。Historyofvaccines.org。2021 年 3 月 8 日访问。https://www.historyofvaccines.org/content/articles/human-cell-strains-vaccine-development
- mRNA 和疫苗生产的未来。Path.org。2021 年 3 月 9 日访问。https://www.path.org/articles/mrna-and-future-vaccine-manufacturing/
- Dubey KK, Luke GA, Knox C, et al. 植物中的疫苗和抗体生产:发展和计算工具。 Brief Funct Genomics.2018;17(5):295-307。
- Ward BJ, Makarkov A, Séguin A, et al. 植物来源的四价病毒样颗粒流感疫苗在成人 (18-64 岁) 和老年人 (≥65 岁) 中的疗效、免疫原性和安全性:两项多中心、随机 3 期试验。 柳叶刀。2020;396(10261):1491-1503。
- Laere E, Ling APK, Wong YP, Koh RY, Mohd Lila MA, Hussein S. 植物性疫苗:生产和挑战。 J 机器人。2016;2016:1-11。
- 保罗 MG, 奥弗斯特 C, 科尔迪克 MH, 斯豪滕 G, 梅塔利 M, Uytdehaag F.人类细胞系 PER.C6 为流感疫苗的生产提供了一种新的生产系统。疫苗。2001 年;19(17-19):2716-2721。
- 植物如何生产 COVID-19 疫苗。Nature.com。2021 年 3 月 9 日访问。https://www.nature.com/articles/d42473-020-00253-2
- Takeyama N, Kiyono H, Yuki Y. 动物和人类植物疫苗:技术和临床试验的最新进展。 Ther Adv 疫苗。2015;3(5-6):139-154。
- HEK293 细胞系。Hek293.com。发布时间:2014 年 7 月 25 日。2021 年 3 月 9 日访问。https://www.hek293.com/
- 瓦德曼 M.一家小型、长势的美国公司最终会生产出最好的冠状病毒疫苗吗?科学。2020 年在线发布。doi:10.1126/science.abf5474
- 脊椎动物蛋白糖基化:多样性、合成和功能。 Nat Rev Mol 细胞生物学。2012;13(7):448-462。
- Palmberger D、Wilson IBH、Berger I、Grabherr R、Rendic D. SweetBac:一种在昆虫细胞中生产哺乳动物化糖蛋白的新方法。 公共科学图书馆一号。2012;7(4):e34226。
- Genzel Y. 设计用于病毒疫苗生产的细胞系:我们的立场如何? 生物技术 J.2015;10(5):728-740。
- Ozdilek A, Paschall AV, Dookwah M, Tiemeyer M, Avci FY.核酸疫苗中的宿主蛋白糖基化是非病毒病原体疫苗设计的潜在障碍。美国国家科学院院刊 2020;117(3):1280-1282。
Hits: 40

