A ‘functional cure’ for HIV may be in reach, early trials suggest
感染艾滋病毒的人必须终生服用抗逆转录病毒药物。但使用基因工程抗体进行的前景良好的试验表明,“功能性治愈”或许触手可及。
早期试验表明,新的基于抗体的疗法已使一些艾滋病患者实现了长期缓解。(图片来源:KATERYNA KON via Shutterstock)
全球约有4000万人感染艾滋病毒(HIV)。尽管治疗方面的进展意味着这种感染已不再像过去那样等同于死刑,但研究人员始终未能找到治愈方法。相反,艾滋病病毒阳性患者余生都必须服用抗逆转录病毒药物组合。
但在2025年,研究人员报告了一项突破性进展,这表明艾滋病病毒的“功能性”治愈——一种无需持续治疗就能长期控制艾滋病病毒的方法——或许确实是可能的。在两项使用工程抗体输注的独立试验中,一些参与者在干预结束后很长一段时间内,即使不服用抗逆转录病毒药物,仍然保持健康。
在其中一项试验中——由南非夸祖鲁-纳塔尔大学和非洲健康研究所的病毒学家Thumbi Ndung’u领导的 FRESH试验——20名参与者中有4人在未服用抗逆转录病毒药物的情况下,病毒载量维持在检测不到的水平,中位时间为1.5年。另一项是在英国和丹麦开展的RIO试验,由伦敦帝国理工学院的临床医生兼艾滋病研究专家Sarah Fidler领导,34名HIV阳性参与者中有6人已维持病毒控制至少两年。
这些具有里程碑意义的概念验证试验表明,免疫系统可以被利用来对抗艾滋病病毒。研究人员目前正计划进行规模更大、更具代表性的试验,以探究是否可以对抗体进行优化,使其适用于更多人群。
“我确实认为这种治疗方法有机会真正改变现状,”菲德勒说,“因为它们是长效药物——即使在体内代谢完之后,药效仍能持续。“到目前为止,我们还没见过有什么药物能达到这样的效果。”
感染艾滋病毒的人如果服用抗逆转录病毒药物,可以过上长久而健康的生活。但他们的寿命通常仍然比没有感染该病毒的人短。而且对许多人来说,每日服用的药片,甚至是较新的双月注射剂,都带来了重大的经济、实际和社会挑战,包括污名化。“在过去大约15到20年里,人们确实一直在努力探索‘我们如何能做得更好?’”菲德勒说。

她说,这个梦想就是“人们所说的治愈艾滋病病毒,或者让艾滋病病毒得到缓解”。但这带来了巨大的挑战,因为艾滋病病毒是伪装高手。感染后,这种病毒进化速度极快,以至于人体无法迅速产生新的抗体来识别并中和它。
而且有些艾滋病病毒会以不活跃的状态潜伏在细胞中,躲避免疫系统的识别。这些逃避免疫的策略让一系列治愈尝试都以失败告终。除了少数几例特殊的干细胞移植手术外,所有干预手段都未能实现彻底治愈——即把艾滋病病毒从体内完全清除。
功能性治愈将是次佳选择。而这正是一种罕见现象带来希望的地方:一些长期感染HIV的人最终确实会产生能够中和病毒的抗体,尽管为时已晚,无法完全清除病毒。这些强效抗体针对HIV病毒外膜蛋白中关键且极少发生变化的部分;病毒正是利用这些蛋白来感染细胞。这些能够识别多种病毒株的抗体被称为广谱中和抗体。
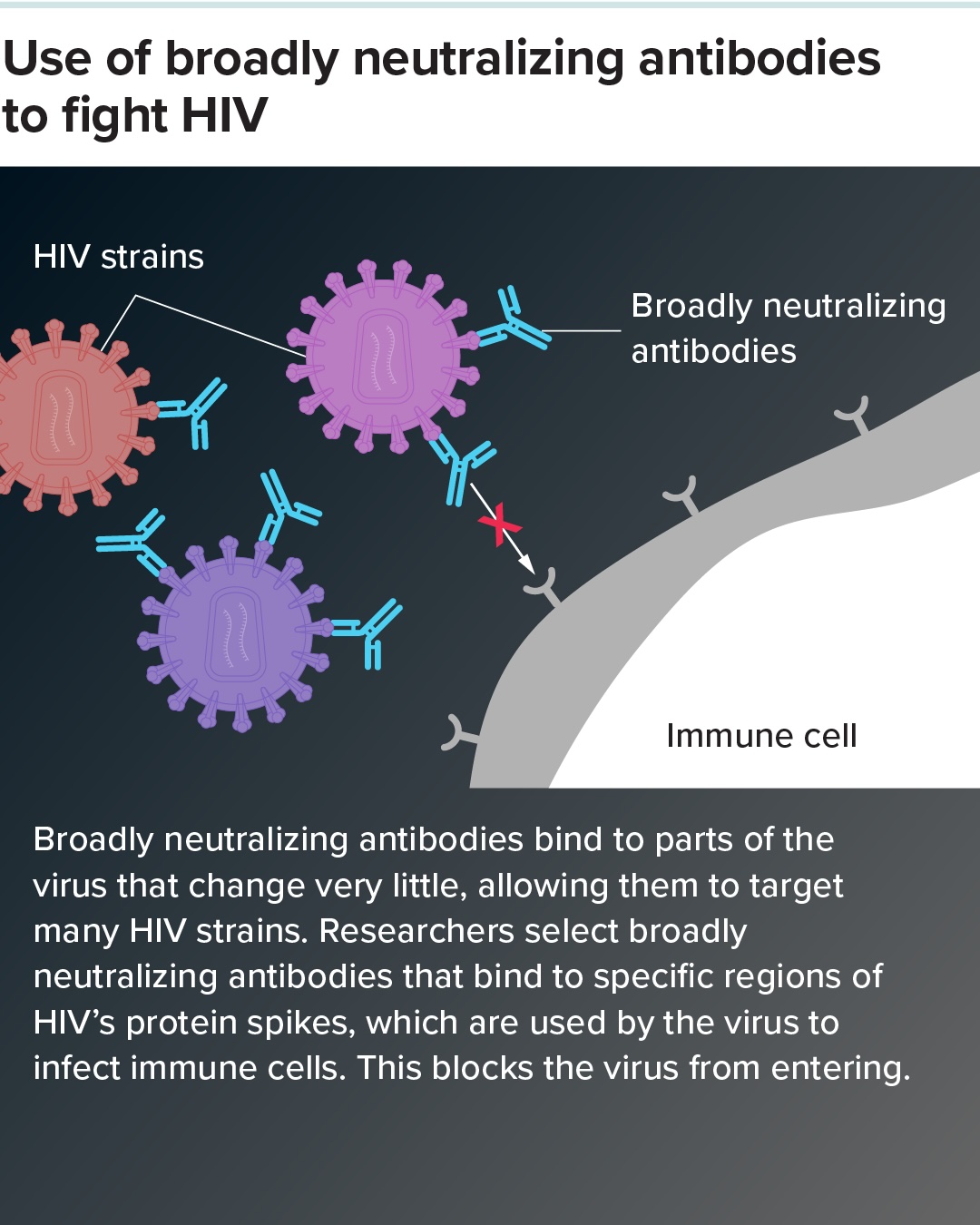
科学家们目前正竞相寻找最有效的广谱中和抗体,并将其改造为功能性疗法。FRESH和RIO可以说是迄今为止最具前景的尝试。
在FRESH试验中,科学家们选择了两种抗体,联合使用时可能对被称为HIV-1 C亚型的艾滋病毒株有效,这种毒株在撒哈拉以南非洲占主导地位。该试验招募了高流行社区的年轻女性,作为更广泛的社会赋权计划的一部分。几年前,该计划已让这些女性在感染后三天内开始接受艾滋病毒治疗。
与此同时,RIO试验选择了两种经过充分研究且被证明具有广泛疗效的抗体。其参与者主要是40岁左右的白人男性,他们在感染后不久就开始服用抗逆转录病毒药物。大多数人感染的是HIV-1 B亚型,这种亚型在欧洲更为常见。
研究人员通过将抗体配对,旨在降低HIV产生耐药性的可能性——这是抗体治疗中常见的挑战,因为病毒需要发生多种突变才能逃避这两种抗体的作用。
两项试验的参与者都接受了抗体注射,这些抗体经过改造后可在体内持续约六个月。随后,他们暂停了抗病毒药物治疗。研究人员希望这些抗体能与免疫系统协同作用,杀死活跃的HIV病毒颗粒,从而控制病毒。如果这种效果无法持续,那么在抗体被分解后,HIV病毒水平就会上升,参与者将重新开始抗逆转录病毒治疗。
然而,令人兴奋的是,两项试验的结果都表明,在一些人身上,这些干预措施引发了持续的、独立的免疫反应,研究人员将这种反应比作疫苗的效果。
在RIO试验中,34名接受广谱中和抗体治疗的患者中,有22人在20周时未出现病毒反弹。此时,他们接受了另一剂抗体注射。超过96周后——远远在抗体消失之后——仍有6人的病毒水平低到足以停用抗病毒药物。
该研究中额外纳入的34名参与者作为对照组,仅接受了生理盐水输注,其中大多数人不得不在4至6周内重新开始治疗;除3人外,其余所有人都在20周内恢复了治疗。
在FRESH试验中也观察到了类似的模式(不过,由于该试验主要是一项安全性研究,因此没有纳入对照组参与者)。20名参与者中有6名在抗体输注后48周内保持了病毒抑制,其中4名在停药一年多后仍维持这一状态。干预两年半后,有1名参与者仍未接受抗逆转录病毒药物治疗。另外两名参与者也维持了对病毒的控制,但最终因个人和后勤原因选择重新开始治疗。
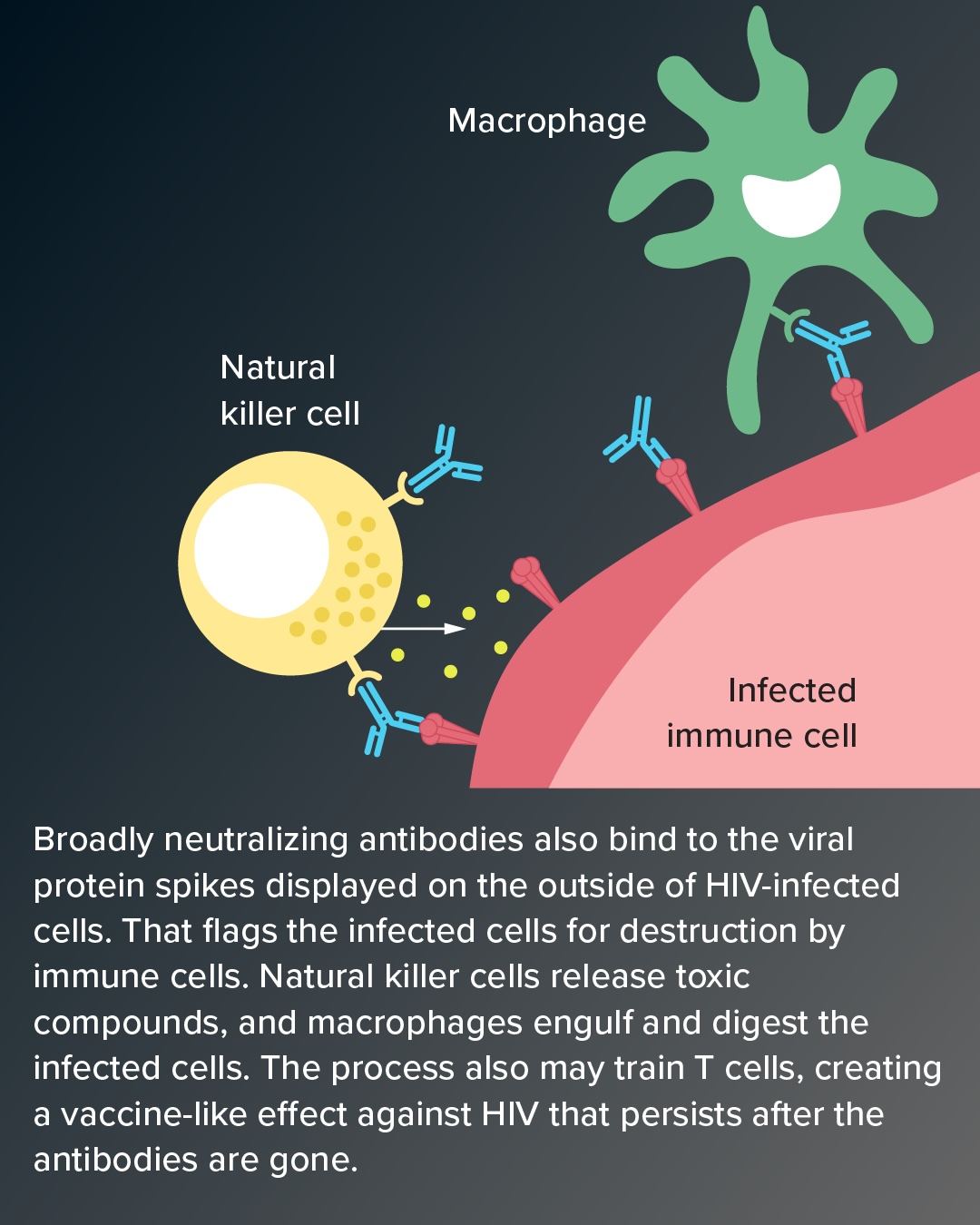
目前尚不清楚该病毒何时可能反弹,因此研究人员在将处于缓解期的参与者称为功能性治愈时持谨慎态度。然而,这些抗体显然似乎能促使免疫系统对抗该病毒。它们附着在受感染细胞上,向免疫细胞发出信号,让其前来杀灭病毒。
重要的是,研究人员认为,这种针对抗体的免疫反应可能还会刺激一种名为CD8+ T细胞的免疫细胞,随后这些细胞会追踪并消灭受HIV感染的细胞。这可能会形成一种“免疫记忆”,即便在抗体消失后,也能帮助身体控制HIV。
这种反应类似于在一小群(不到1%)艾滋病病毒携带者身上观察到的免疫控制现象,这些人被称为“精英控制者”。这些人无需抗逆转录病毒药物的帮助就能抑制艾滋病病毒,将其主要限制在小型病毒库中。约翰·霍普金斯医学院的传染病专家乔尔·布兰克森参与撰写了《2024年免疫学年度评论》中一篇关于天然艾滋病病毒控制者的文章,他表示,这些试验帮助一些参与者实现了类似的效果,这很令人兴奋。“这可能会教会我们如何更有效地做到这一点,而且我们或许能让更高比例的人进入缓解期。”
科学家们确定的一点是,如果人们在感染后尽快开始抗逆转录病毒治疗,实现持续控制的可能性会更高,因为此时他们的免疫系统仍然完好,病毒库也较小。
但即使是在最初感染后很久才开始服用抗逆转录病毒药物的人群中,也可能出现治疗后的控制,这类人群被称为慢性感染患者。“只是这种情况发生的频率较低,”布兰克森说,“因此,这些研究中涉及的策略也有可能适用于慢性感染患者。”
RIO试验中一个特别令人期待的发现是,这些抗体还会对潜伏在某些细胞中的休眠HIV产生影响。这些病毒库是人们停止治疗后病毒反弹的原因,而人们原本认为抗体不会对它们产生作用。研究人员推测,被抗体激活的T细胞能够识别并杀死那些表面仅显示微量HIV的潜伏感染细胞。
与此同时,FRESH干预措施通过加入另一种名为vesatolimod的药物,更直接地针对顽固的HIV病毒库。这种药物旨在刺激免疫细胞对HIV威胁做出反应,并有望“激活”潜伏的HIV颗粒,使其不再隐藏。一旦实现这一点,免疫系统在抗体的帮助下就能识别并杀死它们。
恩东古说,FRESH的研究结果令人兴奋,“因为这在某种程度上可能表明这种疗法是有效的。但显然,由于这是一项小型研究,很难得出非常确凿的结论。”他的团队仍在对数据进行研究。
本文最初发表于《可知杂志》,这是一本致力于让所有人都能获取科学知识的非营利性出版物。订阅《可知杂志》的新闻通讯。
安德里亚·蒂格尔是一位科学作家、编辑兼摄影师,现居南非开普敦。
Hits: 87
相关文章:
- 一种预防艾滋病毒的“突破性”药物,一次“史无前例”的推广
- HIV疫苗在确认中和抗体方面向前迈进了一步
- 促进HIV疫苗研究:研究为验证后续步骤提供了全面的平台
- 试验数据显示,一年两次的疫苗注射成功地预防了女性感染艾滋病病毒
- 艾滋病毒:我们离疫苗或者治愈还有多远?
- 艾滋病治疗和预防的进展
- 突破性的囊性纤维化药物可延长寿命数十年,其开发商获得 250,000 美元的“美国诺贝尔奖”
- 联合国大会第79届会议上的免疫联盟:兑现更健康未来的承诺
- 双歧杆菌支持婴儿疫苗的最佳反应
- 情绪和疫苗反应之间的惊人联系
- 90 亿美元、5 亿儿童、2500 亿美元的投资回报率:为什么全球疫苗免疫联盟布鲁塞尔峰会很重要
- 全球疫苗免疫联盟:25 年,25 个瞬间
- 这些是使您有资格接种更新的 Covid-19 疫苗的条件
- 疾病预防控制中心报告显示,儿童自闭症诊断率处于历史最高水平
- ACIP 完成 9 月会议,就 COVID-19 疫苗进行投票
Powered by YARPP.
