Contents
- 1 全球疫苗接种情况
- 1.0.1 摘要
- 1.0.2 1不是每个应该接种疫苗的孩子都接种了疫苗
- 1.0.3 1.1疫苗全球覆盖率
- 1.0.4 1.2繁荣和疫苗接种覆盖率
- 1.0.5 2疫苗拯救生命
- 1.0.6 2.1疫苗如何工作&群体免疫
- 1.0.7 3疫苗接种的进展
- 1.0.8 3.1天花和疫苗接种的起源
- 1.0.9 3.2疫苗创新
- 1.0.10 3.3美国疫苗可预防疾病的进展
- 1.0.11 3.4麻疹疫苗的发展和美国麻疹的历史
- 1.0.12 3.5疫苗可预防疾病的全球下降
- 1.0.13 4.前进的道路
- 1.0.14 5.最致命的疾病
- 1.0.15 6.通过接种疫苗根除疾病
- 1.0.16 6.1在根除脊髓灰质炎的道路上
- 1.0.17 6.2天花的根除
- 1.0.18 7.公众的支持和怀疑
- 1.0.19 7.1人们不知道我们在全球疫苗接种方面做得有多好
- 1.0.20 7.2人们对疫苗接种覆盖率的看法已经过时了30多年
- 1.0.21 7.3全世界有多少人支持接种疫苗?
- 1.0.22 7.4世界上大多数人认为疫苗对儿童来说很重要
- 1.0.23 7.5世界上大多数人认为疫苗是安全的,但在一些国家不信任度很高
- 1.0.24 7.6全球只有5%的受访者不同意疫苗有效,但在一些国家持怀疑态度的人要多得多
- 1.0.25 7.7在一些国家,许多人对接种疫苗犹豫不决
- 1.0.26 7.8疫苗怀疑论会影响免疫覆盖率吗?
- 1.0.27 8.疫苗政策
- 1.0.28 8.1什么决定了疫苗接种是否是强制性的?
- 1.0.29 8.2强制接种疫苗有效吗?
- 1.0.30 8.3疫苗供应
- 1.0.31 8.4疫苗的成本
- 1.0.32 8.5为什么疫苗接种时间表不同?
- 1.0.33 8.6哪些国家有强制性儿童疫苗接种政策?
- 1.0.34 8.7世界各地的儿童疫苗接种政策有何不同?
- 1.0.35 8.8强制疫苗接种政策因地区而异?
- 1.0.36 8.9是什么推动了强制性疫苗接种的引入?
- 1.0.37 9.覆盖面、影响和潜力
- 1.0.38 9.1通过接种疫苗可以预防的疾病
- 1.0.39 9.2白喉、破伤风和百日咳疫苗
- 1.0.40 9.3麻疹疫苗
- 1.0.41 9.3.1第二剂麻疹疫苗提供更大的保护
- 1.0.42 9.3.2全球麻疹发病率下降
- 1.0.43 9.4轮状病毒疫苗
- 1.0.44 9.4.1轮状病毒疫苗可以拯救更多儿童的生命
- 1.0.45 9.4.2免疫接种率仍然太低
- 1.0.46 9.4.3疫苗效力因地区而异
- 1.0.47 9.5肺炎球菌疫苗
- 1.0.48 9.5.1肺炎球菌疫苗的覆盖率仍然很低
- 1.0.49 9.5.2肺炎球菌疫苗是如何发挥作用的?
- 1.0.50 9.5.3肺炎球菌疫苗的效果如何?
- 1.0.51 9.5.4肺炎球菌疫苗可以避免多少儿童死亡?
- 1.0.52 9.5.5我们能做些什么来提高肺炎球菌疫苗的覆盖率和有效性?
- 1.0.53 9.6 乙型肝炎疫苗
- 1.0.54 9.7 b型流感嗜血杆菌疫苗
- 1.0.55 9.8脊髓灰质炎疫苗
- 1.0.56 9.9结核病疫苗(卡介苗)
- 1.0.57 9.10黄热病疫苗
- 1.0.58 10.定义和测量
- 1.0.59 数据源
- 1.1 摘要
- 1.2 1不是每个应该接种疫苗的孩子都接种了疫苗
- 1.3 2疫苗拯救生命
- 1.4 4.前进的道路
- 1.5 5.最致命的疾病
- 1.6 6.通过接种疫苗根除疾病
- 1.7 7.公众的支持和怀疑
- 1.8 8.疫苗政策
- 1.9 水痘的例子
- 1.10 9.覆盖面、影响和潜力
- 1.11 10.定义和测量
- 1.12 11.国家和国家以下各级的覆盖面
- 1.13 数据源
- 1.14 World Health Organization – Immunization surveillance, assessment and monitoring
- 1.15 UNICEF
- 2 Endnotes
- 3 Cite this work
全球疫苗接种情况
摘要
1不是每个应该接种疫苗的孩子都接种了疫苗
1.1疫苗全球覆盖率
1.2繁荣和疫苗接种覆盖率
2疫苗拯救生命
2.1疫苗如何工作&群体免疫
3疫苗接种的进展
3.1天花和疫苗接种的起源
3.2疫苗创新
3.3美国疫苗可预防疾病的进展
3.4麻疹疫苗的发展和美国麻疹的历史
3.5疫苗可预防疾病的全球下降
4.前进的道路
5.最致命的疾病
6.通过接种疫苗根除疾病
6.1在根除脊髓灰质炎的道路上
6.2天花的根除
7.公众的支持和怀疑
7.1人们不知道我们在全球疫苗接种方面做得有多好
7.2人们对疫苗接种覆盖率的看法已经过时了30多年
7.3全世界有多少人支持接种疫苗?
7.4世界上大多数人认为疫苗对儿童来说很重要
7.5世界上大多数人认为疫苗是安全的,但在一些国家不信任度很高
7.6全球只有5%的受访者不同意疫苗有效,但在一些国家持怀疑态度的人要多得多
7.7在一些国家,许多人对接种疫苗犹豫不决
7.8疫苗怀疑论会影响免疫覆盖率吗?
8.疫苗政策
8.1什么决定了疫苗接种是否是强制性的?
8.2强制接种疫苗有效吗?
8.3疫苗供应
8.4疫苗的成本
8.5为什么疫苗接种时间表不同?
8.6哪些国家有强制性儿童疫苗接种政策?
8.7世界各地的儿童疫苗接种政策有何不同?
8.8强制疫苗接种政策因地区而异?
8.9是什么推动了强制性疫苗接种的引入?
9.覆盖面、影响和潜力
9.1通过接种疫苗可以预防的疾病
9.2白喉、破伤风和百日咳疫苗
9.3麻疹疫苗
9.3.1第二剂麻疹疫苗提供更大的保护
9.3.2全球麻疹发病率下降
9.4轮状病毒疫苗
9.4.1轮状病毒疫苗可以拯救更多儿童的生命
9.4.2免疫接种率仍然太低
9.4.3疫苗效力因地区而异
9.5肺炎球菌疫苗
9.5.1肺炎球菌疫苗的覆盖率仍然很低
9.5.2肺炎球菌疫苗是如何发挥作用的?
9.5.3肺炎球菌疫苗的效果如何?
9.5.4肺炎球菌疫苗可以避免多少儿童死亡?
9.5.5我们能做些什么来提高肺炎球菌疫苗的覆盖率和有效性?
9.6 乙型肝炎疫苗
9.7 b型流感嗜血杆菌疫苗
9.8脊髓灰质炎疫苗
9.9结核病疫苗(卡介苗)
9.10黄热病疫苗
10.定义和测量
数据源
摘要
自从天花疫苗发明以来,疫苗大大降低了传染病在世界各地的流行。这篇研究文章解释了哪些疫苗可用以及它们在哪里,它们对全球健康的影响是什么,以及世界如何在疫苗的帮助下在对抗早期死亡和疾病方面取得更多进展。
过去几十年,疫苗接种覆盖率大幅提高,但2018年全球有1350万儿童没有接种疫苗
疫苗是预防疾病的最成功和最具成本效益的方法之一
疫苗覆盖面的扩大导致了疾病的减少
世界上90%的人认为给儿童接种疫苗很重要
许多疫苗的覆盖率仍然太低,我们正在错失拯救更多生命的机会
1不是每个应该接种疫苗的孩子都接种了疫苗
1.1疫苗全球覆盖率
这张图表显示了世卫组织推荐的一些最重要的疫苗在一岁儿童中的全球接种覆盖率。对于许多基本疫苗来说,覆盖率现在远远高于80%。然而,疫苗接种率仍然不够。
如果您单击“播放”按钮,您会看到大多数疫苗的覆盖范围随着时间的推移而大幅增加。
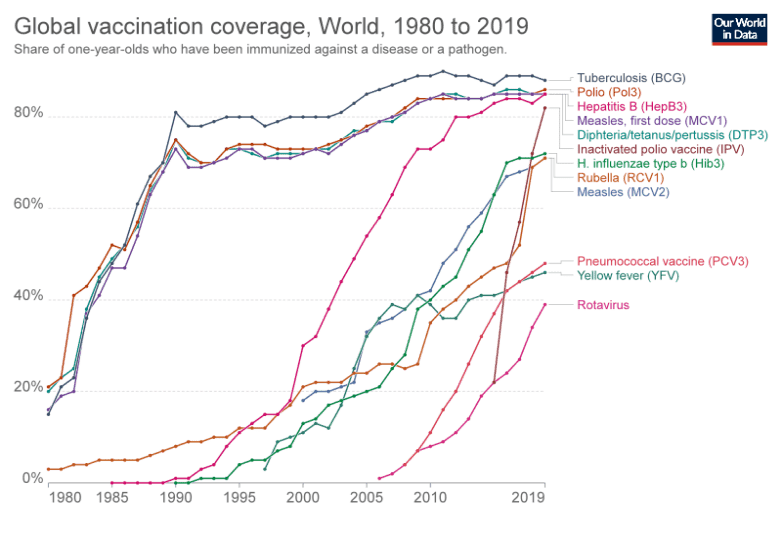
白喉、破伤风和百日咳疫苗经常被用作衡量全球疫苗接种覆盖率的关键指标,因为它是获得常规免疫服务的一个良好指标。2018年,第三剂百白破疫苗的覆盖率为86%。这意味着在1.35亿1岁以下儿童中,有1900多万没有接受全面免疫。第一剂百白破的覆盖率为90%,表明2018年1350万儿童没有接种疫苗。
2018年,全球只有35%的儿童接种了轮状病毒疫苗,该疫苗可以保护儿童免受腹泻疾病 — 主要原因之一儿童死亡率。同样,肺炎球菌疫苗可以保护儿童免受肺炎这是儿童死亡的主要原因,只有47%的一岁儿童接种了疫苗。
相关图表——数字接种疫苗的儿童. 这张图表显示了全球有多少一岁儿童接种了疫苗。
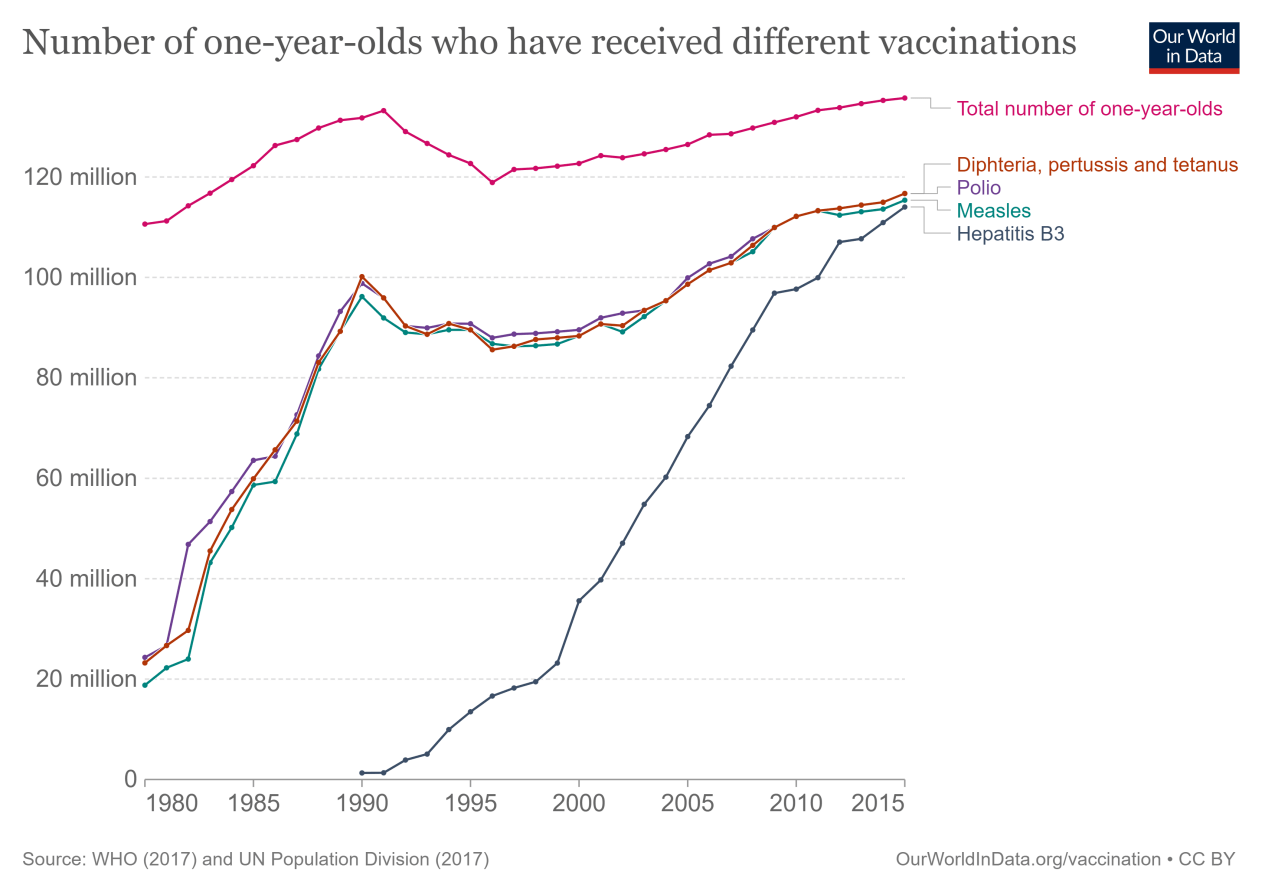
1.2繁荣和疫苗接种覆盖率
为什么世界上不是所有的儿童都接种疫苗?
这张图表显示,疫苗接种覆盖率低的是贫穷国家。白喉、百日咳和破伤风的疫苗覆盖率是一个国家免疫计划强度的良好标志,因为需要多次接种。所有富裕国家的疫苗接种覆盖率都超过90%。覆盖面较低的是中低收入国家——有些国家还不到50%。
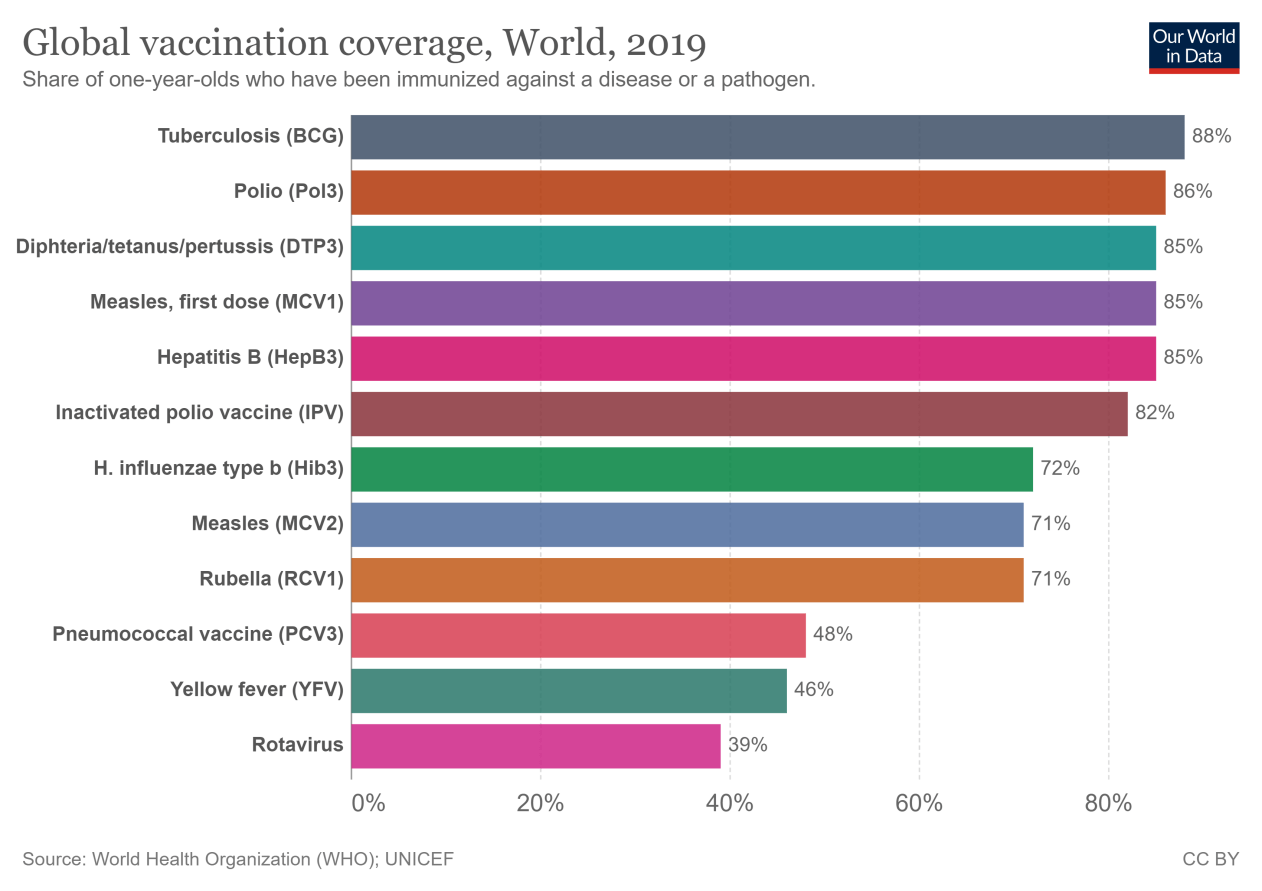
2019年全球疫苗接种覆盖率
但图表也显示,一些贫穷国家——如布隆迪、卢旺达和孟加拉国——实现了高覆盖率。同样,大部分人口生活在极端贫困中的国家通常(但不总是)免疫接种率较低,因为这张图表显示了。
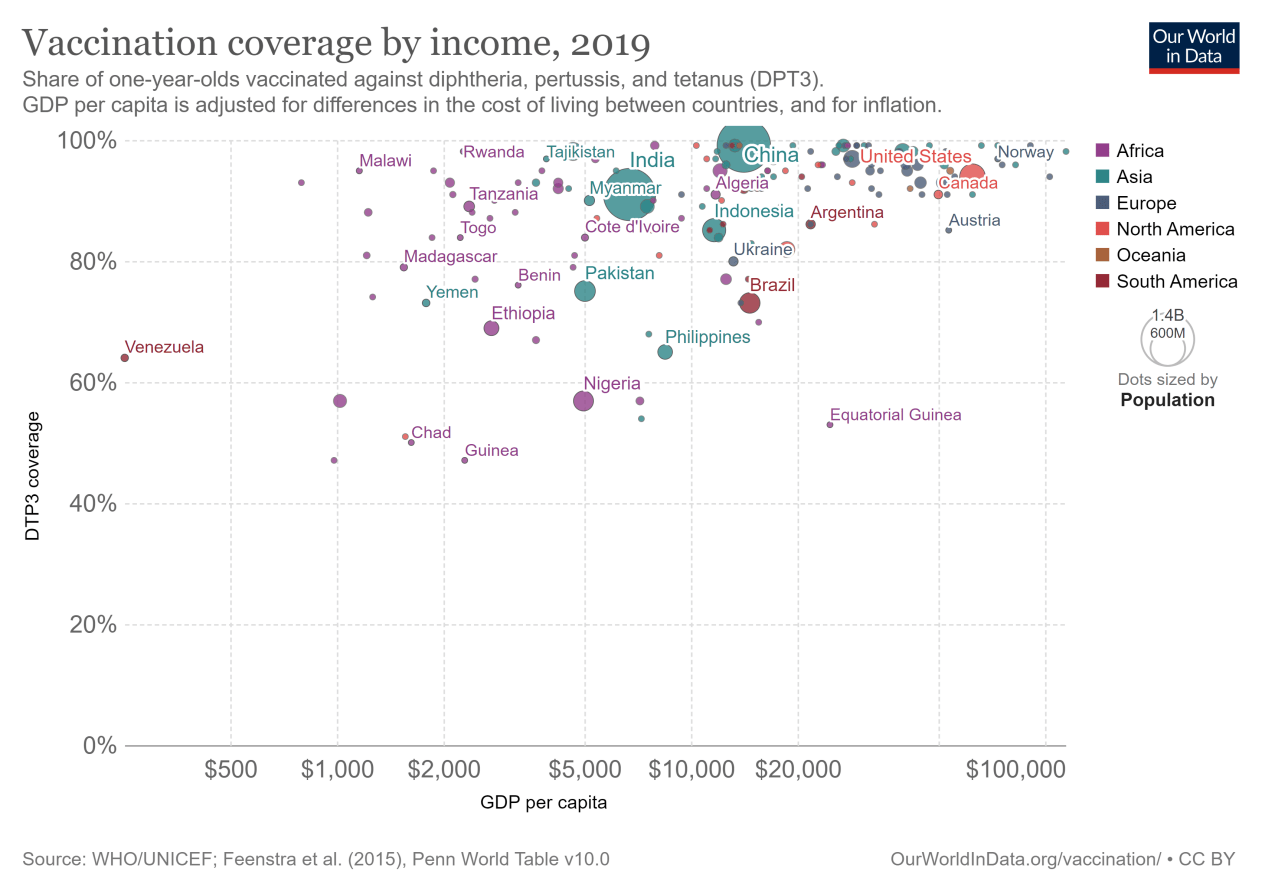
2019年按收入分列的疫苗接种覆盖率
2疫苗拯救生命
我们知道疫苗可以拯救生命。但是疫苗拯救了多少生命呢?
世界卫生组织(WHO)建议,疫苗接种每年可防止200-300万人死亡。然而,尽管我们确信疫苗拯救了数百万人的生命,但计算一个精确的数字是不可能的。此外,从重要的方面来看,引用的世卫组织数据是一个非常低的估计值。
在这个反事实的世界里,疫苗将永远不会被开发出来,这个世界将如此不同,以至于对疫苗的影响进行估计是不可能的。说明这一点的一个例子是考虑天花疫苗的影响:天花曾经是一种极其常见和致命的传染病,但由于接种了疫苗,这种疾病早在1977年就在全球范围内被根除了。如果科学家没有开发出疫苗,就不可能确切知道今天有多少人会死于天花。合理的估计是每年约有500万人丧生,这意味着在1980年至2018年期间,约有1.5亿至2亿人的生命得到拯救。这就清楚地说明了为什么很难估计每年挽救的生命数量,也说明了为什么世卫组织的估计值相当低。
2.1疫苗如何工作&群体免疫
疫苗发挥作用的基本机制很简单:疫苗通过引入使我们生病的病原体(如细菌或病毒)或其毒素或其表面蛋白之一的弱化或死亡形式,在个体中产生免疫力。疫苗诱导获得性免疫,这样当你的身体遇到真正的致病因子时,它就准备好发起防御。
高疫苗接种覆盖率会带来集体社会利益。对于大多数疾病,免疫接种的人口比例越大,人口中的每个人受到的保护就越好,因为疾病传播可以减少或停止。群体免疫是一种社区保护,是在高比例的人口接种疫苗时产生的,这样传染病就不太可能传播。
群体免疫提供了一个保护屏障,尤其是对那些不能接种疫苗。这些包括弱势群体,如太小而不能接种疫苗的婴儿或免疫受损的儿童,他们是疫苗接种率低的第一批潜在受害者。
当一个人对某种疾病有免疫力时,他们可以作为一道屏障,减缓或防止疾病传播给其他人。当一个群体中对某种疾病有免疫力的人数达到一定程度时,这种疾病就不再在该群体中持续存在,这种情况称为群体免疫阈值(HIT)。表格显示了几种疾病的HIT。麻疹和百日咳是高度传染性的空气传播疾病,大部分人需要接种疫苗以阻止传播。因此,这些疾病需要达到最高的HIT。例如,两剂麻疹疫苗可提供99%的保护,而在没有免疫的情况下,终生感染风险接近100%。
疫苗可预防疾病的群体免疫阈值
| 疾病 | 传播方式 | 基本传染数RO | 群体免疫阈值 |
|---|---|---|---|
| 麻疹 | 空运的 | 12–18 | 92–95% |
| 百日咳 | 空气飞沫 | 12–17 | 92–94% |
| 白喉 | 唾液 | 6–7 | 83–86% |
| 风疹 | 空气飞沫 | 6–7 | 83–86% |
| 天花 | 空气飞沫 | 5–7 | 80–86% |
| 脊髓灰质炎 | 粪-口途径 | 5–7 | 80–86% |
| 腮腺炎 | 空气飞沫 | 4–7 | 75–86% |
| 严重急性呼吸综合征 | 空气飞沫 | 2–5 | 50–80% |
| 埃博拉病毒 | 体液 | 1.5–2.5 | 33–60% |
| 流行性感冒 | 空气飞沫 | 1.5–1.8 | 33–44% |
3疫苗接种的进展
天花和疫苗接种的起源
疫苗创新
美国疫苗可预防疾病的进展
疫苗可预防疾病的全球下降
通过接种疫苗根除疾病
现在我们总共有至少28种人类疾病的有效疫苗让我们得以实现这一目标的突破是在18世纪晚期,天花疫苗是第一种疫苗。
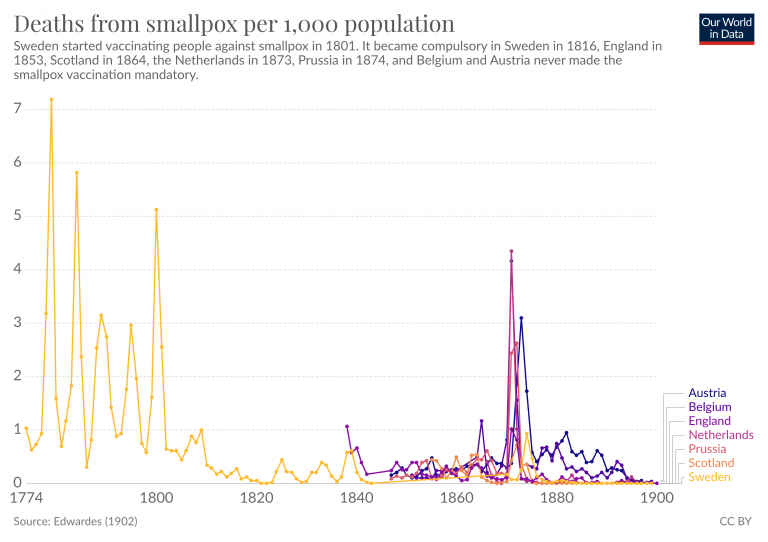
3.1天花和疫苗接种的起源
疫苗接种历史悠久。疫苗接种的早期形式被称为“变异”或更广泛地称为“接种”。在亚洲实行了很长时间,这是一种古老的深思熟虑的技术,天花干燥的天花痂被吹到鼻子里使人感染一种通常较轻的疾病。到18世纪,天花传播到了非洲、印度和奥斯曼帝国,接着是英国和美国,在这些地方,更常用的感染方法是在皮肤上穿孔。
变异确实有效,但也有很大的风险。那些患有天花的人可能感染更严重的天花而死亡,他们也可能将疾病传染给他人。
1796年,英国医生爱德华·詹纳展示了另一种接种方法,他用的是牛痘。牛痘是一种类似于天花的疾病,以前曾观察到感染牛痘可以预防天花。詹纳进行了一项实验,用牛痘病变的物质给他的园丁的八岁儿子詹姆斯·菲普斯接种疫苗。两个月后,詹纳让男孩接触天花病变物质,当菲普斯没有患上天花时,他得出结论,他已经免受这种疾病的侵害。詹纳称这一过程为“疫苗接种”,源于拉丁语“vacca ”,意为“母牛”,因为这种首次疫苗接种源于牛痘病毒。
继詹纳的发现成为通过接种疫苗控制疾病的第一次科学尝试之后,天花疫苗经历了多次迭代,出现了通过现代细胞培养技术生产的更新疫苗(通过细胞培养传递病毒使疫苗更安全)。到20世纪中叶,人们越来越相信天花可能是人类能够根除的第一种疾病。1967年,世卫组织发起了一项全球根除天花计划。一个国家超过80%的人口接受了大规模疫苗接种,但游牧民族或生活在政治不稳定地区的人带来了特殊的问题。在脚踏式注射器的发展过程中出现了许多创新“ped-o-jet”和分叉针头,使用起来既高效又经济。
为了覆盖大部分人群,流行病学家威廉·佛吉发展根除升级(E2)以控制10月期间的天花爆发(这是天花传播的季节性低谷,在此期间预防几个病例就可以阻止天花的连锁传播)。面临的其他障碍包括强迫一名印度宗教领袖接种疫苗,以说服他的追随者接种疫苗,在饱受战争蹂躏的尼日利亚就疫苗运输停火进行谈判,在爆发疫情的周围进行同心环接种疫苗,以及奖励报告天花病例的现金奖励。最后,1977年,最后一例自然感染天花的病例在索马里的阿里·毛乌·马阿林报告,1980年世卫组织宣布天花已经根除。我们涵盖了天花的历史,包括疫苗接种和根除,在我们的条目中有更详细的介绍天花.
3.2疫苗创新
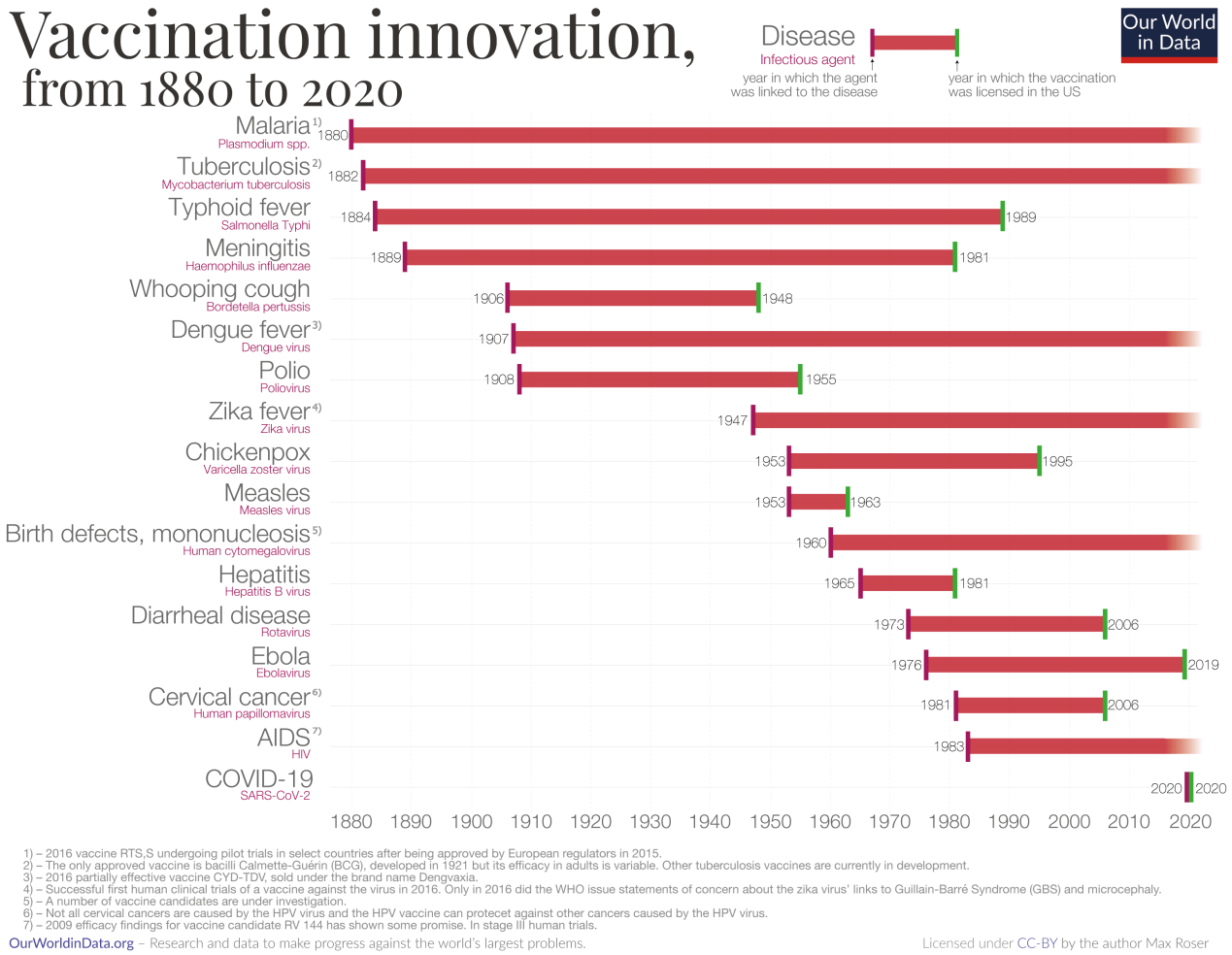
这里的图表显示了疫苗开发创新的时间表。每个条形开始于病原体首次与疾病相关联的年份,结束于针对该病原体的疫苗接种在美国获得许可的年份。
对于某些疾病而言,从感染因子与疾病相关联到疫苗研制出来之间的时间跨度相对较短。2020年前,发展最快的是麻疹。1953年,这种病原体与这种疾病有关,疫苗于1963年在美国获得许可。2020年,这一记录被打破几种疫苗在短短一年内被开发出来疫情冠状病毒.
疟疾事实证明越来越难,因为一个多世纪以来,代理人与疾病联系在一起。阿方斯·莱佛兰在1880年发现疟原虫是疟疾的病因。8
在过去几十年中开发的早期疫苗不够有效,直到最近,没有一项科学努力导致获得许可的疫苗。最近,疟疾疫苗有了新的希望,正如我们在我们关于疟疾条目中的相关部分.
疫苗创新伴随着科学和政治经济的发展:
- 细菌培养技术使得白喉、破伤风和百日咳的细菌疫苗在20世纪早期得以发展。
- 第一次和第二次世界大战促使大学、政府和私营公司共同努力。
- 到了20世纪50年代,病毒组织培养技术使得针对脊髓灰质炎、麻疹、腮腺炎、风疹和水痘。
- 分子生物学的新技术和先进的化学技术最近导致了针对乙型肝炎、流感和肺炎球菌的疫苗,肺炎球菌导致肺炎,脑膜炎球菌导致脑膜炎和败血症。
3.3美国疫苗可预防疾病的进展
这里的可视化显示了在美国引入每种疫苗后,疫苗可预防疾病的病例和死亡的减少。该数据由Roush和Murphy (2007)发表9并且可以在表格中查看数据这里.
对于一些疾病,美国已经实现了100%的病例和死亡减少,对于许多其他疾病,这种减少通常也是非常显著的。

3.4麻疹疫苗的发展和美国麻疹的历史
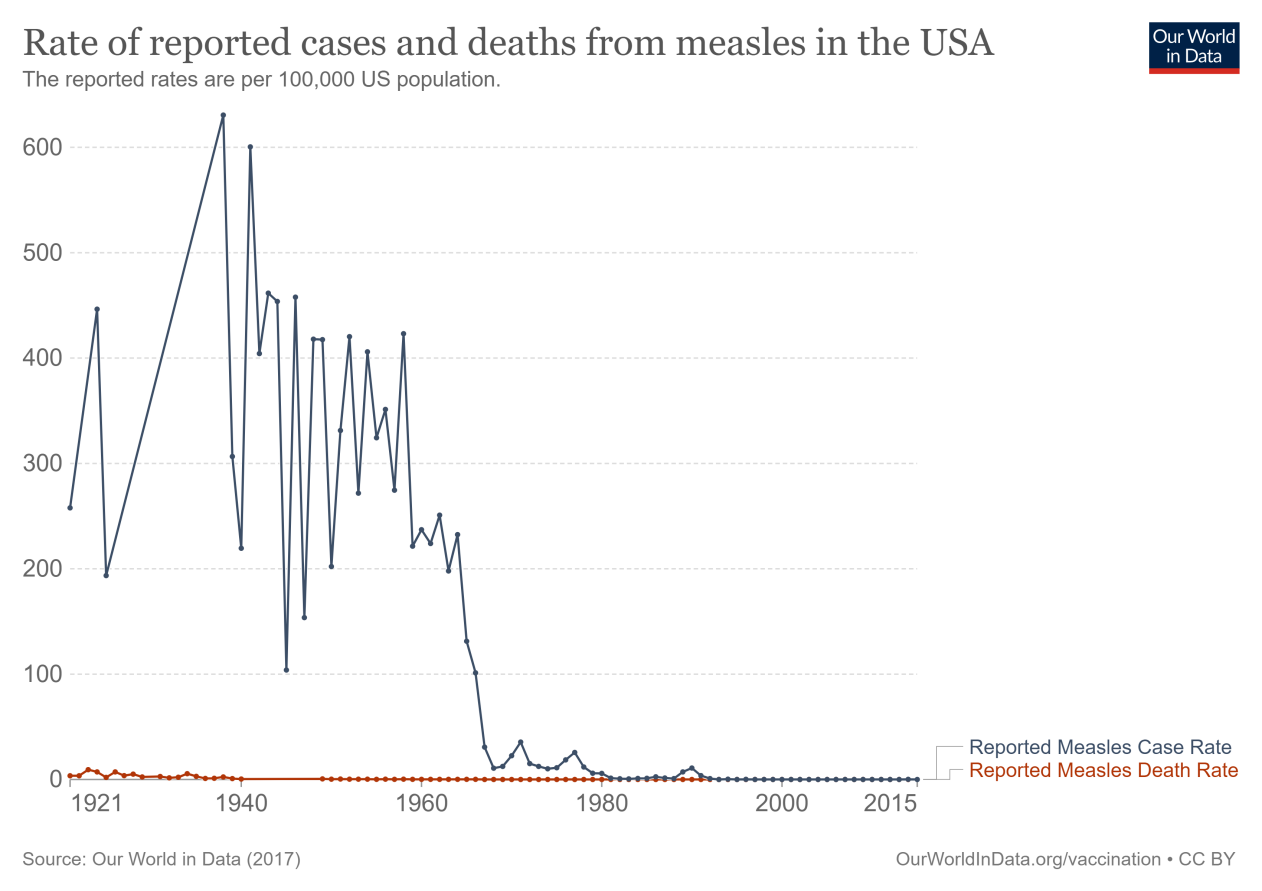
正如可视化显示的那样,疫苗的引入并不是对抗这些疾病取得进展的唯一原因。在1960年引入疫苗之前,高收入国家(如美国)的麻疹病死率一直在下降——从线性轴转换到对数轴可以很好地看出这一点。生活条件、营养和医学进步的改善意味着感染麻疹致死的可能性越来越小。
然而,在引入麻疹疫苗之前,病例率几乎没有变化——正如我们的可视化结果所示。
可以看到显示病例和死亡总数的图像这里.
3.5疫苗可预防疾病的全球下降
世卫组织估计200万到300万人死亡每年通过白喉、破伤风、百日咳和麻疹免疫接种来预防。12
尽管如此,世卫组织还估计,VPD仍然是造成150万人死亡每年。
在图表中,我们看到了从1990年到2017年全球每年5岁以下儿童的死亡人数。完全或部分可通过疫苗预防的死亡人数用彩色显示。13图表显示,在这25年期间,儿童死亡人数的减少主要是通过减少疫苗可预防疾病的死亡人数实现的:非疫苗可预防疾病的死亡人数下降幅度不大,而疫苗可预防疾病造成的儿童死亡人数从1990年的510万下降到27年后的180万。
两种疫苗每年拯救数百万人的生命:预防白喉、破伤风和百日咳的“百白破”疫苗和预防麻疹、腮腺炎和风疹的“MMR”疫苗。14在1963年引入麻疹疫苗之前,麻疹在全球范围内造成了大量死亡,估计为每年260万。因为大约86%的今天世界人口已经免疫,2017年,因麻疹死亡的人数已大幅减少至约95,000人。破伤风和百日咳以前也是更大的杀手,百日咳尤其影响5岁以下的儿童,破伤风打击新生儿(估计杀死了787,000名新生儿与2013年的49,000人相比).
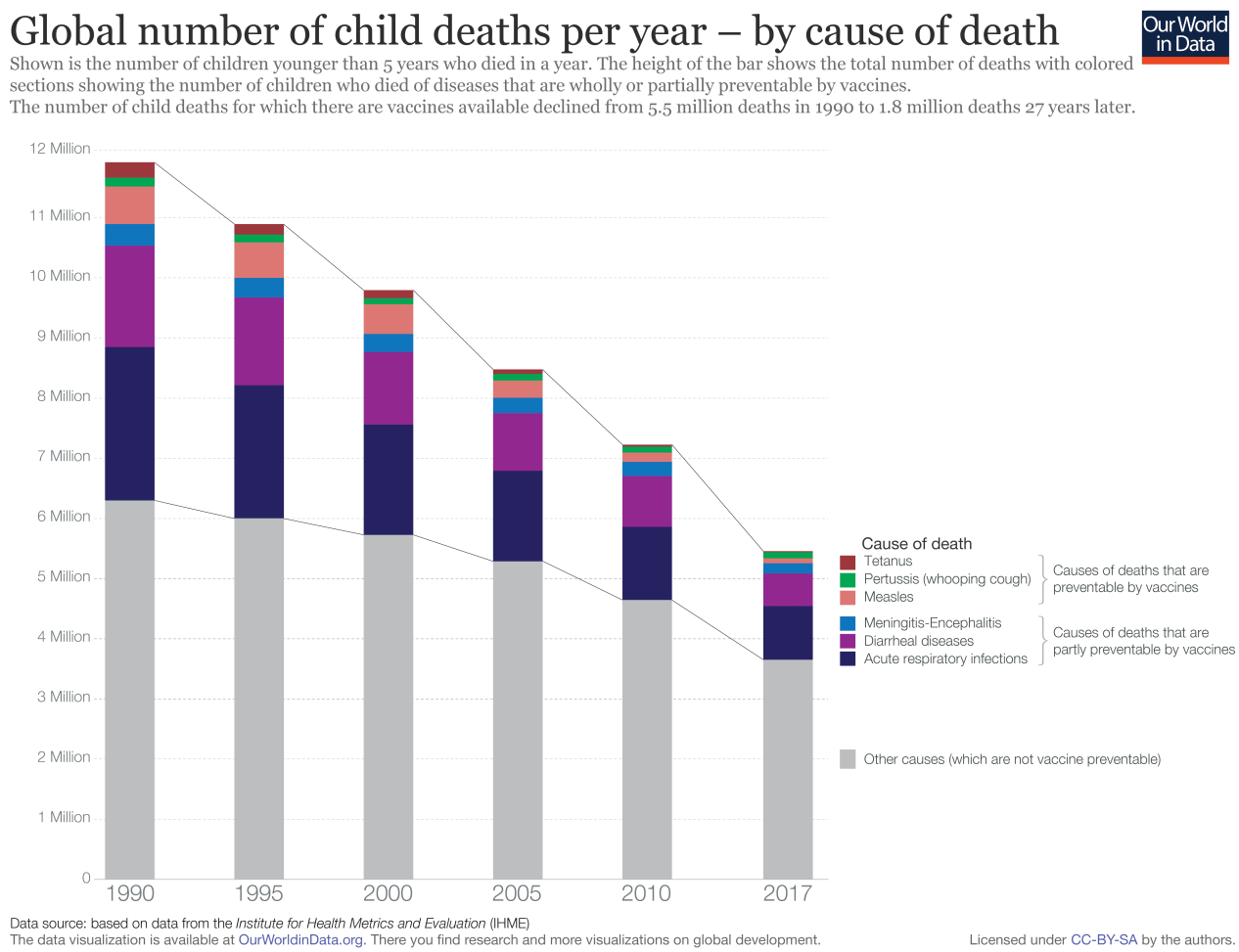
4.前进的道路
然而,全球疫苗接种覆盖率的增长在过去几年中略有放缓。世卫组织估计世界范围内仍然有1950万婴儿有VPD的风险,因为他们错过了基本疫苗。
此外,需要接受所有推荐剂量的疫苗才能发挥最大效力。就麻疹而言,建议接种三剂疫苗。尽管据估计85%的儿童接种了第一剂疫苗,第二剂这一比例降至64%。 因此,问题不仅在于缺乏疫苗接种,而且在于疫苗接种不足导致疫苗可预防疾病(vaccine-preventable diseases ,VPDs)死亡。
那么什么是最致命的VPD呢?哪些疾病继续导致最多人死亡?
5.最致命的疾病
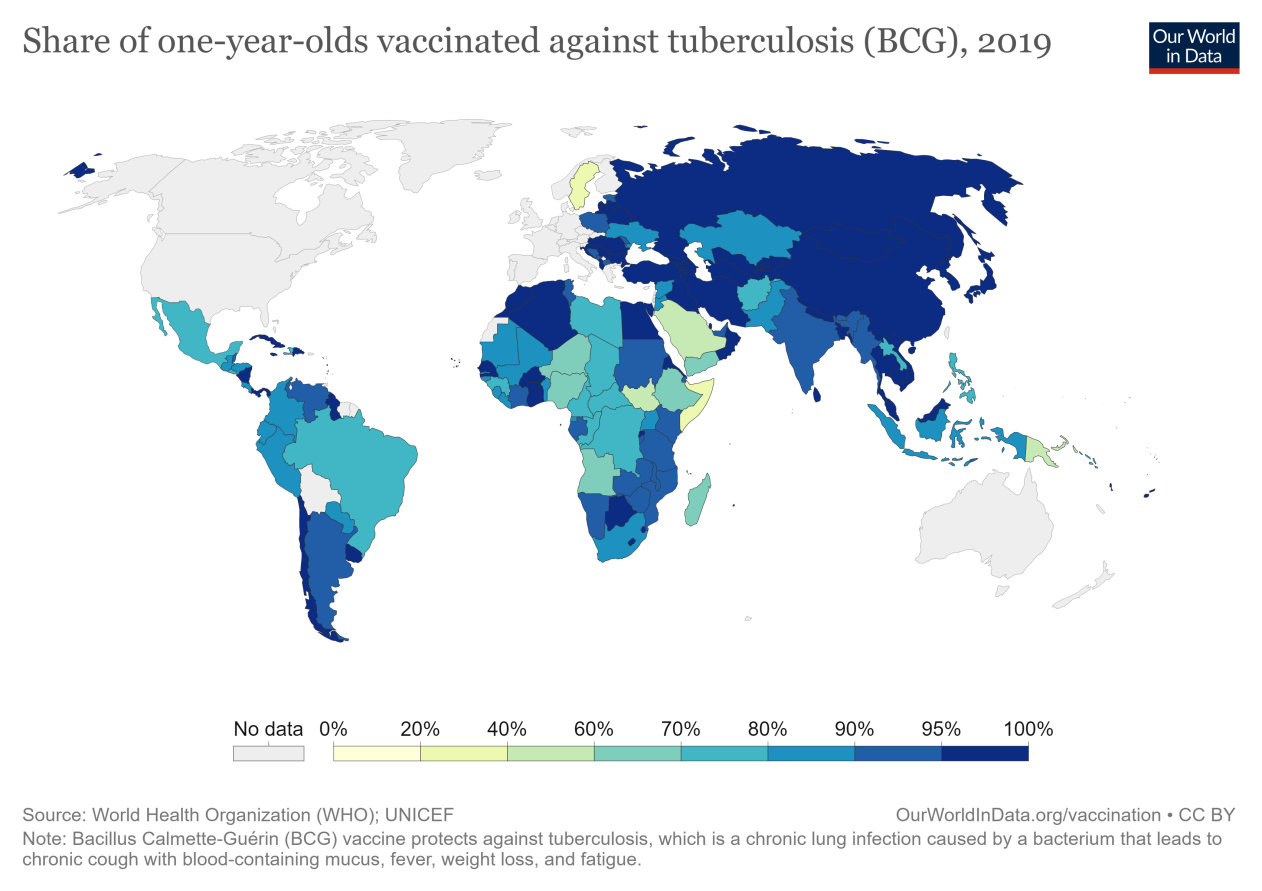
肺结核:确定哪些是最致命的VPD需要承认一些疫苗比其他疫苗更有效。虽然列入国家常规计划的大多数疫苗都非常有效,但迫切需要一种更好的结核病疫苗。尤其是撒哈拉以南非洲和亚洲部分地区受到结核病的影响,如世界地图所示。
结核病疫苗——卡介苗(BCG)——已经使用了近100年。它可以预防严重的肺结核对肺结核无效(在肺中)并对成人具有不同的抗结核效力。
此外,用于治疗结核病的抗生素的耐药性正在增加,这意味着一些人不再能够通过药物治愈。预计2016年有耐多药结核病为49万例。
没有完全有效的疫苗以及抗生素治疗面临严重困难的事实使结核病成为最致命的VPD。
脑膜炎球菌性脑膜炎和乙型肝炎也是致命的VPD。
脑膜炎球菌性脑膜炎:尽管2010年引入了A型流脑疫苗,针对该地区最常见类型脑膜炎的有效疫苗,但在2016年脑膜炎球菌引起的脑膜炎导致近13万人死亡。许多病例发生在从塞内加尔到埃塞俄比亚的撒哈拉以南非洲所谓的“脑膜炎带”。并非脑膜炎地带的所有国家都实施了大规模A型流脑疫苗接种运动并且也不受益于昂贵的A型流脑疫苗将疫苗引入富裕国家以预防其他类型的脑膜炎球菌性脑膜炎。
乙型肝炎:乙肝疫苗也非常有效(在预防疾病方面估计有95%的效率),这意味着增加疫苗接种可以导致死亡人数的显著减少。尽管如此,乙肝疫苗的全球覆盖仍然滞后。2015年,虽然对于第三剂疫苗覆盖率达到84%,出生剂量的覆盖率仅为39%。数学模型的估计表明,如果婴儿覆盖率达到90%,并且在出生时注射第一剂疫苗,84%的全球乙型肝炎相关死亡可以避免。
6.通过接种疫苗根除疾病
根除是疾病疫苗接种的最终目标。
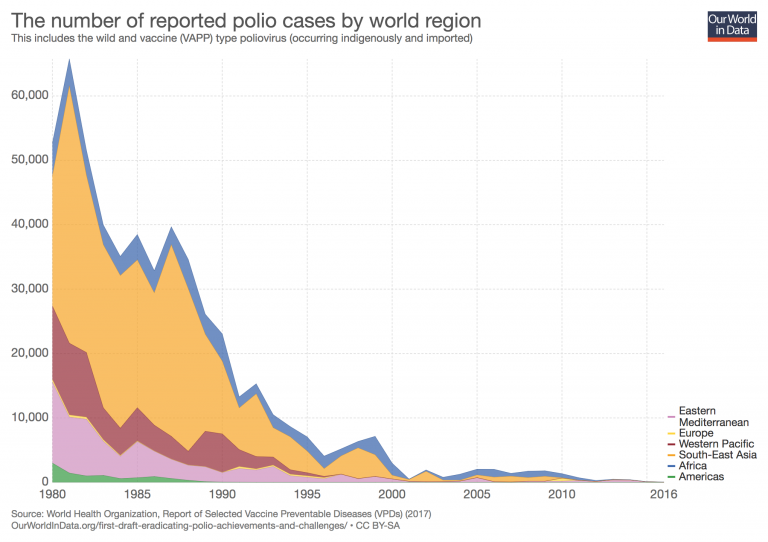
6.1在根除脊髓灰质炎的道路上
脊髓灰质炎是全球根除的目标。1955年开发的脊髓灰质炎疫苗使这成为可能。世卫组织估计,在2015年,全世界85%的婴儿接种了三剂脊髓灰质炎疫苗。自20世纪80年代以来,麻痹性脊髓灰质炎病例的数量减少了99%以上,从每年估计的35万到40万瘫痪病例到2017年报告了22起案件。
我们在一篇完全致力于脊髓灰质炎的文章中提出了根除脊髓灰质炎努力的经验证据。
6.2天花的根除
尽管由于疫苗的引入,疫苗可预防疾病已经失去了威胁,这些好处可能会被遗忘,但世界各地的人们——包括较富裕国家的人们——继续受益于疫苗接种仍然是事实。
全球卫生最大的成就之一是根除了天花。由于全球疫苗接种计划,仅仅几十年前每年导致几十万人死亡的天花在1980年被成功根除。
你可以在我们关于天花的条目中找到关于这种疾病及其根除的更多细节。
7.公众的支持和怀疑
人们不知道我们在全球疫苗接种方面做得有多好
全世界有多少人支持接种疫苗?
疫苗怀疑论会影响免疫覆盖率吗?
7.1人们不知道我们在全球疫苗接种方面做得有多好
今天,疫苗保护了全世界数百万人免受传染病的侵害。在这场斗争中,我们比大多数人意识到的要领先得多。
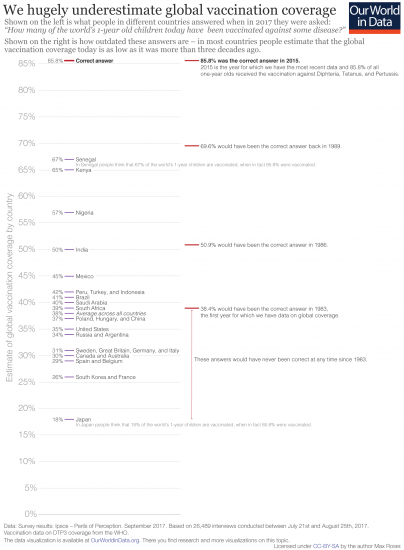
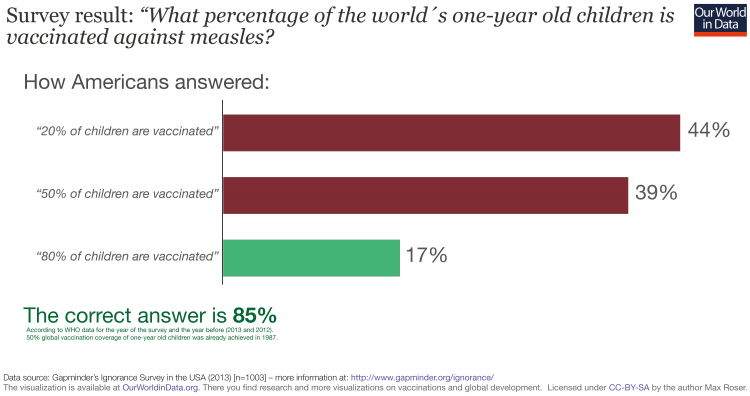
第一张图表显示了这种误解的证据。在这张图表中,我们绘制了人们在被问到时的回答“今天世界上有多少1岁的儿童已经接种了某种疾病的疫苗?”。正确答案为85.8%;这是1岁儿童接种第三剂预防白喉、破伤风和百日咳混合疫苗的比例。
但在所有接受调查的国家,人们对全球覆盖面都过于悲观。美国人认为世界上只有35%的儿童接种了疫苗,真实覆盖率高出50个百分点。22
在日本,人们甚至更悲观,认为只有18%的人接种了疫苗。正如在全球发展问题中经常出现的情况一样,我们再次看到,较贫穷国家的人民对世界更准确的看法:在肯尼亚和塞内加尔,人们认为世界上大约三分之二的儿童接种了疫苗,但即使是这些最高的估计也低了20个百分点。
我们大大低估了全球疫苗接种覆盖率23
7.2人们对疫苗接种覆盖率的看法已经过时了30多年
这里的图表说明了人们的回答有多过时。大多数人认为今天的全球疫苗接种覆盖率与20世纪80年代甚至更早的时候一样低。24
世界卫生组织建议常规接种疫苗以预防疾病、死亡和残疾,包括白喉、百日咳、破伤风、脊髓灰质炎、麻疹和乙型肝炎。25
我们创造了一个图表这显示了接受疫苗接种的一岁儿童的绝对数量。
疫苗接种的最大差距在于,所有儿童都接受了全面的疫苗接种,并尽可能避免感染传染病。疫苗联盟Gavi的分析表明在73个最贫穷的国家中,7%的婴儿完全免疫(即接受所有推荐疫苗的所有剂量).
7.3全世界有多少人支持接种疫苗?
总部设在伦敦的研究慈善机构威康信托基金会发表了他们的惠康全球监测2019年关于对科学和重大健康挑战的态度。这是世界上同类研究中规模最大的,调查了来自140多个国家的140,000多人。作为的一部分盖洛普世界民意测验,这项30个问题的调查在2018年进行。26
威康信托基金会的调查提出了三个与对疫苗的态度相关的核心问题:人们是否认为疫苗对儿童来说很重要;他们认为疫苗安全吗?他们相信疫苗是有效的吗?
7.4世界上大多数人认为疫苗对儿童来说很重要
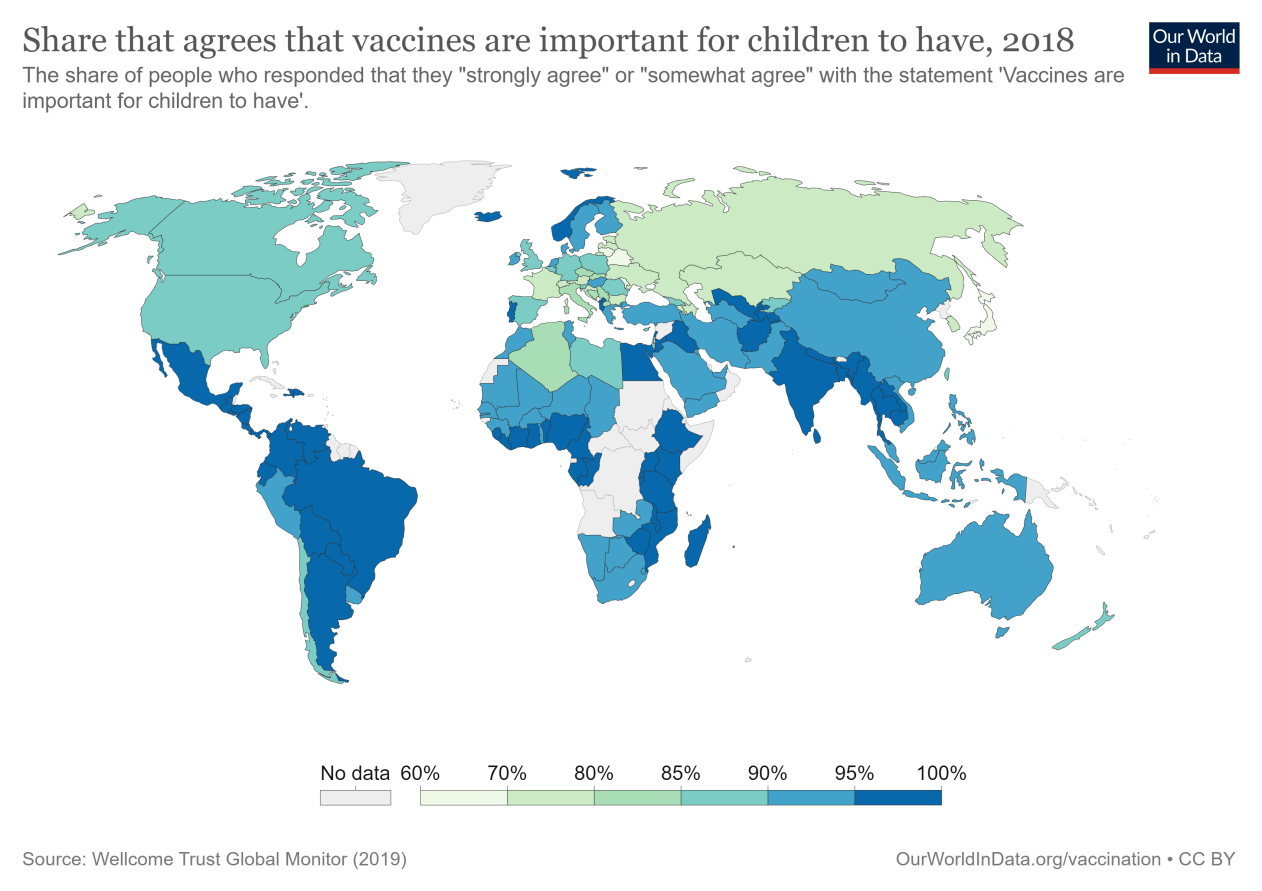
世界上超过90%的人(92%)认为儿童接种疫苗很重要。
地图上显示了世界各地的支持情况。我们看到几乎所有国家都高度支持疫苗接种。在大多数国家,超过80%的受访者认为儿童疫苗接种很重要,在许多国家,这一比例超过90%。
在态度上存在明显的南北分歧:南亚的支持率最高,为98%;南美97%;北非94%;92%在南部非洲。支持率仍然很高,但在整个北美地区有所下降(87%);西欧(83%)和东欧(80%)。
在委内瑞拉、巴勒斯坦、埃塞俄比亚和北塞浦路斯接受调查的人中,100%的人认为疫苗最重要。27
7.5世界上大多数人认为疫苗是安全的,但在一些国家不信任度很高
如果一些父母认为疫苗不安全,或者可能会产生弊大于利的副作用,他们可能不同意孩子接种疫苗。这些安全问题有多普遍?
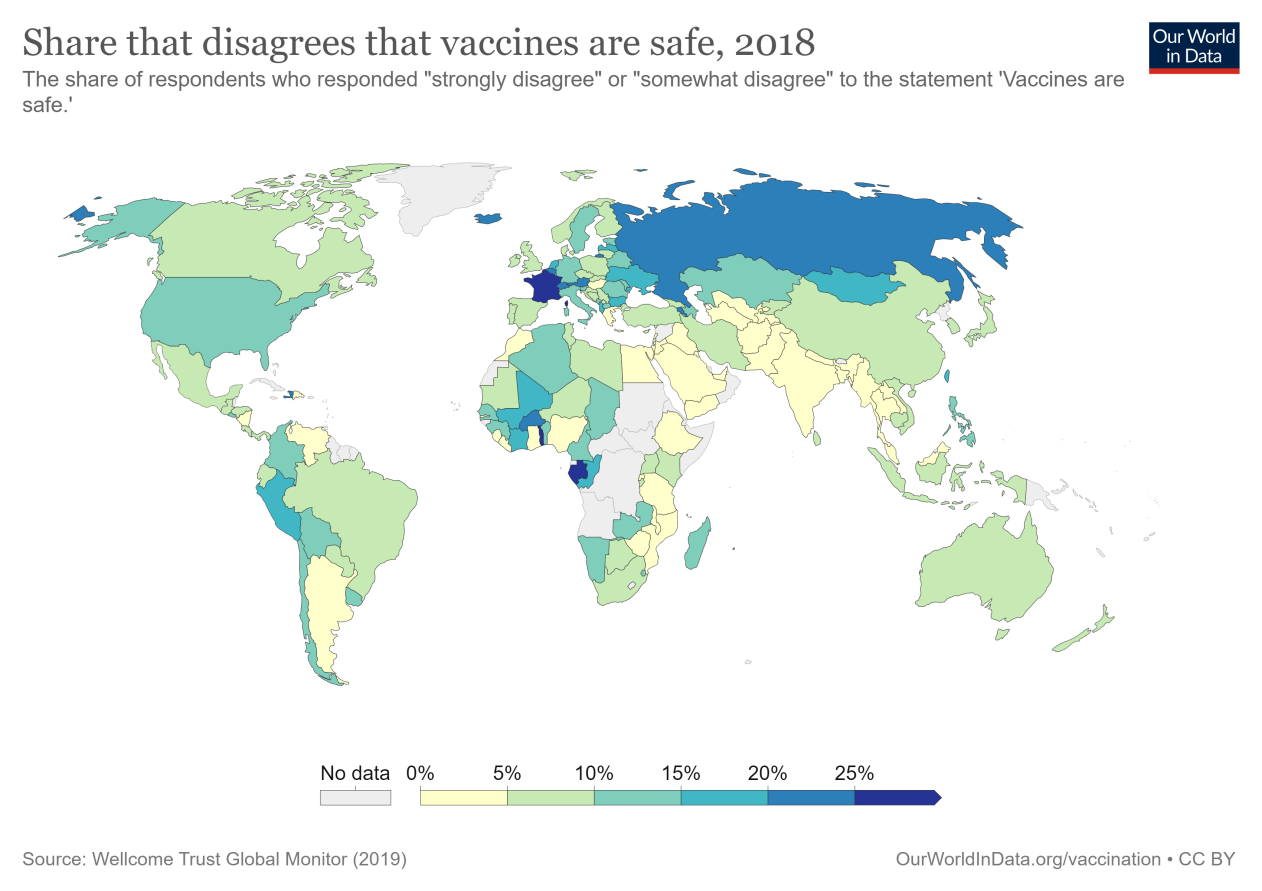
在全球范围内,一小部分人不同意疫苗是安全的。全世界只有7%的受访者表示他们“强烈不同意”或“有点不同意”疫苗是安全的这一说法。
在许多国家,这些担忧非常少:例如,在孟加拉国,不到1%的人不认为疫苗是安全的。在邻国印度,只有2%的人不同意。我们可以在地图上看到这种分布。
对疫苗的信任度并不是到处都很高。有一些明显的异常值。法国人对此最为怀疑:三分之一的人不认为疫苗是安全的。邻国瑞士和比利时的许多人也非常怀疑:超过20%的人不同意。对疫苗安全高度不信任的其他国家有加蓬(26%);多哥(25%);俄罗斯(24%);奥地利(21%)和冰岛(21%)。
7.6全球只有5%的受访者不同意疫苗有效,但在一些国家持怀疑态度的人要多得多
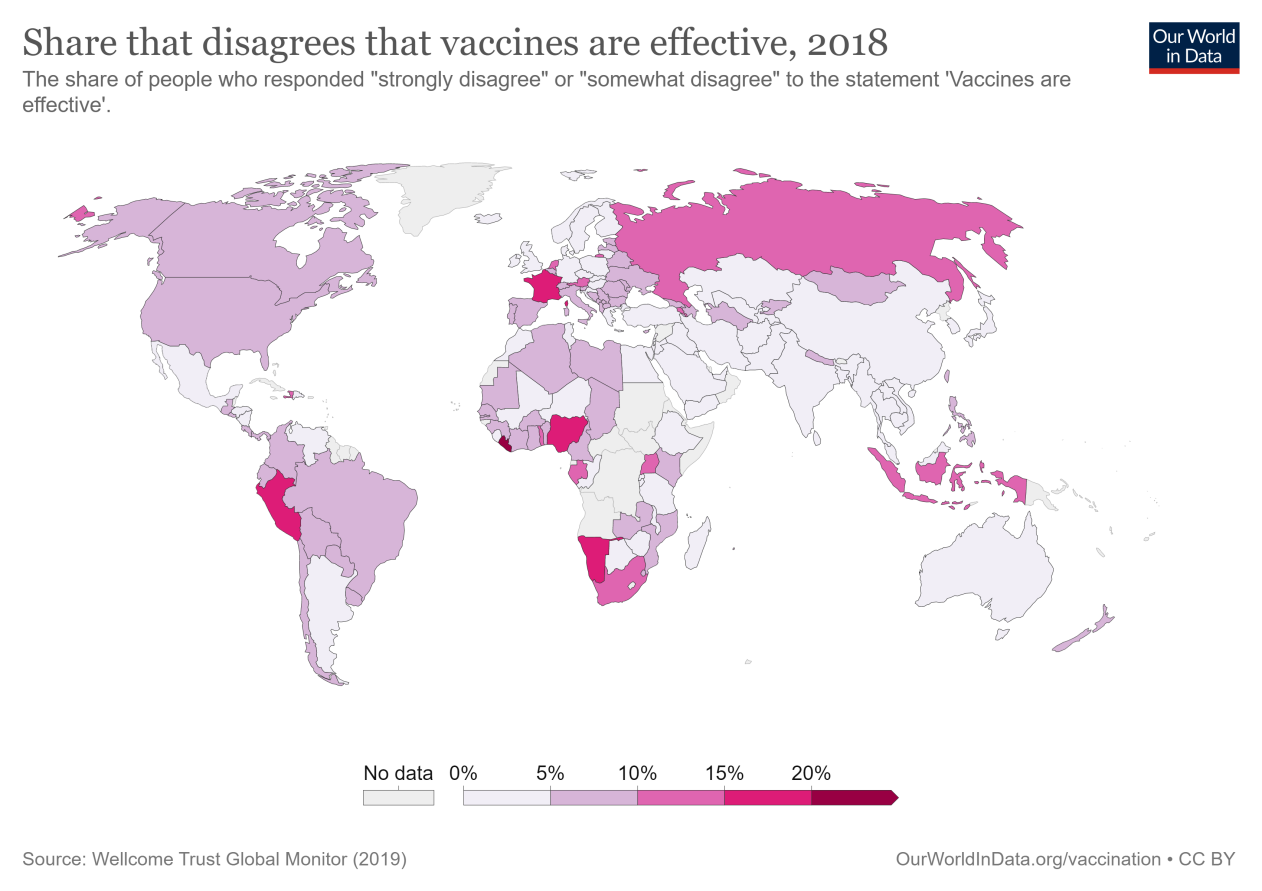
对于“疫苗是有效的”这一说法,所有被调查国家中只有5%的受访者表示“强烈不同意”或“有些不同意”。绝大多数人不认为疫苗是无效的。
但是,和其他被调查的问题一样,这在不同的国家有很大的不同。我们在地图上看到了这个。在一些国家,极少数受访者不同意:在孟加拉国和埃及不到1%;印度和埃塞俄比亚为2%;而中国、德国和英国为3%。
利比里亚持最怀疑的态度,28%的人不同意疫苗是有效的。但是法国的怀疑态度也很高(18%);纳米比亚(16%);尼日利亚(16%);和秘鲁(15%)。
7.7在一些国家,许多人对接种疫苗犹豫不决
威康信托基金会发现人们对疫苗持非常积极的态度——这是一种健康干预措施拯救了数百万人的生命和根除了最严重的疾病之一这是一个非常积极的发现。
但是,当我们只看全球监测中对问题的同意和不同意时,有一个令人担忧的发现被隐藏了。
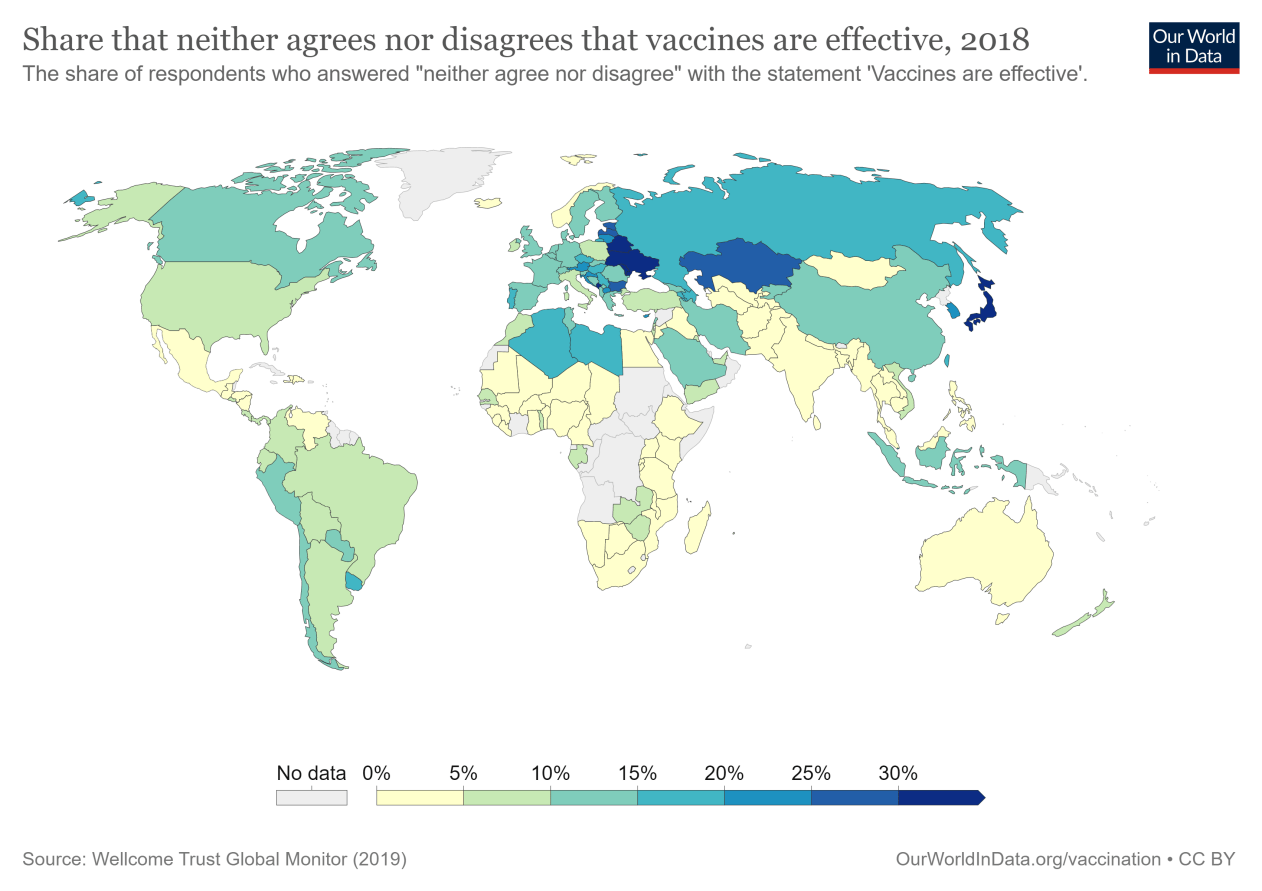
以日本为例。只有66%的日本受访者认为疫苗对儿童很重要——与其他国家相比非常低。但是很少有人不同意疫苗是安全的(只有8%),也很少有人不同意疫苗是有效的(只有3%)。如果很少有人认为疫苗是不安全和无效的,为什么对疫苗的支持会如此之低?
许多日本受访者两种回答都没有。28%的人回答“既不同意也不反对”儿童疫苗接种是否重要;55%回答了关于疫苗的安全性;三分之一的人对其有效性没有定论。在这里,没有进一步的问题,很难完全解释这些未决定的人的意见:也许他们没有意见;或者他们认为疫苗在某些情况下是安全或有效的,但不是所有的情况;或者一些疫苗是安全的,但其他的不是。有了这些数据,完全理解他们的推理是不可能的。
正如我们在地图上看到的,这种姿态在其他几个国家也很普遍。
虽然在疫苗接种的重要性、安全性和有效性方面,犹豫不决或意见分歧可能不如否定主义更令人担忧,但这仍然表明许多人没有意识到疫苗在免疫接种中发挥的巨大作用根除疾病,以及拯救世界各地的生命。疫苗的成功故事是一个我们不常提及的故事。
“两者都不是”组的人可能更容易被那些否认疫苗接种的安全性、有效性和重要性的人提出的论点所说服,这也是事实。
在一个相关帖子我们来看看为什么围绕疫苗接种的否定主义存在,以及什么是解决它的有效方法。
7.8疫苗怀疑论会影响免疫覆盖率吗?
当考虑疫苗怀疑主义的重要性时,要问的关键问题是:它实际上对行为有影响吗?真的会影响接种疫苗的儿童比例吗?
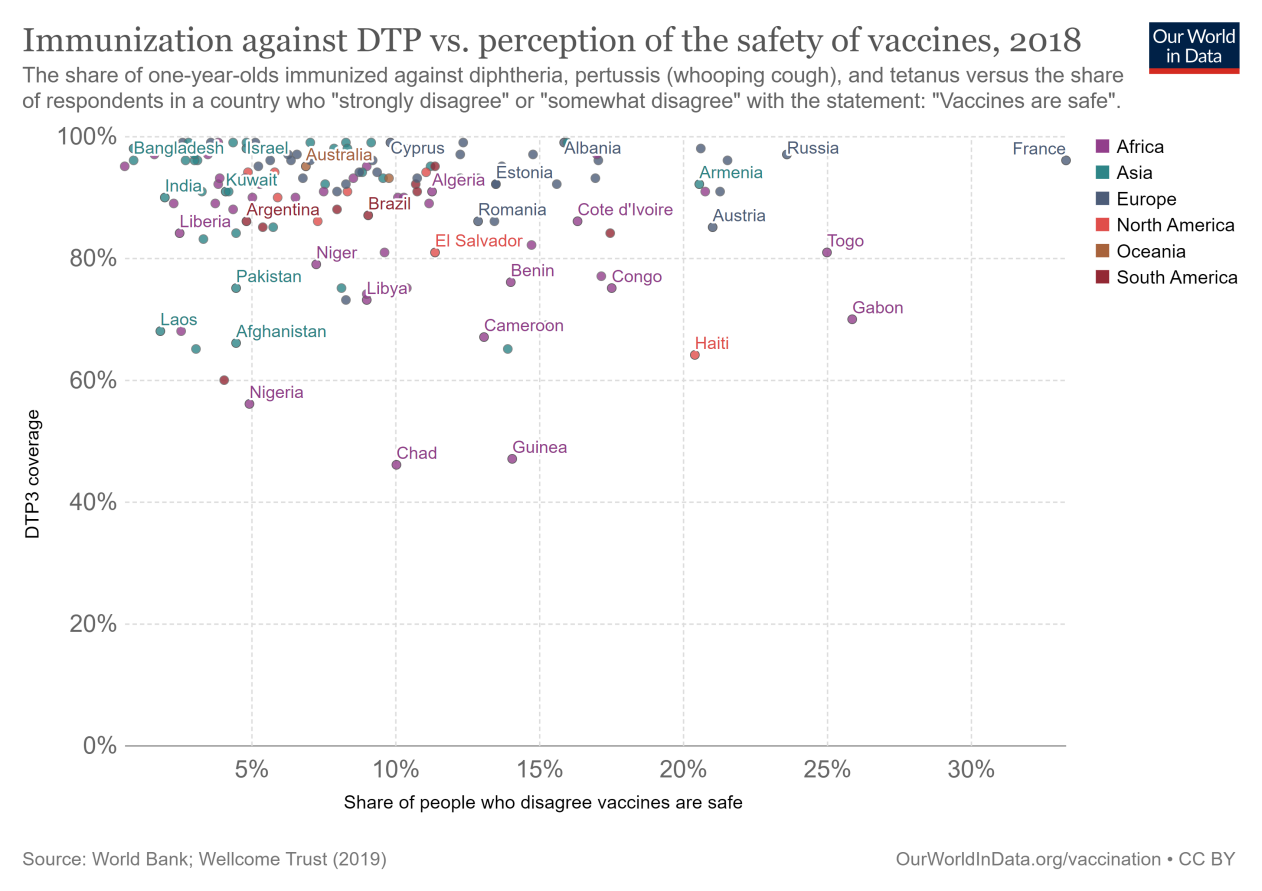
在图表中,我们看到了疫苗接种率的比较——这里是2015年接种白喉、百日咳和破伤风疫苗(DTP)的儿童比例,这是可获得的最近一年——与给定国家中不同意疫苗安全的受访者比例的比较。
你也可以看到这个关系了吗麻疹疫苗覆盖率。
总的来说,我们看到公众对疫苗安全性的广泛关注似乎与疫苗接种率没有很强的相关性。虽然三分之一的法国公众不同意它们的安全性,但法国97%的儿童都接种了疫苗。
然而,一些国家疫苗接种率低还有许多其他原因:在中低收入国家,疫苗的可获得性、可负担性和可获得性可能很差。覆盖率低往往不能反映人们对它们的看法。在许多贫穷国家,情况与法国相反:绝大多数人认为疫苗是安全的,但只有大约二分之一的儿童接种了百白破疫苗。
一个突出的国家是乌克兰:我们看到那里的疫苗接种率异常的低其收入水平–不到四分之一的儿童接种了百白破疫苗。乌克兰对疫苗安全性的怀疑度高达15%。
有证据表明怀疑态度反映在疫苗可预防疾病的病例和死亡中吗?在过去的几年里报道的增长在以前接近消灭麻疹的国家中,麻疹病例的数量。例如,在欧洲,有超过34000例麻疹仅2019年前两个月。乌克兰占了大多数(70%以上)这些情况。在这里以及阿尔巴尼亚和罗马尼亚,一些麻疹病例导致了儿童死亡。
针对百白破的免疫接种与对疫苗安全性的认知,2018
这 分享 关于 一岁的孩子 免疫的 反对 白喉, 百日咳 (欢呼 咳嗽), 和 破伤风 对抗 这 分享 关于调查对象 在 a 国家 谁 “强烈地 不同意” 或者 “有点吧 不同意” 随着 这 声明: “疫苗 是 安全”。
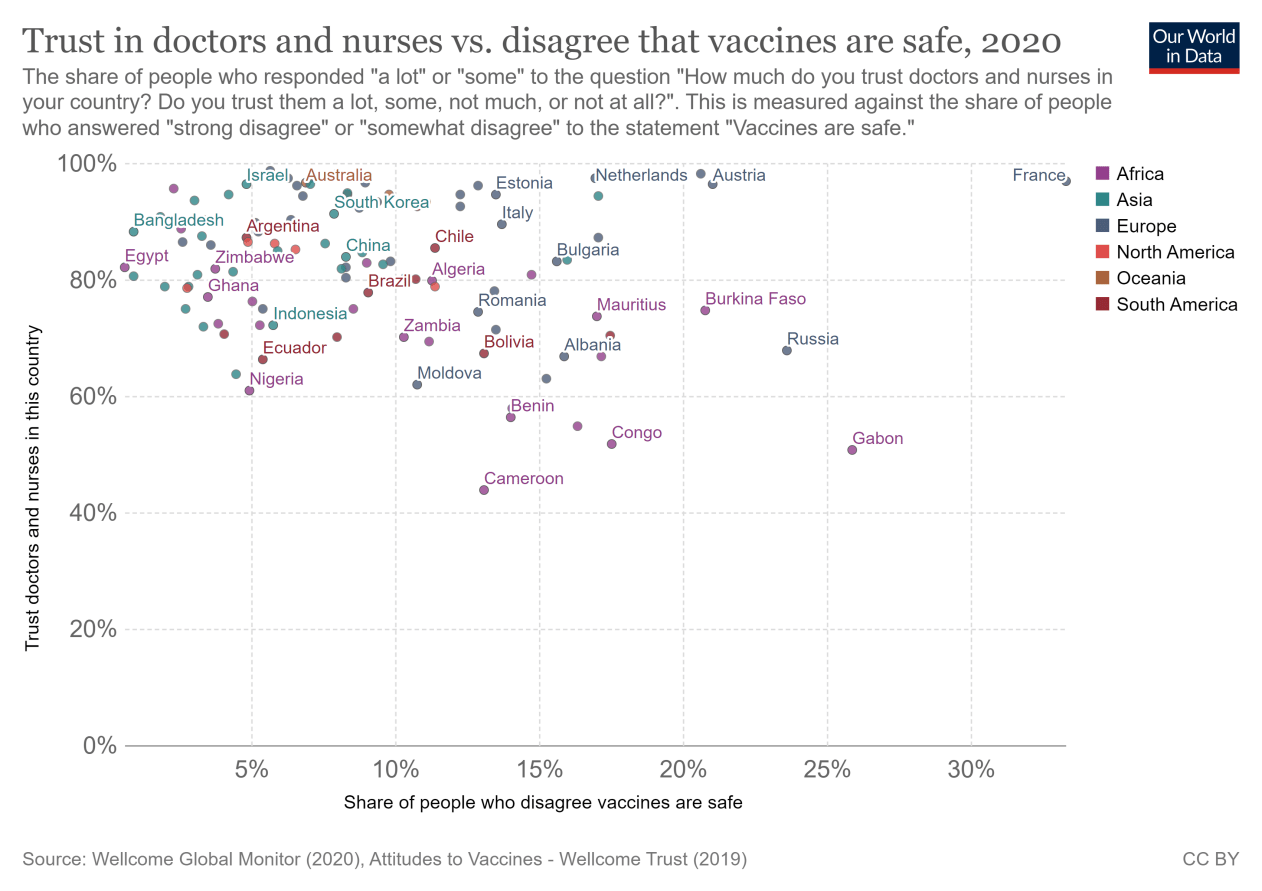
可视化显示了信任本国医生和护士的人的比例与不同意疫苗安全的人的比例之间的关系。总的来说,我们发现,对疫苗安全性不信任程度较高的国家往往对卫生专业人员的信任度也较低。
然而,也有一些例外:法国对卫生工作人员的信任度相对较高,但对疫苗的安全性最不信任。
卫生官员担心,对疫苗接种的怀疑将开始转化为疫苗接种率的降低。怀疑情绪高涨的一个原因是社交媒体上错误信息的传播。
社交媒体公司确实有责任处理错误信息,并需要考虑如何谨慎应对。目前,美国和英国的政治家要求社交和在线媒体公司禁止或控制反疫苗接种信息。禁止或严格控制可以减少对这类信息的接触,但不能解决根本问题:公众正在询问有关疫苗的问题,并希望在网上找到答案。一种担忧是,禁止某些类型的信息和团体会加剧猜疑,只会推动其他地方的活动。
尽管如此,要求社交媒体公司采取行动的呼声越来越高。要求采取行动亚当·希夫致谷歌和脸书的首席执行官引发了一连串的反应。在一封公开信中,他要求对疫苗错误信息采取行动,此后,英国卫生大臣马特·汉考克等人也提出了类似的要求。
8.疫苗政策
什么决定了疫苗接种是否是强制性的?
疫苗供应
疫苗的成本
为什么疫苗接种时间表不同?
哪些国家有强制性儿童疫苗接种政策?
世界各地的儿童疫苗接种政策有何不同?
强制疫苗接种政策因地区而异?
是什么推动了强制性疫苗接种的引入?
8.1什么决定了疫苗接种是否是强制性的?
各国在疫苗接种是强制性的、强制的(根据具体要求)还是自愿的方面有所不同。Navin和Largent (2017年)对这些政策进行了有益的区分。强制性政策是当拒绝接种疫苗是非法的,而强制性接种疫苗时,某些商品和服务是有限的,因为不接种疫苗。28
遵循何种政策在很大程度上取决于历史遗产,当人们考虑到世界各地的一些不同法规及其历史时,这一点就变得很清楚了:
强制性疫苗接种:许多东方集团国家在共产主义时代引入了强制性疫苗接种。例如,在罗马尼亚,疫苗接种以前是强制性的,在疫苗接种率下降后,该国正在经历重新引入强制性疫苗接种的过程。意大利和法国也是如此,它们对三种疾病进行了强制接种,但由于疫苗接种率下降,2018年1月将这一数字增加到11种。
强制性疫苗接种:一些国家,如美国,要求儿童在进入公立学校或日托所时必须接种疫苗。美国的一个早期案例为各州根据个人自由保护公共健康的司法管辖权铺平了道路。29在雅各布森诉马萨诸塞州(1905)一案中,最高法院裁定,在天花流行期间,各州有权要求接种天花疫苗。从那时起,美国就有了学校疫苗接种要求的历史。《义务教育法》导致公立学校学生人数增加,通过在拥挤的大教室中密切接触,导致天花爆发的风险增加。30同样,在澳大利亚,有两项政策惩罚不给孩子接种疫苗的父母。“不打就不玩”政策将未接种疫苗的儿童排除在国家资助的儿童保育机构之外。2016年的“不打预防针就不付钱”政策取消了国家福利,因为它不向出于良心拒绝接种疫苗的父母提供普遍的“家庭津贴”福利金。
自愿接种疫苗:一些自愿接种疫苗的国家很早就反对接种疫苗,如英国和荷兰。1853年,英格兰和威尔士通过了一项法律,要求普遍接种天花疫苗,但来自反疫苗主义者的反对导致通过了允许出于良心拒服兵役的法律。31
入境疫苗接种要求:对于黄热病流行或存在蚊媒的非洲和南美洲国家,需要疫苗接种证明。只有这样,该国才会在入境时签发签证,以防止这种疾病的输入(特别是如果旅行者来自或曾到过其他黄热病流行地区)。32在过去的几个世纪(17至19世纪),黄热病传播到北美和欧洲,导致大规模爆发,破坏了经济和发展,在某些情况下导致大量人口死亡。在整个18世纪和19世纪,黄热病是新旧世界港口最可怕的疾病之一。沙特阿拉伯是唯一要求脑膜炎球菌病和脊髓灰质炎的额外疫苗接种去麦加朝圣的朝圣者。
8.2强制接种疫苗有效吗?
强制接种疫苗是否会提高疫苗接种率并不是一个简单的问题,因为它在很大程度上取决于国家背景、历史环境、文化和社会规范,以及实施和执行此类法律的可行性。
当然在东方集团国家当《疫苗接种法》是强制性的时,疫苗接种率一直很高,但不清楚这是因为法律还是因为共产党统治下的行为和合规机制。某些疫苗在历史上是强制性的,如天花、脊髓灰质炎和黄热病。这里的疫苗接种率也很高,但这也鼓励了对疫苗接种的有组织的反对和公众的不满。这是公共卫生当局的一个主要担忧,即政府和公民之间的信任关系受到威胁(特别是在鼓励自我责任、个性化和选择的健康领域)。
有些国家的疫苗接种率很高,但却没有强制接种疫苗,政府不希望通过强制接种疫苗来破坏公众信任和自我责任,特别是在没有必要接种疫苗的情况下。有人认为高覆盖率是通过“其他方法或努力”实现的,因此在瑞典、挪威、丹麦、荷兰和英国等国家接受强制性疫苗接种可能会有问题。33
近年来,政府已经采取行动应对流行病,强制接种疫苗,正如我们在2017-18年看到的法国、意大利、德国和罗马尼亚的强制接种疫苗。
我们可以看到疫苗接种政策变化影响的一个国家是美国。在美国,各州决定允许在学校接受教育或使用日托的儿童接种哪些疫苗。不幸的是,公立学校意味着学校是儿童疾病的流行场所,这就是为什么需要这样的疫苗接种法。
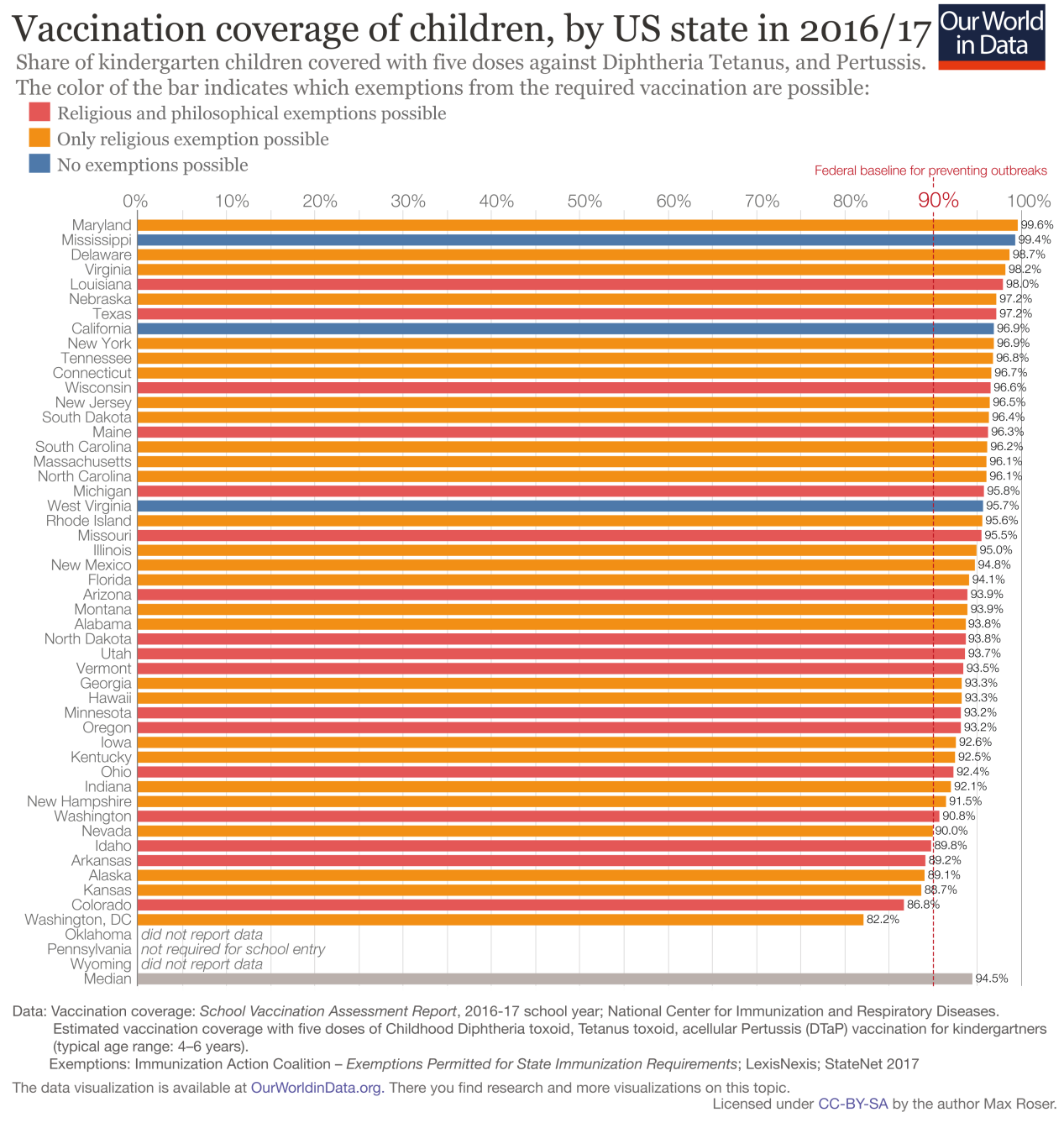
在个别国家,豁免是出于医疗原因,但许多国家也允许哲学、个人信仰或宗教豁免。只有三个州——密西西比州、西弗吉尼亚州和加利福尼亚州——允许医疗豁免。加州的免疫接种率已经上升继2015年参议院新法案SB 277取消疫苗接种的非医疗豁免后。
这里的图表显示了疫苗接种覆盖率和每个州允许的豁免。更少的豁免通常意味着更高的疫苗覆盖率。事实上,密西西比州经常被列为疫苗接种率最高的州,因为该州只允许医疗豁免。但显而易见的是,密西西比居民也一直是不健康的和贫困的在整个国家。健康状况很差,许多居民负担不起医疗保健费用(2017年,该州没有医疗保险的比例最高).因此,居民接受获得儿童保育和公立学校所需的补贴疫苗接种或许并不令人惊讶。
8.3疫苗供应
供应限制给国家获得疫苗接种带来了问题。根据,194个国家中有三分之一的国家已经在一个月或更长时间内用完了疫苗数据提交给世卫组织和联合国儿童基金会——这包括高收入和低收入国家。在美国,疾病控制和预防中心(CDC)声明短缺的原因是多方面的,包括“……公司退出疫苗市场、制造或生产问题以及库存不足”。2018年,它被举报疫苗供应严重不足的短缺包括针对黄热病、乙型肝炎、霍乱、丙型脑膜炎、白喉、百日咳、破伤风、甲型肝炎和结核病的疫苗。
人们对疫情疫情中的疫苗供应表示担忧。例如,2016年在安哥拉爆发的黄热病疫苗供应有限,导致建议分剂量扩大现有供应。35
劳里·加勒特认为由于这种药物变得如此便宜(2008年每支疫苗60美分),很少有公司有动力生产它,而且疫苗的世界库存接近于零,迫使世卫组织将来自巴西等国家的捐赠疫苗(发送了1800万剂)稀释为5比1,希望它们仍然足够有效。罗马尼亚在2016年经历了平行疫苗出口的情况,出口的疫苗多于供应的疫苗,以满足该国的需求。麻疹、腮腺炎和风疹(MMR)疫苗的短缺是2016-17年麻疹爆发的部分原因。36
在经历经济危机的委内瑞拉,存在着严重的包括疫苗在内的药品短缺,这导致了估计有一百万未接种疫苗的儿童以及白喉和麻疹等疾病的重新出现。
8.4疫苗的成本
有五大制药公司37占疫苗产量80%的公司有:赛诺菲巴斯德、葛兰素史克、默克、辉瑞和诺华。38
许多疫苗只由一两家供应商提供。对于较新的疫苗,由于开发疫苗所需的高投资,供应商通常特别少。39正如人们对竞争的预期,世卫组织报告说,当更多的供应商生产疫苗时,会导致这些疫苗的价格下降。40
过去,疫苗通常被制药公司视为利润较低的产品,这导致投资不足,一些公司干脆退出生产。41
但随着全球疫苗市场收入的增加,以及富裕国家政府和保险公司愿意为新疫苗支付更多费用,这种情况已经发生了变化。
此外,印度和中国等增长中的经济体正在加大对疫苗的投资,并发展其国内生产能力。较贫穷的国家现在有全球疫苗和免疫联盟来帮助政府集中资源和作出预先购买承诺。42
Gavi是一个成立于2000年的国际组织,旨在将公共和私营部门聚集在一起,为贫困国家的儿童平等提供新的和未充分使用的疫苗。它补贴低收入国家负担不起的疫苗。除了补贴疫苗本身,免疫联盟还提供疫苗引进赠款,这有助于支付将新疫苗引入常规免疫计划的费用。这里的地图显示了哪些国家有资格获得GAVI的支持。
一些疫苗仍然很贵。例如,百日咳疫苗有两种版本:含有完整百日咳细菌的全细胞(wP)或含有部分百日咳细菌的无细胞(aP)。百日咳疫苗通常与白喉和破伤风混合生产DTwP或DTaP疫苗。43
DTaP稍微贵一点;它有时被称为“无痛疫苗”,因为它引起的局部反应和疼痛较少,但不应给7岁以上的儿童使用。然而,DTwP已被证明在预防疾病向未接种疫苗的人和免疫力弱的人传播和扩散方面更有效。
新疫苗往往更贵,因为它们受专利保护。例如,当开发HepB疫苗时,许多低收入国家负担不起每剂30美元的费用。44
今天,各国支付的价格之间往往存在差异,如小表所示。
美国和发展中国家疫苗的价格差异45
| 疫苗 | 发展中国家的每剂成本 | 美国的每剂成本 |
| 乙肝 | $0.58 – 13.20 | $50 – 100 |
| 卡介苗 | $0.16 – 1.11 | $100 – 200 |
| 黄热病 | $4.30 – 21.30 | $50 – 100 |
8.5为什么疫苗接种时间表不同?
水痘的例子
水痘(水痘)是一种疫苗的例子,一些国家将其纳入常规的儿童疫苗接种计划,而其他国家则没有。接下来的问题是,为什么对是否推广疫苗有不同的看法。日本是最早普及水痘疫苗接种的国家之一。46
澳大利亚、加拿大、德国、卡塔尔、韩国、沙特阿拉伯、中国台湾、乌拉圭、美国、意大利(仅西西里岛)和西班牙(仅马德里)随后跟进,并采用了普遍水痘疫苗接种。当极端的水痘病例发生时,人们呼吁疫苗成为免费提供通过英国的国民医疗服务体系。然而,大多数欧洲国家不接种水痘疫苗,除了“高危”人群。不采用普遍接种的主要原因是费用高。其他支持理由是,它通常是一个轻度疾病以及带状疱疹病例减少的好处——如前所述这里.
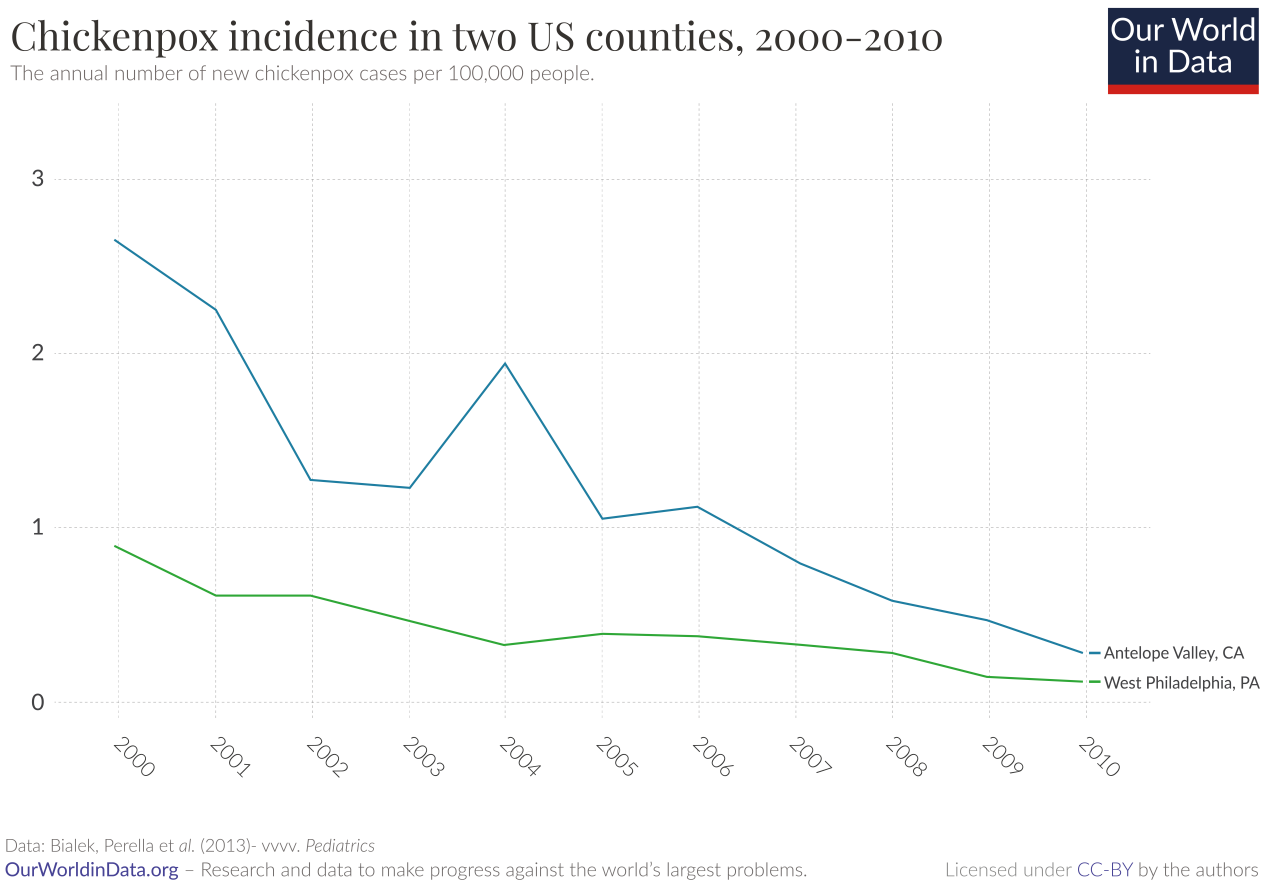
美国疾病控制和预防中心负责水痘主动监测项目(VASP)从1995年到2010年监测水痘疫苗接种计划的影响,图表中显示了主要发现。洛杉矶县的疫苗覆盖率从1997年的37.9%上升到2010年的95.1%,费城从1997年的41.2%上升到2010年的94.6%(19至35个月大的儿童接种一剂疫苗)。到2010年,与1995年相比,羚羊谷(加利福尼亚州)和西费城(宾夕法尼亚州)的水痘发病率下降了98%。疫情和住院率也迅速下降。从1995年到1998年,住院率从每100,000人中2.2人到3.3人不等,但到了2006-2010年,这一比率在羚羊谷下降到每100,000人中0.2人,在费城下降到每100,000人中0.5人。
水痘就是一个例子,它也有助于回答这样一个问题,即更好的卫生条件或疫苗接种实际上是否是降低发病率的原因。虽然两者都很重要,但在卫生的重要性被发现并成为疾病的预防措施后,最近采用的疫苗接种如水痘疫苗接种可以证明疫苗接种在降低发病率方面的作用。由于卫生标准已经达到很高的水平,疫苗的额外益处得到了证实。对发病率的影响表明,在美国如此显著地降低水痘发病率的不是卫生,而是疫苗接种。
8.6哪些国家有强制性儿童疫苗接种政策?
随着的广泛推广新冠肺炎疫苗在全球范围内,一些国家已经开始考虑强制接种疫苗,尽管还没有一个国家强制其人口接种疫苗。47虽然新冠肺炎重新引起了关于疫苗接种政策的争论,但它一直是许多其他疾病的重要话题。世界卫生组织(世卫组织)估计,疫苗每年拯救200万至300万人的生命(不包括COVID)。针对疫苗可预防的儿童疾病的疫苗的开发是儿童死亡率下降的关键驱动力儿童死亡.
尽管这是一个如此重要的主题,但令人惊讶的是,缺乏关于哪些国家有强制性疫苗政策的信息,而且一个国家的国家免疫计划中最常见的强制性疫苗是儿童疫苗。
在这篇文章中,我们提出了一个新的全球数据集,它着眼于世界各地的儿童疫苗接种政策。
8.7世界各地的儿童疫苗接种政策有何不同?
我们最近制定了全球强制性儿童疫苗政策,因为它们正成为各国政府试图解决疫苗接种率低问题的日益重要的政策干预手段。48
“强制”和“授权”这两个词在不同国家有着完全不同的含义。虽然这一术语被广泛使用,但其定义却很模糊。49强制要求为某种目的接种疫苗,最常见的是与儿童入学有关。虽然定义上的分歧仍然存在,但更好地理解各国的政策以及推动政策随时间变化的原因仍然很重要。
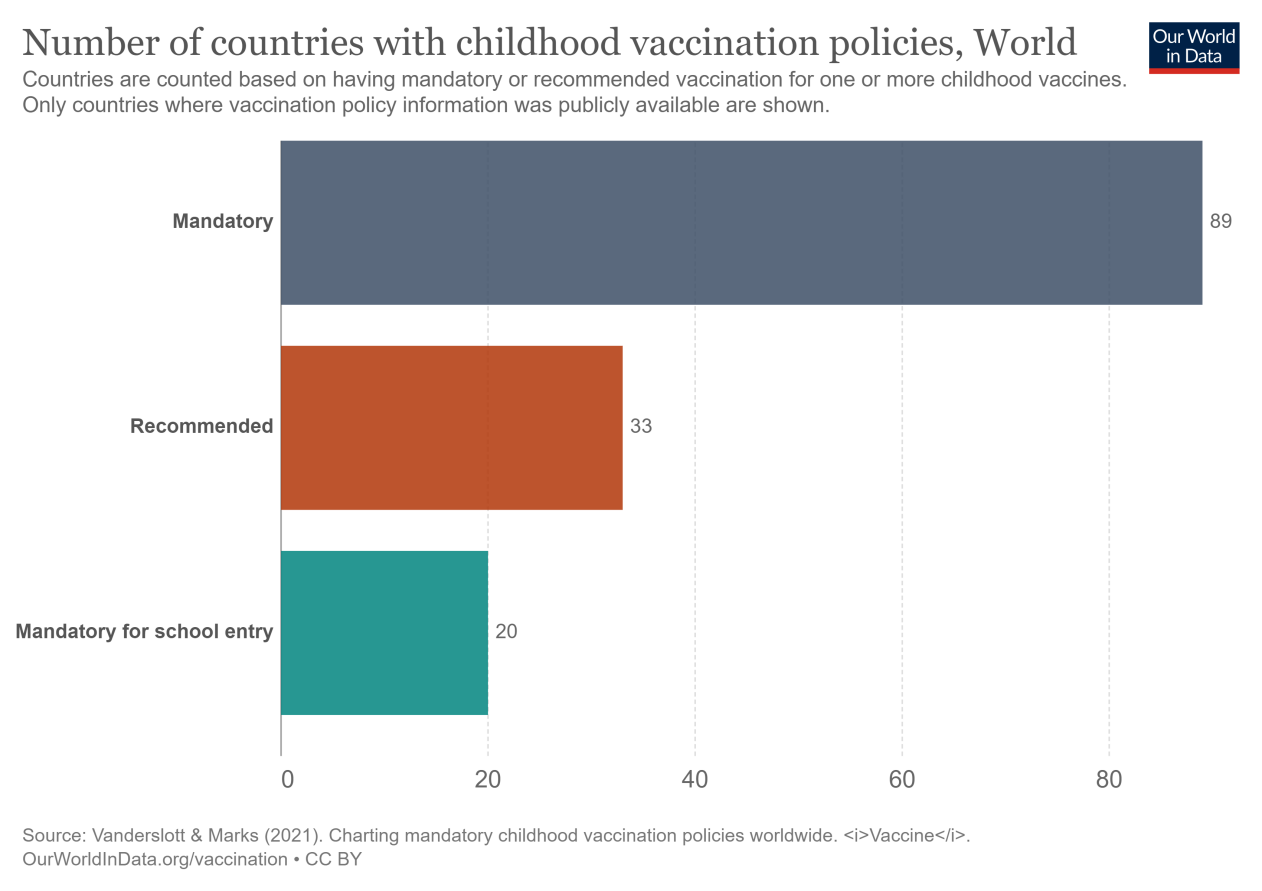
我们的列表显示了一个国家是否有针对一种或多种疫苗的强制性疫苗接种政策,以及强制要求的严格程度,分为三个级别:强制性、入学强制性或推荐性。儿童疫苗包括预防以下疾病的疫苗麻疹,腮腺炎,风疹,白喉、破伤风、百日咳, 脊髓灰质炎、狂犬病、乙型肝炎、轮状病毒, B型流感嗜血杆菌,以及肺结核–其中一些作为联合疫苗使用。如果一个国家强制要求至少一种疫苗,我们将该国归类为具有强制政策。
地图中显示了世界各地疫苗接种政策的差异。通过覆盖149个国家,我们可以发现一些趋势,这些趋势围绕着疫苗在哪里和为什么是强制性的。
注意:这是一个依靠众包来记录政策变化的实时数据集。如果您了解任何国家的任何新政策或政策变化,请务必联系:Samantha.vanderslott @ pediatrics.ox.AC.uk。

8.8强制疫苗接种政策因地区而异?
我们发现,评估世卫组织地区的政策——欧洲、美洲、西太平洋、非洲和东地中海——是分解我们对全球政策分析的有用方法。
在图表中,您可以看到具有特定政策授权的国家数量的细分。您可以使用交互式图表上的“更改区域”开关按区域查看。
欧洲混合了强制政策和推荐政策。但大多数欧洲国家——28个国家中的16个——没有强制接种疫苗。19世纪初,欧洲国家是第一批强制接种天花疫苗的国家之一泰国(Thailand)世纪,这也导致了提前推后。早期引入和早期推回,以及当今促进公民和卫生当局之间相互信任和责任的方法,可能是许多欧洲国家经常建议而不是强制接种疫苗的部分原因。50前苏联(苏维埃社会主义共和国联盟)或受东欧集团影响的国家以前有强制性疫苗接种,许多国家在后苏联时代保留了这一政策。
美洲的大多数国家——35个国家中的29个——都强制接种疫苗。在美国,疫苗接种由各州管理,尽管在所有的州都是强制入学的。在加拿大,只有三个省制定了适用于入学儿童的强制性疫苗接种政策。
在西太平洋地区,强制性政策的变化是双向的。一些国家如新加坡已经转向强制接种疫苗,而其他国家如韩国在1999年从强制疫苗过渡到推荐疫苗。对其他国家来说,强制性政策更加模糊。在中国,尽管文献中多次提到这种说法,但没有证据表明有具体的立法要求接种疫苗。51
很难获得关于非洲各国疫苗接种政策的信息,这表明该区域缺乏具体的政策。然而,我们发现的政策是强制接种疫苗。
东地中海地区的大多数国家都有强制性疫苗。以色列是一个例外,它只建议根据国家免疫技术咨询小组概述的疫苗接种计划进行疫苗接种。
东南亚有一些国家实行强制性疫苗接种。印度与其他大国相似,在邦一级有不同的强制性疫苗接种政策。最后,我们注意到有些国家在次国家一级有强制性政策,如加拿大各省、印度和澳大利亚各州,但我们根据国家政策对这些国家进行了分类,这些政策覆盖了全国大部分地区。
8.9是什么推动了强制性疫苗接种的引入?
总的来说,我们发现最近疫情的发生是引入强制性疫苗接种的主要因素,特别是对欧洲的高收入和中高收入国家。例如,在大规模爆发后,德国在2020年强制学校和日托机构接种麻疹疫苗。52类似地,在2014年至2015年麻疹爆发后,塞尔维亚通过引入更严厉的惩罚措施,收紧了强制性疫苗接种法律。53可以详细研究麻疹报告病例的趋势这里.
其次,由于缺乏其他政策选择,许多低收入和中低收入国家采取了强制性疫苗接种政策。尽管如此,由于疫苗供应、交付和获取方面的问题,许多国家仍未达到目标接种率。例如,在圭亚那,疫苗接种是强制性的,但疫苗接种的覆盖面受到供应链管理的阻碍,无法保持一致的储存温度和冷冻敏感疫苗的分发。54在尼日利亚,疫苗接种是强制性的,一些州已经颁布立法,将拒绝接种疫苗定为犯罪。然而,正如Onyemelukwe (2016)所指出的,疫苗的有效分发和吸收存在着结构、后勤、政治、系统、宗教和文化障碍,从冷链问题到腐败和安全问题。55因此,疫苗接种在政策上与实践上往往存在差异。
这些发现将有助于决策者考虑强制性疫苗接种的优点:
1)在过去,疾病(如麻疹)的爆发导致了强制性疫苗的引入,即使在以前建议所有疫苗接种的国家也是如此;
2)强制接种疫苗不应是唯一的政策工具,但需要与疫苗的可获得性和可用性相结合;
3)这不仅仅是一个是否强制接种疫苗的问题,而是如何强制接种、人们是否会遵守以及对国家与公民关系的影响。
总之,强制接种疫苗必须慎重考虑。一个国家过去在强制接种方面的经验、疫苗接种服务、执行能力、公众态度以及疾病爆发的现状都将在是否应该引入强制接种疫苗方面发挥作用。
9.覆盖面、影响和潜力
9.1通过接种疫苗可以预防的疾病
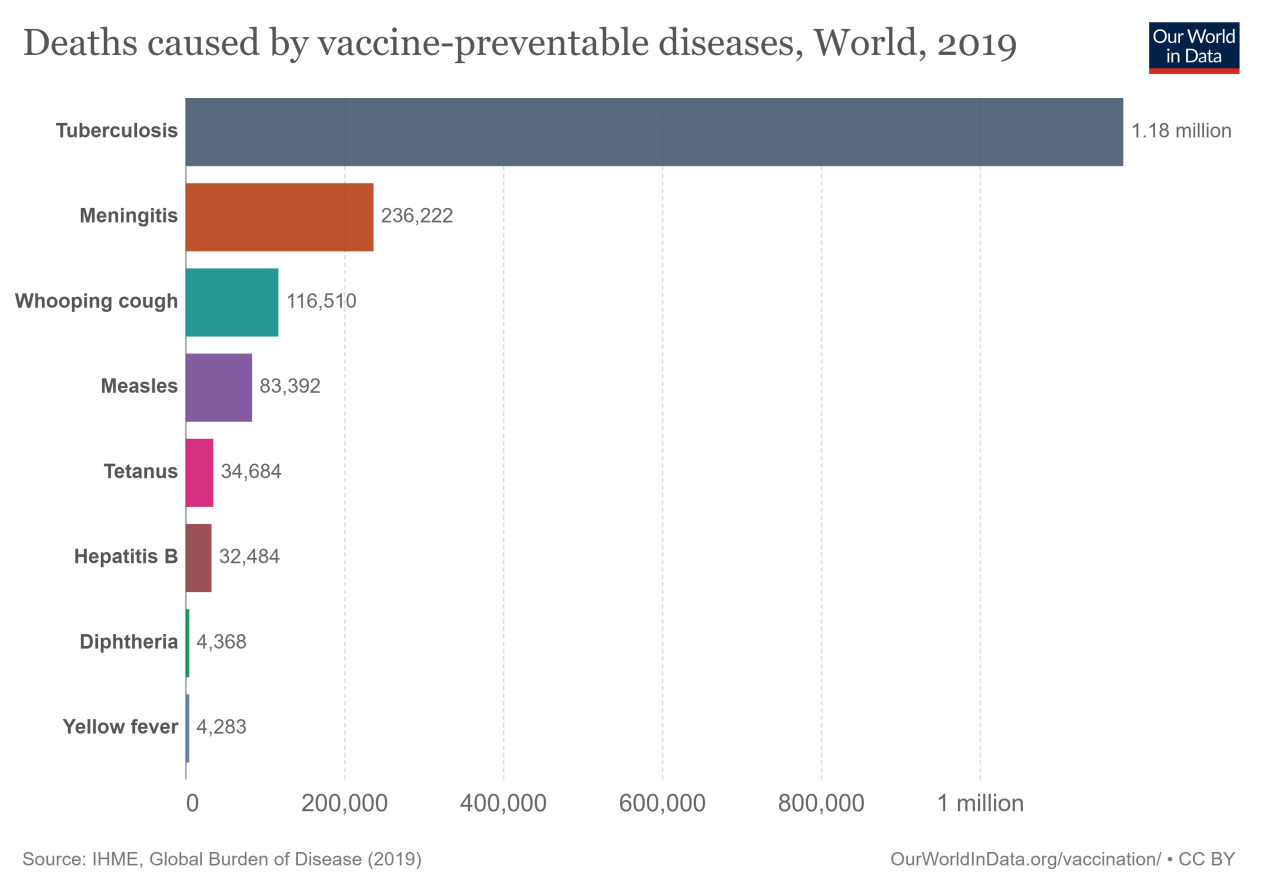
图表显示了一些最常见和最严重的疫苗可预防疾病导致的全球死亡人数。
现在有更多的疾病有疫苗可用,甚至更多的疫苗正在研发中。世卫组织公布了26种疾病有哪些疫苗可用–包括日本脑炎、肺炎球菌疾病、水痘/水痘、人乳头瘤病毒、甲型肝炎和轮状病毒。
9.2白喉、破伤风和百日咳疫苗
白喉、破伤风和百日咳都是细菌性疾病,通常使用针对这三种疾病的联合疫苗。
- 白喉主要感染咽喉和上呼吸道,在5-10%的病例中是致命的。
- 破伤风不会在人与人之间传播,而是通过生活在土壤和动物肠道中的细菌孢子传播。这些细菌通过伤口进入体内,并释放出一种影响神经的毒素,导致肌肉僵硬和痉挛。
- 百日咳是一种传染性极强的呼吸道疾病,俗称百日咳。患有百日咳的儿童往往会咳嗽4到8周,但死亡率最高的是幼儿。为卫生工作者和孕妇接种疫苗是预防太小而不能接种疫苗的婴儿患病的最有效策略。
图表显示了世界各地儿童白喉、破伤风、百日咳、破伤风三联疫苗免疫覆盖率的长期进展。
世卫组织报告2017年,全球85%的婴儿(1.165亿婴儿)接种了3剂白喉-破伤风-百日咳疫苗(DTP3)。同样在2016年,130个国家的百白破三联疫苗覆盖率达到至少90%。
如果我们看看按世界区域分列的时间变化南亚尤其突出。今天,85%的一岁儿童接种了疫苗,而在1980年,这一数字仅为6%。
在每个国家内,疫苗接种覆盖率可能有很大差异。这世卫组织报道在所有地区,最富有的20%城市家庭的儿童比最贫穷的20%家庭的儿童更有可能获得免疫。
然而,一些国家落在了后面。乌克兰表现突出,其2015年的百白破疫苗接种率特别低,为23%,低于1999年的98%。艾德·霍尔特(ed Holt)2013年为《柳叶刀》(the Lancet)撰写的文章将这一下降归因于:“公众对疫苗接种的不信任、疫苗供应不足以及卫生系统的腐败”。因此,乌克兰正受到影响疫苗接种率的多种因素的综合影响,包括公众态度和系统性的接种问题。此外,2014年以来的动荡和俄罗斯的军事干预很可能使情况恶化。如今,只有赤道几内亚的接种率更低,为16%。如同人权观察观察到这个国家的财富很少用于满足公民的需求。
尼日利亚疫苗接种不足的儿童人数居高不下,其中340万儿童没有接种百白破三联疫苗(印度为290万)。
9.3麻疹疫苗
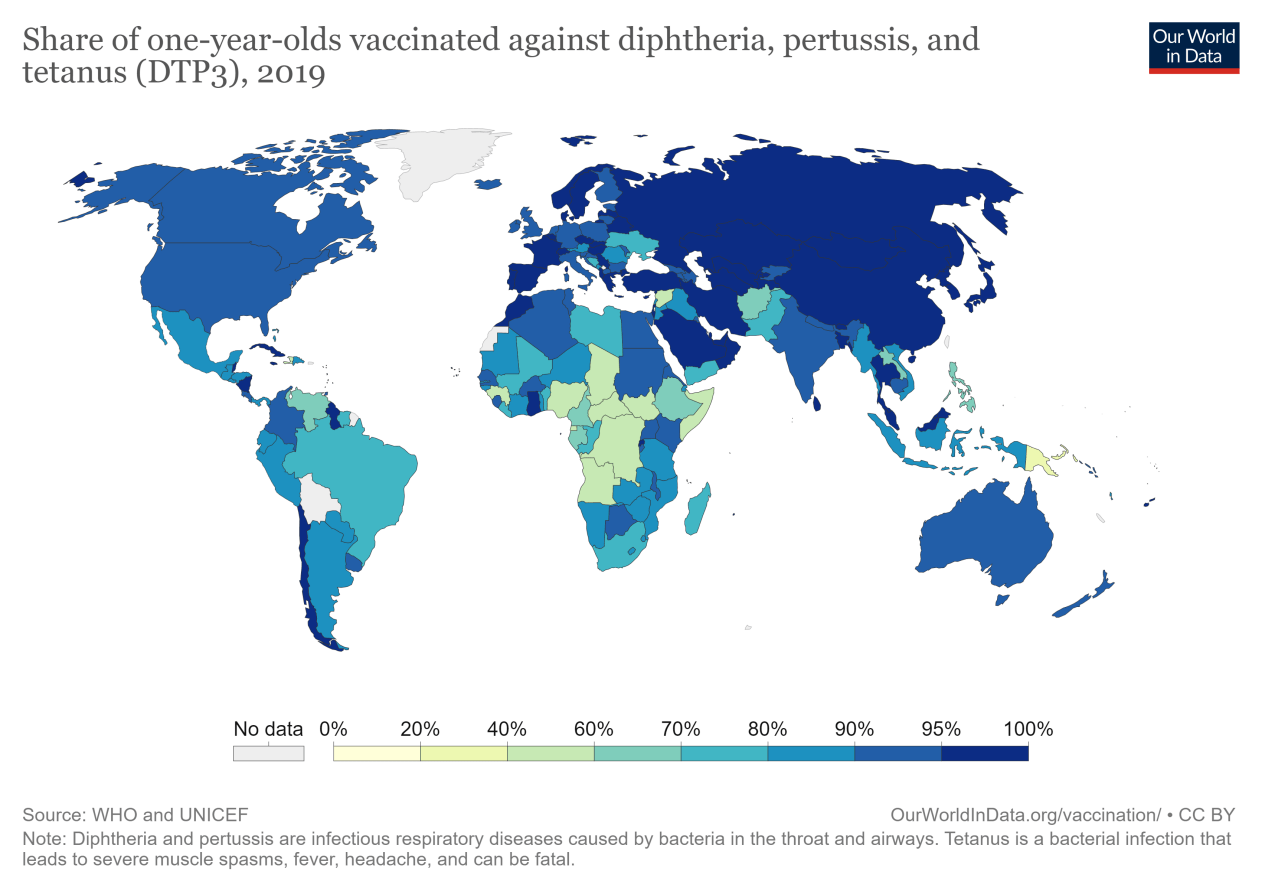
麻疹是一种高度传染性的病毒引起的疾病,尽管有安全有效的疫苗可用,但全球仍有数千人感染。每年约有90,000人死于麻疹,其中绝大多数(87%)是5岁以下的儿童。麻疹疫苗接种导致2000年至2016年间麻疹死亡率下降了84%。
麻疹疫苗是在1963年开发的。1983年——有全球数据的第一年——只有二分之一的儿童接种了麻疹疫苗。最新数据显示,这一份额已从2000年的72%上升至全球的85%。
撒哈拉以南非洲地区的麻疹疫苗接种率最低,同时还有饱受冲突和不稳定的国家(如叙利亚、阿富汗和伊拉克)。但一些太平洋岛屿——如巴布亚新几内亚和瓦努阿图——表现不佳。
今天(2014年的数据)每年有1.143亿儿童接种麻疹疫苗,平均每天313,071名儿童。
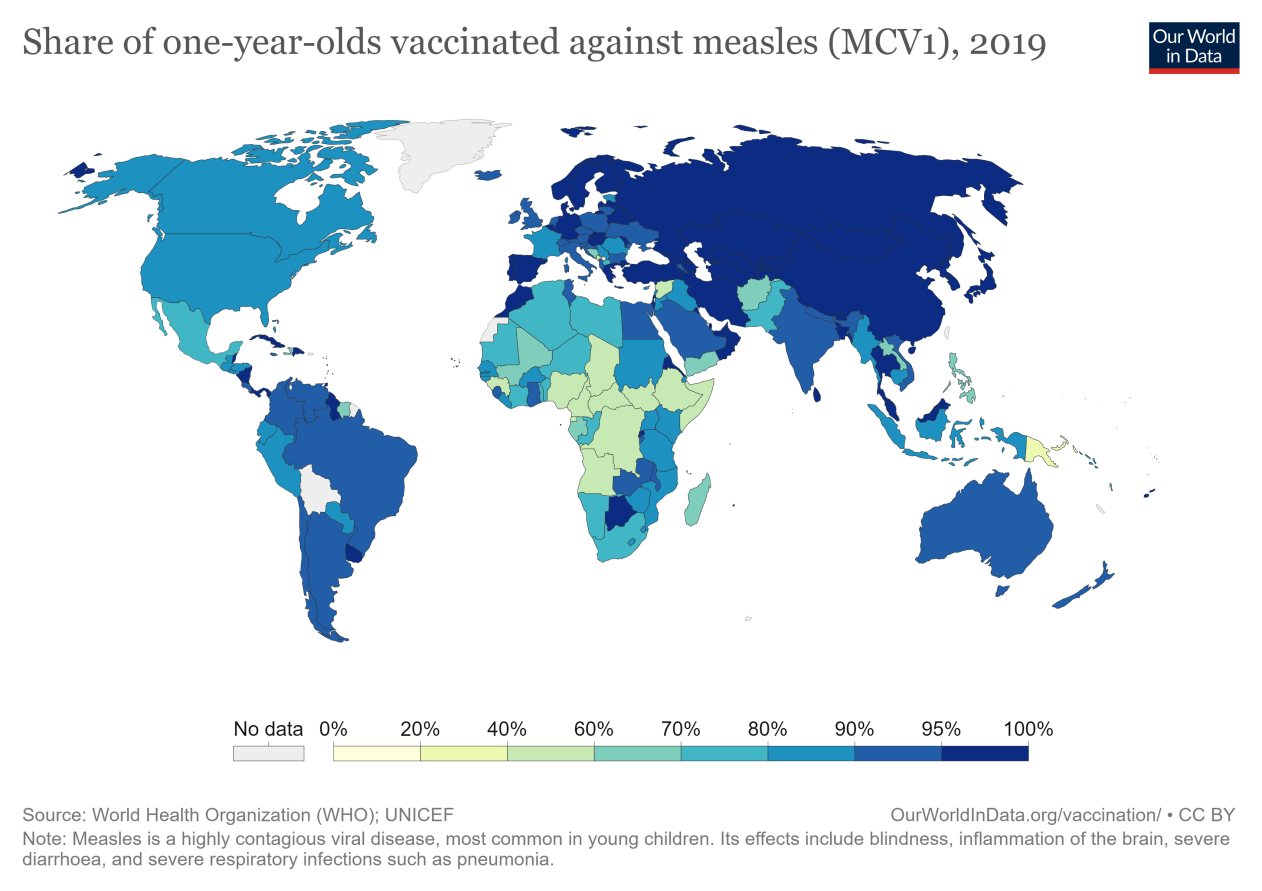
9.3.1第二剂麻疹疫苗提供更大的保护
截至2018年,世卫组织估计已有171个国家将第二剂疫苗纳入常规免疫接种。更高水平的保护需要两剂。
目前全球平均水平是67%。南非的覆盖率最低,撒哈拉以南非洲的许多国家仍未将疫苗纳入其免疫覆盖范围。
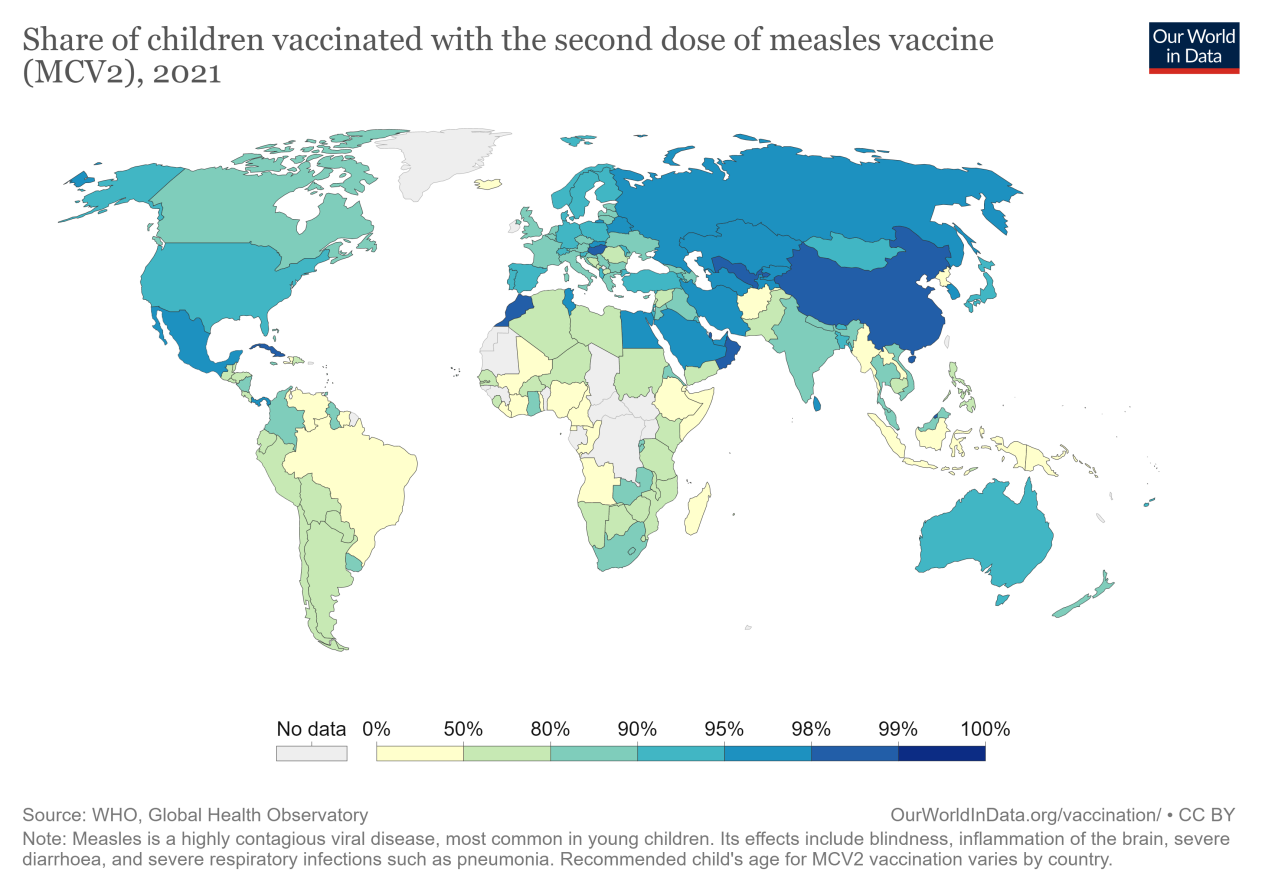
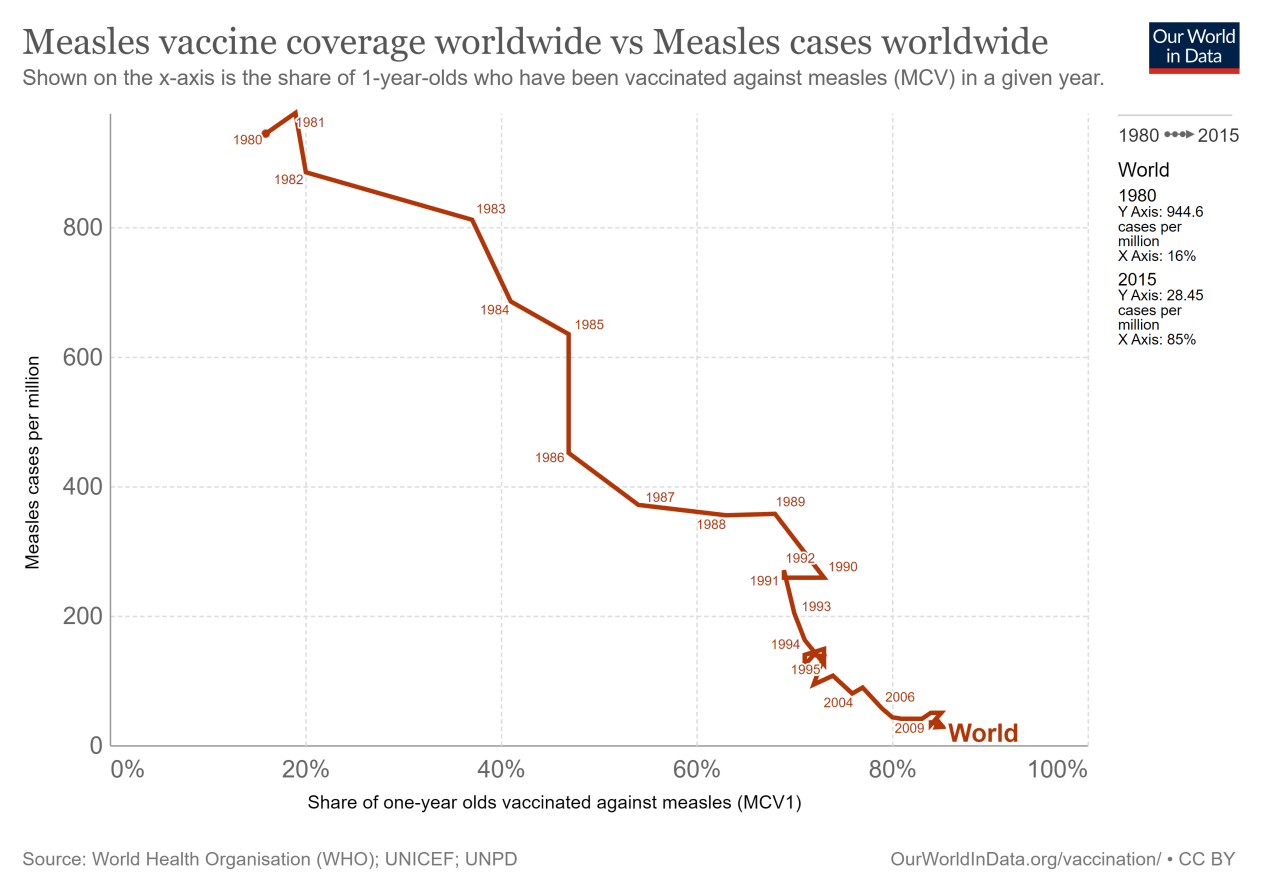
9.3.2全球麻疹发病率下降
一岁儿童全球疫苗接种覆盖率的增加以及该疾病报告病例的同时下降;从全球每百万人近1000例到每百万人28例。这意味着减少了33倍。
随着时间的推移,各个国家的变化情况见这种视觉化.
9.4轮状病毒疫苗
第一个广泛使用的轮状病毒疫苗于2006年在美国获得批准。今天,世界卫生组织推荐使用四种口服轮状病毒疫苗:Rotarix、RotaTeq、RotaSiil和Rotavac。
Rotarix和RotaTeq是最广泛使用的,两者在临床试验中都显示出抗轮状病毒感染的良好疗效。
自从轮状病毒疫苗被批准使用以来,它们对减少轮状病毒相关的死亡有显著的影响。根据2018年发表的一项研究,轮状病毒疫苗的使用在2016年防止了全球约28,900名儿童死亡。然而,如图表所示,全面使用疫苗——即全球100%的覆盖率——本可以防止额外的83,200例死亡。这意味着,即使按照目前的有效率,2016年53%的5岁以下儿童轮状病毒死亡可以通过全面疫苗覆盖来避免。
除了拯救生命,轮状病毒疫苗也减轻了医疗系统的负担。2008年至2016年间,轮状病毒疫苗的引入使腹泻相关的住院人数平均减少了40%。
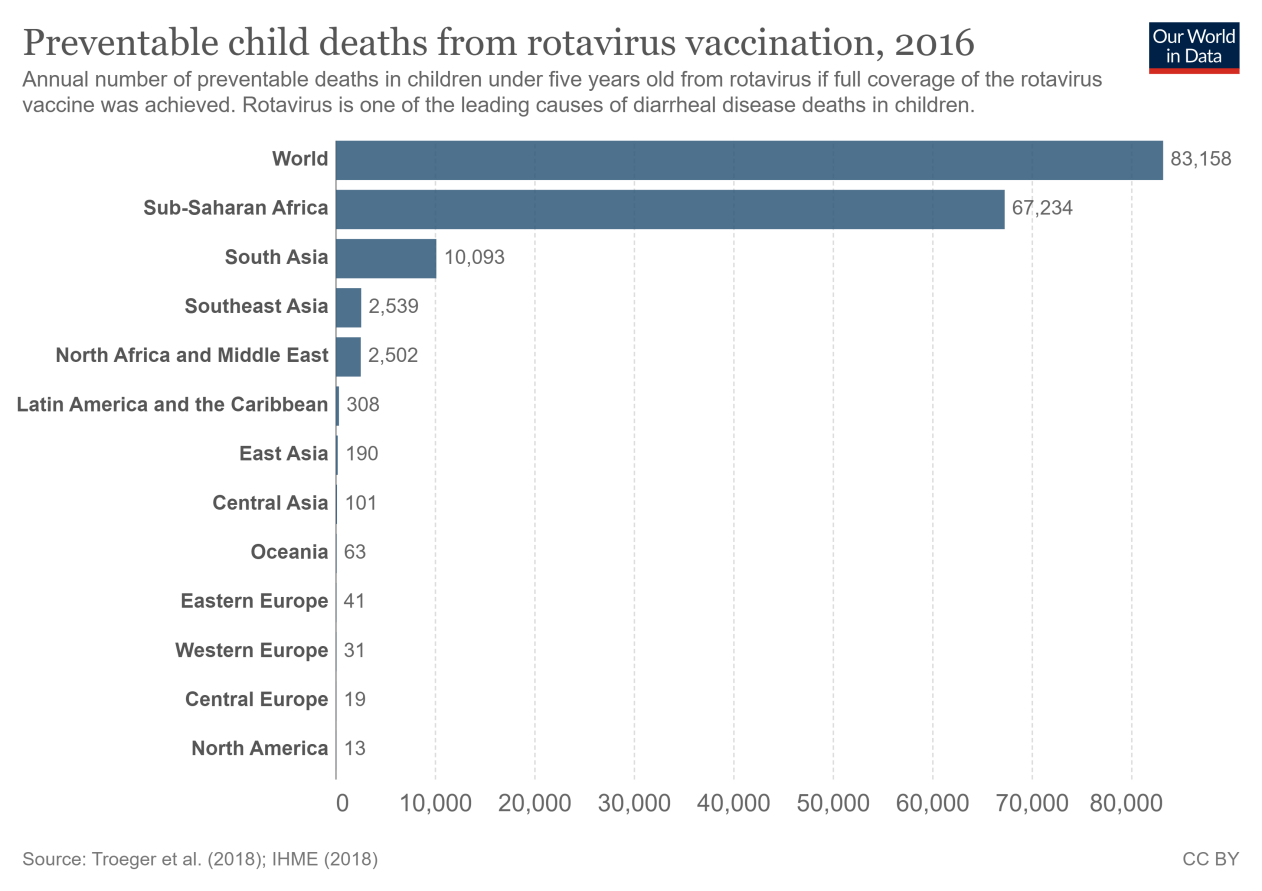
9.4.1轮状病毒疫苗可以拯救更多儿童的生命
如果拯救更多儿童生命的余地如此之大,那么这些儿童仍在死亡的原因是什么?
要发挥轮状病毒疫苗的全部潜力,有两个关键障碍:免疫率和疫苗在特定地区的效力。
9.4.2免疫接种率仍然太低
根据世卫组织的数据,截至2018年底,101个国家正在使用轮状病毒疫苗。引入疫苗的主要驱动力是腹泻疾病的负担、资金的可获得性以及对疫苗有利的环境。
疫苗只给儿童接种——建议接种应在出生后15周开始,并在第32周结束。然而,全球覆盖率仍然很低:据估计,2018年只有35%的一岁以下儿童接种了疫苗。
该图显示了世卫组织对一岁儿童接种全部推荐剂量疫苗(Rotarix疫苗两次免疫或RotaTeq疫苗三次免疫)比例的估计。对于许多数据覆盖率低的国家,预计接受疫苗接种的婴儿比例非常低。然而,一些国家的免疫接种率确实迅速上升。在仅仅几年的时间里,包括苏丹、马拉维和冈比亚将免疫接种率从不到10%提高到80-95%。
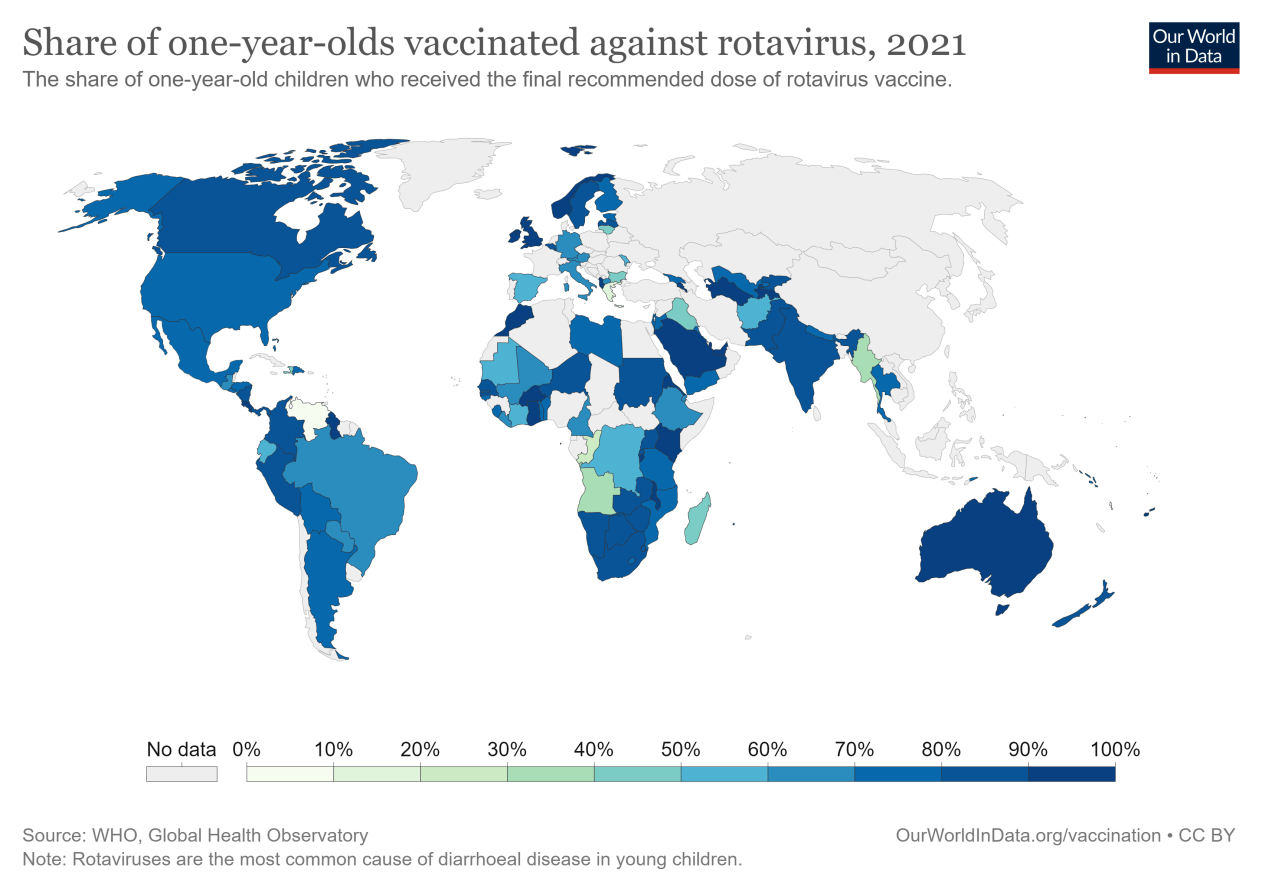
9.4.3疫苗效力因地区而异
因为大多数轮状病毒病例发生在撒哈拉以南非洲轮状病毒感染的死亡率也是最高的在这一地区,提高和保持高免疫覆盖率是至关重要的。然而,除了为需要的人提供疫苗之外,我们还需要努力提高其效力。
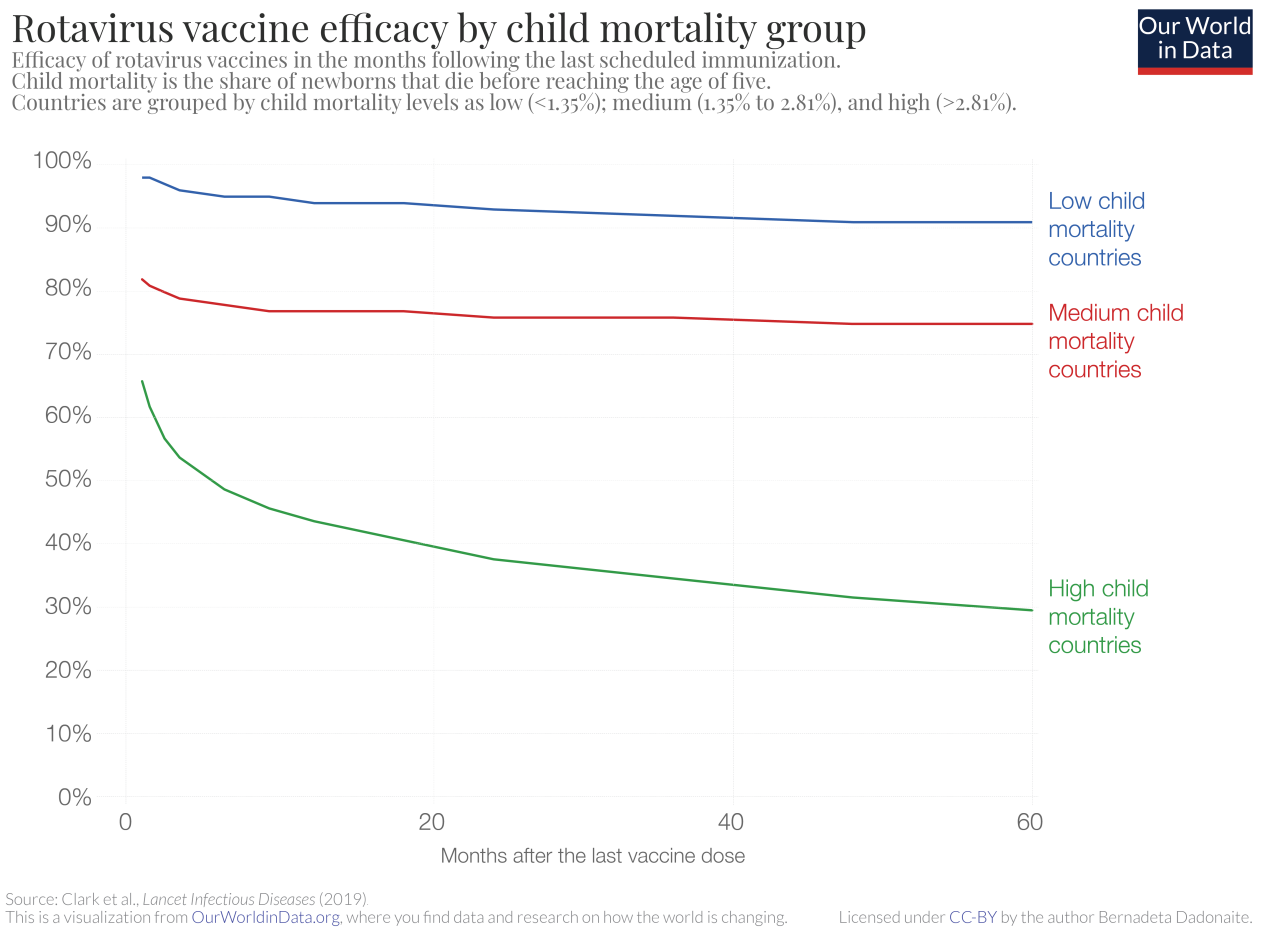
轮状病毒疫苗的疫苗效力被定义为接种疫苗的儿童组与未接种疫苗的儿童组相比,腹泻发病率降低的百分比。众所周知,轮状病毒疫苗的效力在所有国家并不相同,在儿童死亡率高的国家,疫苗的效力要低得多。
来自克拉克等人研究了口服轮状病毒活疫苗在不同国家接种后的效果变化。图表显示,在儿童死亡率高的国家,不仅疫苗的即时效力较低——儿童死亡率低的国家为98%,儿童死亡率高的国家为66%——而且随着时间的推移,儿童死亡率高的国家的疫苗效力下降更快。
接种疫苗五年后,轮状病毒疫苗在儿童死亡率低的国家将患腹泻的几率降低了90%,在死亡率高的国家仅降低了30%。
下表显示了轮状病毒疫苗在预防严重腹泻和减少不同地区5岁以下儿童因腹泻住院方面的效果。
在高收入国家,轮状病毒疫苗接种已被证明可将严重轮状病毒腹泻病例减少91%,住院率减少94%。在东亚和拉丁美洲,有效率较低,但仍然很高——分别预防了88%和80%的严重腹泻病例。然而,在南亚和撒哈拉以南非洲的有效性明显较低,仅减少约一半病例的严重腹泻。
对疫苗不同反应的原因还不完全清楚。
低收入国家儿童对口服轮状病毒疫苗的肠道反应可能不同。这可能是由多种原因造成的,包括微量营养素缺乏症接种疫苗前暴露于某些病原体,以及存在慢性疾病,例如疟疾或者艾滋病病毒。总的来说,对活疫苗的肠道反应差意味着疫苗的效力降低。考虑到上述各点,有几种干预措施可以进一步增加轮状病毒疫苗的益处。除了扩大疫苗覆盖面之外,改善(婴儿和母亲的)营养健康以及改善卫生和环境卫生条件(以降低破坏性病原体的流行率)也会对疫苗效力产生积极影响。
我们仍处于轮状病毒疫苗使用的早期阶段。尽管疫苗已经带来了巨大的好处,但它还可以走得更远。提高疫苗接种覆盖率,特别是在撒哈拉以南非洲和南亚地区,是持续降低儿童腹泻死亡率的关键。即使在疫苗效力处于中等水平的情况下,每年也可以防止大量额外的儿童死亡。上面显示可预防死亡人数的柱状图表明了扩大疫苗覆盖范围拯救更多生命的潜力。这已经考虑到了疫苗有效性的地区差异。
除了扩大覆盖面之外,提高疫苗的有效性将进一步解决导致死亡的主要原因之一。
| 结果 | 地区 | 疫苗效力 |
|---|---|---|
| 严重轮状病毒腹泻 | 发达的 | 91% |
| 东亚和东南亚 | 88% | |
| 拉丁美洲和加勒比 | 80% | |
| 南亚 | 50% | |
| 撒哈拉以南非洲 | 46% | |
| 轮状病毒感染住院 | 发达的 | 94% |
| 东亚和东南亚 | 94% | |
| 拉丁美洲和加勒比 | 84% | |
| 撒哈拉以南非洲 | 58% |
9.5肺炎球菌疫苗
我们有许多方法可以减少死于肺炎的儿童人数,包括消除以下主要风险因素营养不良和空气污染,并提供更好的获得治疗。
但是我们有另一个非常有效的干预措施,疫苗对抗导致儿童肺炎的主要病原体。
肺炎链球菌是5岁以下儿童肺炎的主要原因——2016年,它导致了52%的儿童致命肺炎病例。肺炎球菌疫苗是针对以下目标的疫苗南肺炎细菌。在这里,我们看看他们的有效性,以及我们如何能够最大限度地增加他们挽救的儿童数量。
9.5.1肺炎球菌疫苗的覆盖率仍然很低
自2007年世界卫生组织开始建议将肺炎球菌疫苗纳入国家儿童免疫规划以来,使用该疫苗的国家数量一直在逐步增加。
但在许多国家,肺炎球菌疫苗的覆盖率仍然很低。在印度和尼日利亚,这两个国家在2019年因肺炎死亡的儿童中,分别只有44%和58%的一岁儿童接种了疫苗。
2018年,全球不到一半(47%)的一岁儿童接受了全程肺炎球菌疫苗接种。这意味着,5500万本可以受到疫苗保护的儿童仍然没有接种疫苗——对于一种不仅可以预防肺炎(儿童死亡的主要原因)而且可以预防一系列其他疾病(如下所述)的疫苗来说,这是一个惊人的高数字。
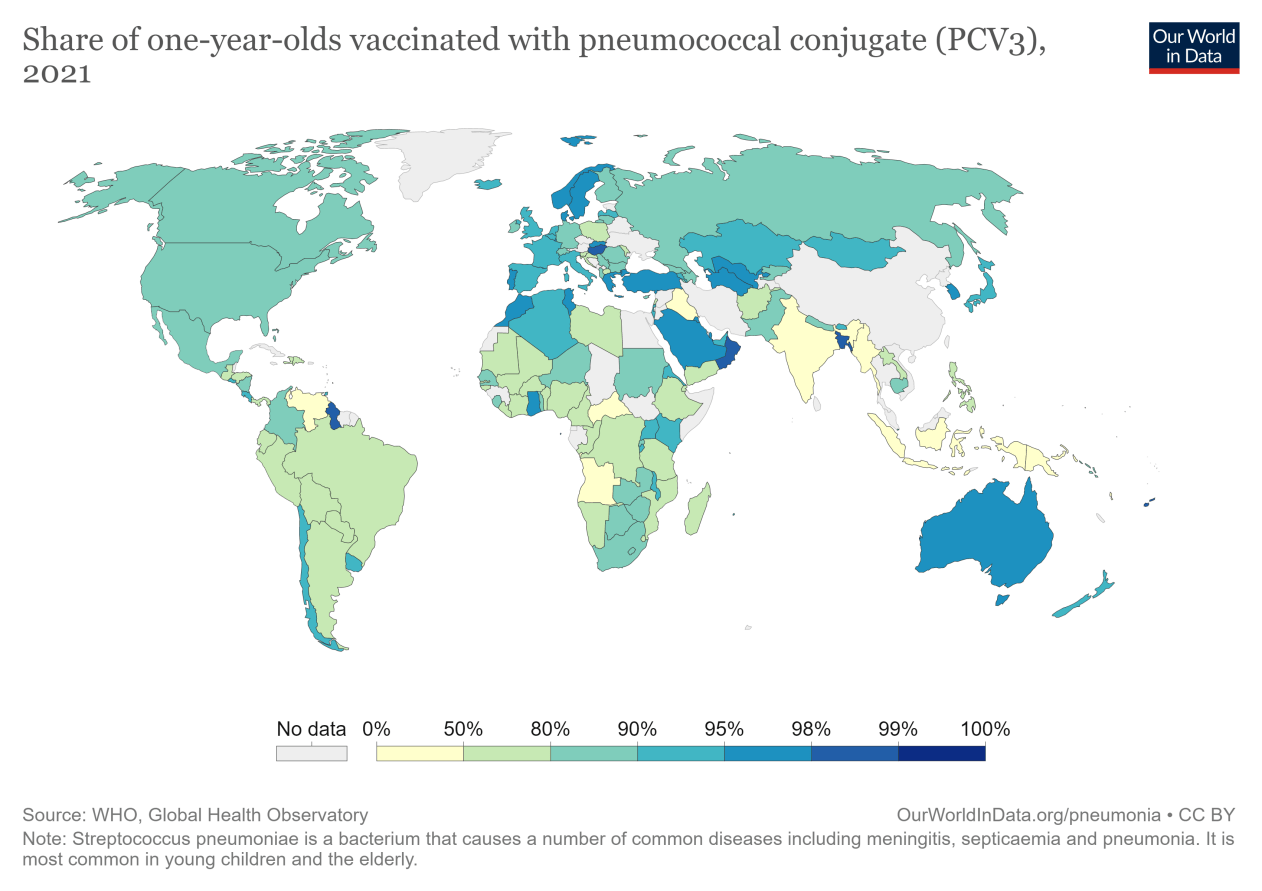
9.5.2肺炎球菌疫苗是如何发挥作用的?
肺炎链球菌通常简称为肺炎球菌,是一种常见于健康人上呼吸道的细菌。一般来说,这种细菌是无害的,或者会引起较轻的疾病,如支气管炎、鼻窦炎和耳部感染。肺炎球菌疫苗对这些较轻的疾病也有效,但重要的是还能防止所谓的肺炎球菌侵袭性疾病(PID)。当肺炎球菌从定居上呼吸道移动到通常无菌的定居部位,如血液、脑脊液或胸膜腔(肺周围充满液体的空间)时,就会发生PID。细菌入侵导致威胁生命的疾病,如败血症、脑膜炎和重症肺炎。
有两种类型的肺炎球菌疫苗可供使用:结合多糖肺炎球菌疫苗(PCV)和非结合多糖肺炎球菌疫苗(PPSV)。这两种疫苗都旨在引发针对多种肺炎球菌血清型的免疫反应,这些血清型由对细菌表面发现的糖的不同免疫反应来定义。为了广泛有效,疫苗需要针对一定数量的这些肺炎球菌血清型进行保护,但没有必要包括所有可能的血清型,因为只有有限的子集负责70%-80%的侵袭性肺炎球菌疾病。然而,正如我们将在后面讨论的,记住这种不同的肺炎球菌血清型是很重要的,因为随着疫苗覆盖率的增加,我们可能会看到包含疫苗的血清型被不太占优势的血清型所取代,这意味着将需要新的疫苗版本。
虽然有两种类型的肺炎球菌疫苗可用,但对于两岁以下的儿童,仅推荐使用结合型(即PCV)疫苗,因为非结合型(即PPSV)疫苗在这么小的年龄无效。
9.5.3肺炎球菌疫苗的效果如何?
在临床试验中,PCV在减少由疫苗制剂中包含的细菌血清型引起的侵袭性肺炎球菌疾病方面显示出80%的功效。接种疫苗的儿童被诊断为肺炎的可能性降低27%,死于肺炎的可能性降低11%。
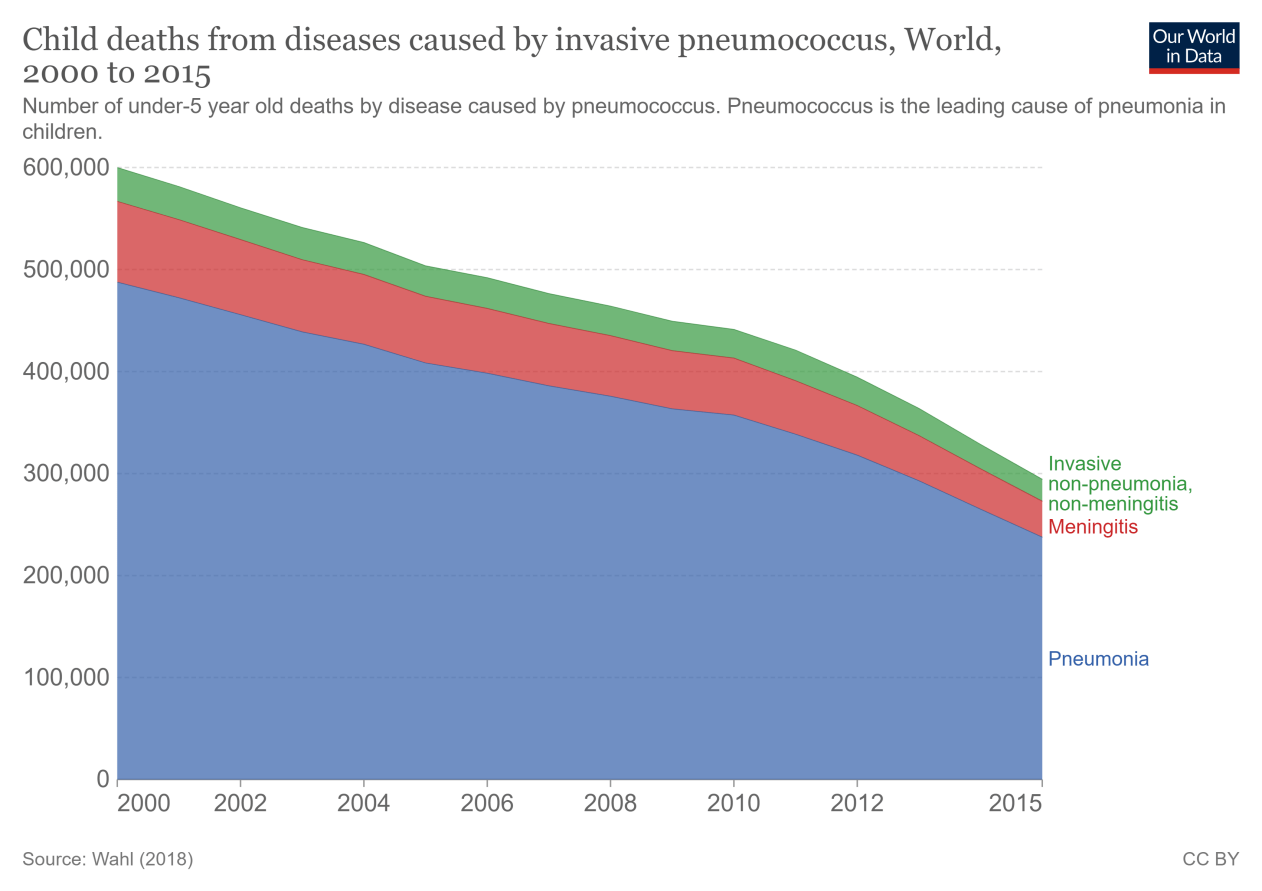
几项研究试图估计PCV疫苗已经挽救和可能挽救多少生命。一个柳叶刀研究得出结论,在2000年至2015年期间,在120个国家中,肺炎球菌导致的儿童死亡人数从60万下降到29.4万——下降了54%。这种下降主要归因于PCV疫苗:在此期间,据估计这些疫苗挽救了250,000名儿童的生命。这些死亡中的大多数是由肺炎引起的,但疫苗也防止了肺炎球菌脑膜炎和其他疾病的死亡。
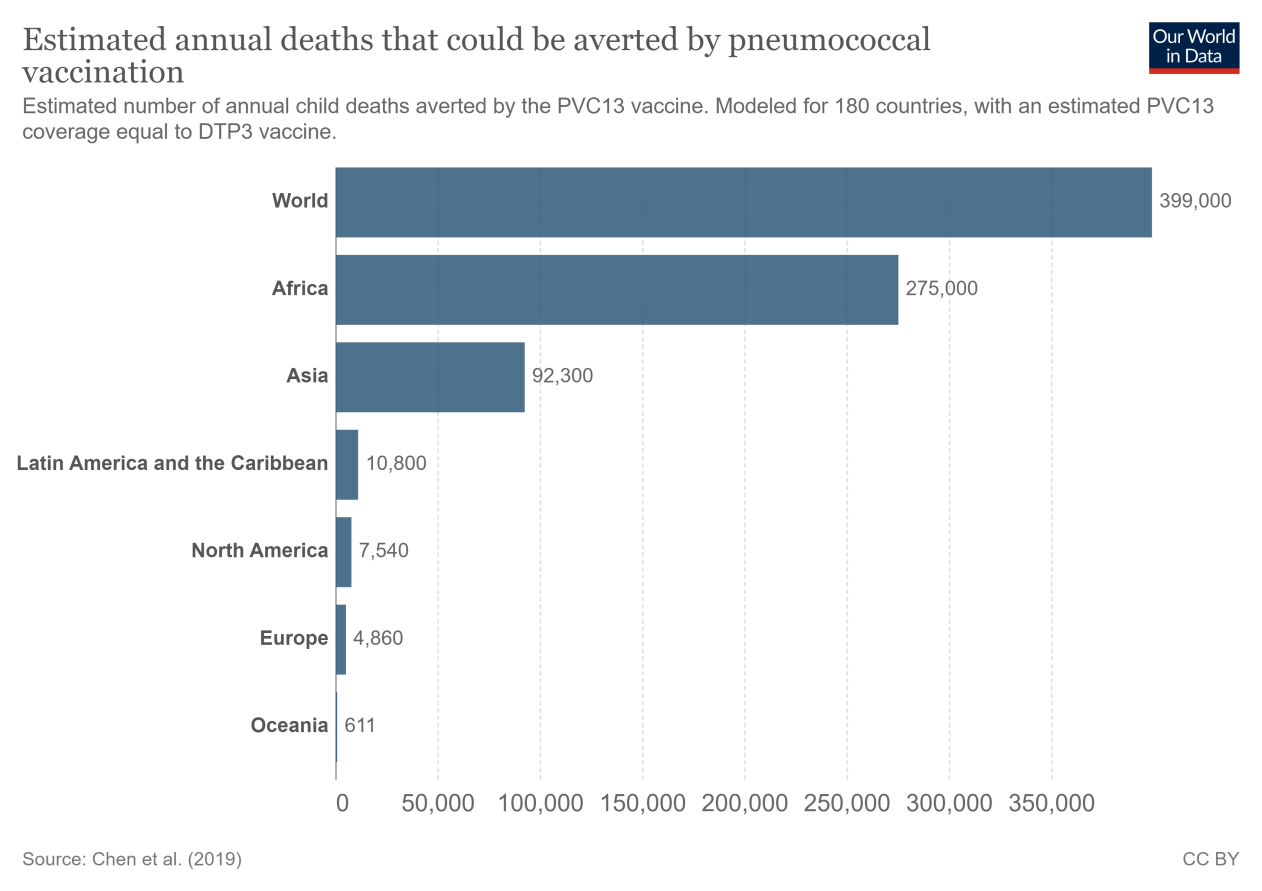
9.5.4肺炎球菌疫苗可以避免多少儿童死亡?
图表显示了对肺炎球菌疫苗潜在影响的估计。
它是基于最近发表在柳叶刀全球健康该杂志计算出,如果PCV疫苗覆盖率至少达到白喉、破伤风和百日咳疫苗接种399,000名5岁以下儿童的生命可以得到拯救。此外,研究人员估计每年可以避免5460万例肺炎发作。
这些数字估计了PCV疫苗接种相对于没有该疫苗的世界的影响——由于疫苗已经使用,这意味着这些生命中的一些已经被PVC疫苗接种所挽救。然而,在许多国家PCV疫苗接种率仍远低于DTP3疫苗接种率,表明我们还没有充分利用肺炎球菌疫苗的潜力。
9.5.5我们能做些什么来提高肺炎球菌疫苗的覆盖率和有效性?
如果我们想充分利用肺炎球菌疫苗的潜力,继续提高免疫覆盖率和在尚未使用PCV疫苗的国家引入PCV疫苗是非常重要的。
PCV疫苗是国家免疫规划中最昂贵的疫苗之一。价格从GAVI的每剂3.05美元不等,支持低收入国家到美国等高收入国家169美元。对于正在脱离GAVI支持的中低收入国家来说,未来疫苗接种费用的增加给国家卫生保健预算带来了相当大的压力。
但考虑到肺炎球菌疾病的高负担,即使价格很高,PCV疫苗也被认为是具有成本效益的,在低收入和中等收入国家的投资回报估计约为3。
PCV疫苗包括可能的肺炎球菌血清型的有限子集。已知肺炎球菌血清型的分布因国家而异,PCV疫苗包括全球最常见的疫苗。
哪些非疫苗血清型在特定国家最常见,可能会影响特定疫苗的潜在影响。然而,并非所有国家都收集血清型分布数据,因此对潜在影响的评估受到影响。值得注意的是,自从PCV疫苗引入以来,由不太常见的血清型引起的肺炎球菌侵袭性疾病发病率有所上升。这表明,通过降低疫苗包含血清型的流行率,疫苗无意中为非疫苗血清型提供了空间,对非疫苗血清型的效果不太好。这意味着,如果PCV的血清型配方没有被不断地重新评估,疫苗的有效性可能会随着时间的推移而降低。在未来,可能需要新版本的肺炎球菌疫苗,其不依赖于细菌血清型而更好地发挥作用。这种疫苗已经在开发中。
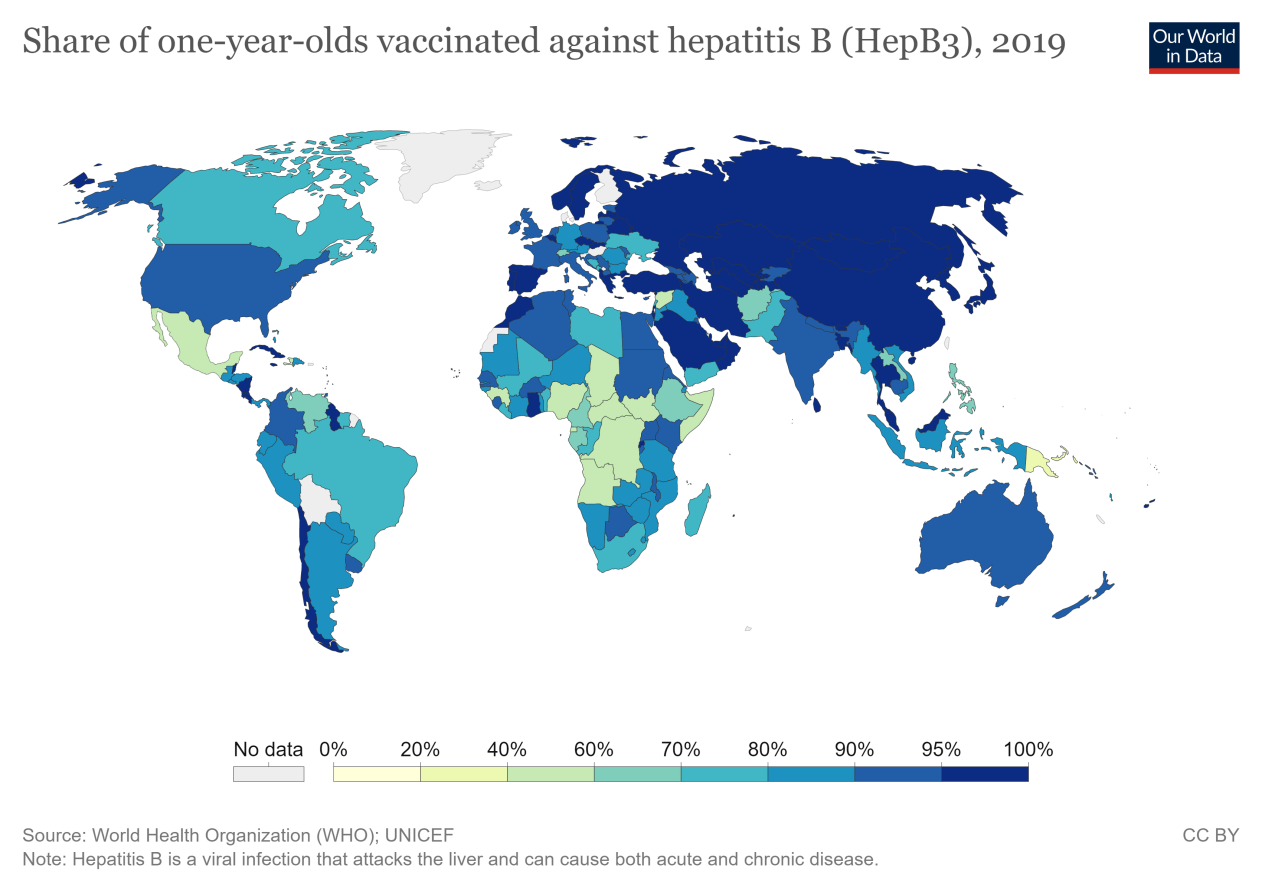
9.6 乙型肝炎疫苗
乙型肝炎(HepB)是一种高度传染性的病毒感染,攻击肝脏,并通过接触受感染者的血液或其他体液传播。据估计,每年约有100,000人死于乙型肝炎引起的慢性肝病。世卫组织建议所有婴儿应在出生后尽快接种第一剂疫苗,最好在24小时内。
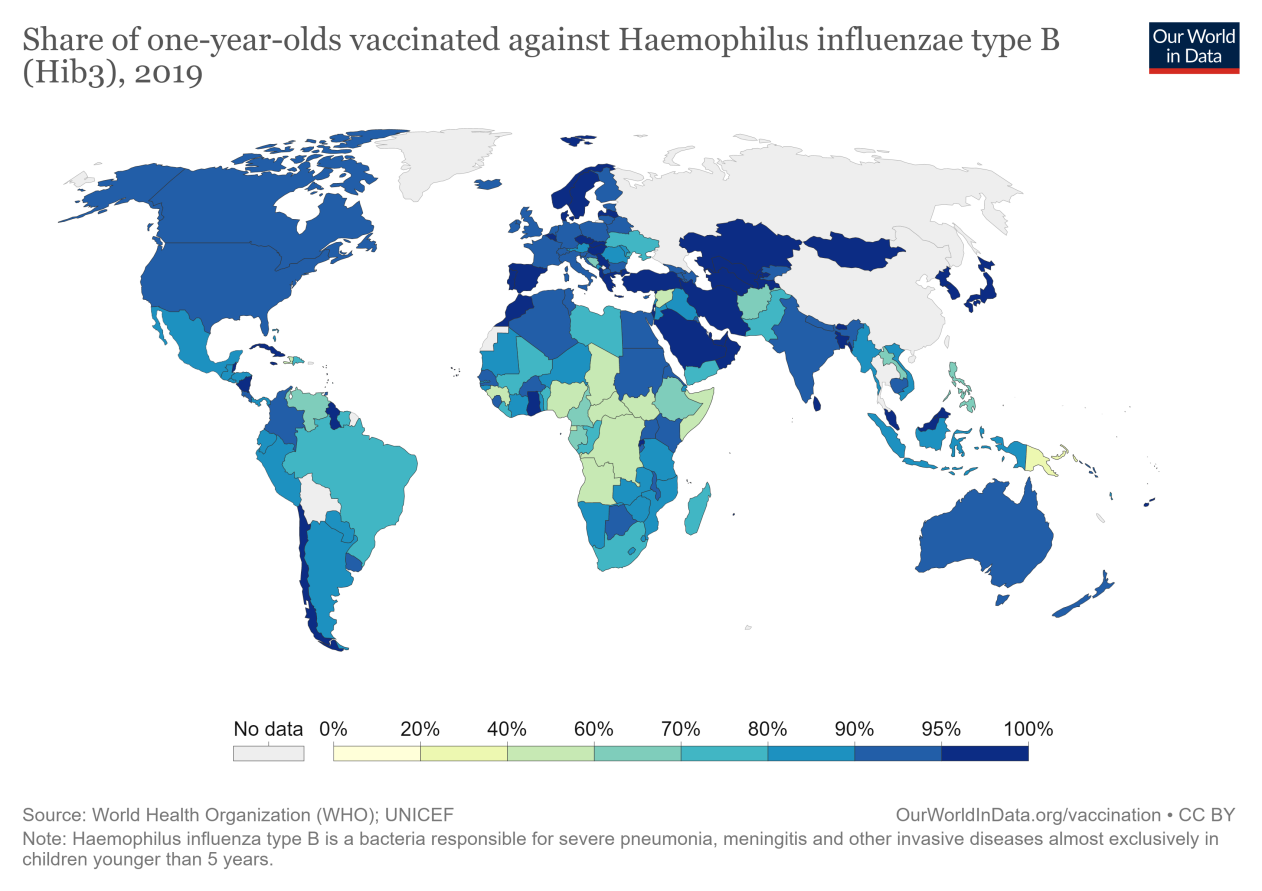
9.7 b型流感嗜血杆菌疫苗
b型流感嗜血杆菌(Hib)是一种细菌感染,可导致脑膜炎和肺炎,通过呼吸道从感染者传播到易感者。这里的图表显示了Hib疫苗接种的覆盖范围。
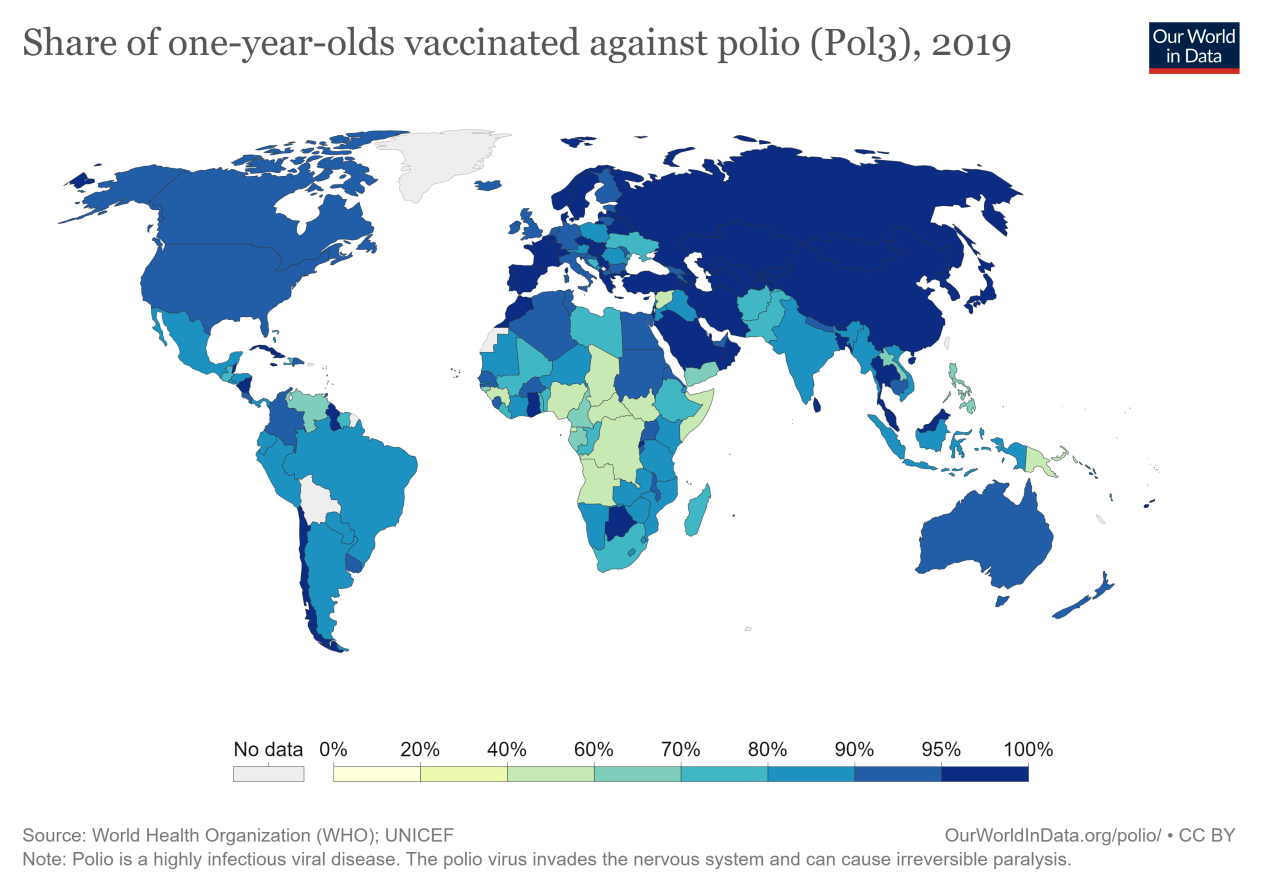
9.8脊髓灰质炎疫苗
脊髓灰质炎(IPV OPV)是一种高度传染性的病毒性疾病。一旦脊髓灰质炎病毒侵入神经系统,它可以在几小时内造成不可逆的瘫痪。脊髓灰质炎无法治愈,只能通过治疗来缓解症状。由于有了针对这种病毒的疫苗,世界正在根除这种疾病:上世纪80年代,每年有35万例麻痹性脊髓灰质炎病例,而2016年世界上只有42例。
9.9结核病疫苗(卡介苗)
一个多世纪前开发的卡介苗(BCG)是目前唯一可用的结核病疫苗。
将近40亿人接种了卡介苗——这使它成为世界上使用最广泛的疫苗。
卡介苗是基于一种减毒株牛型结核菌这是一种细菌,与结核分枝杆菌–导致结核病的病原体。20世纪20年代,卡介苗已经在比利时和法国进行了小规模试验,二战后,卡介苗的使用范围扩大到欧洲各地的儿童。20世纪50年代,世卫组织开始在全球范围内推荐使用卡介苗。
卡介苗可以有效地保护儿童和青少年免受严重形式的结核病和脑膜炎。然而,研究表明,疫苗提供的保护时间长短因研究人群而异:从英国的15年到阿拉斯加的50-60年。这种可变性的原因尚不清楚,但诸如用于免疫接种的不同疫苗种子菌株和已经暴露于其他分枝杆菌菌株的人群中已存在的免疫力等因素可能是重要的。
值得注意的是,卡介苗不能保护人们免受原发感染,也就是说,它不能防止人们已经感染 M. tuberculosis,肺结核首先感染的细菌。如果一个人已经被感染,卡介苗也不能防止潜伏结核的活化。因此,疫苗对预防结核分枝杆菌在人群中传播的作用有限。
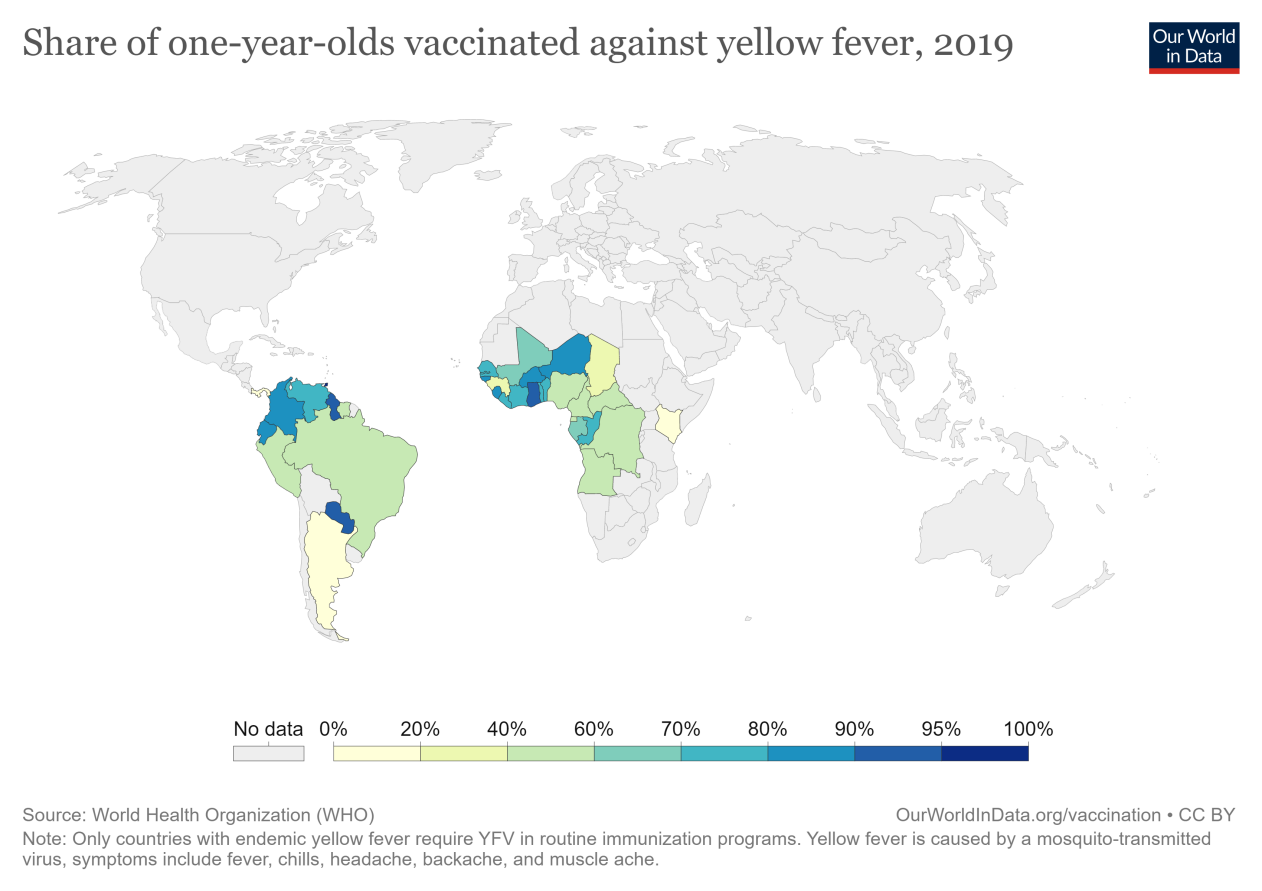
9.10黄热病疫苗
黄热病(YF)是一种由受感染的蚊子传播的病毒性疾病。在非洲和美洲有40个国家和地区面临黄热病危险,其中36个国家和地区将黄热病疫苗接种纳入其常规免疫计划。总的来说,2018年的疫苗覆盖率估计为49%。
10.定义和测量
计算覆盖率
覆盖率的计算方法是目标年龄组中接受疫苗注射的人数比例。接种疫苗的日期要么取自儿童的家庭记录,根据护理人员回忆记录,要么取自医疗机构记录。
虽然看起来很简单,但关于疫苗接种的家庭调查应答数据的几个方法问题已经被很好地记录下来。101
人们开始质疑父母回忆儿童免疫史的准确性以及电话收集数据的局限性。
即使准确估计低收入环境中的目标人群也很困难,在比较国家报告的数字和独立调查时发现了差异。102
此外,很少考虑儿童疫苗接种。在一个国家的免疫计划中,DTP3疫苗接种往往是最常用作强度标志的疫苗接种,因为需要接种三次。103
11.国家和国家以下各级的覆盖面
重点是国家覆盖率,但即使国家覆盖率很高,国家以下一级的覆盖率也可能揭示不平等,这就是为什么世卫组织和儿童基金会正在加紧努力收集高质量的国家以下一级的覆盖率数据。104
2015年,在194个世卫组织成员国中,只有158个报告了地区一级的覆盖率估计数。国家数据仅提供了免疫覆盖率的一部分情况。不同级别的覆盖数据,包括次国家或地区级别的覆盖数据,有助于了解哪里可能存在接种不足或未接种疫苗的儿童群体。
数据源
World Health Organization – Immunization surveillance, assessment and monitoring
- Data: Immunization coverage, system indicators and schedule, and disease incidence
- Geographical coverage: WHO member nations
- Time span: 1980 onwards for many countries
- Available at: Online here
UNICEF
- Data: Percent of one-year-olds immunized
- Geographical coverage: UN member nations
- Time span: 1980 onwards for many countries
- Available at: Online from UNICEF here. Also available via Gapminder here (search “vaccine” to find the data).
来源:Samantha Vanderslott, Bernadeta Dadonaite and Max Roser (2013) – “Vaccination”. Published online at OurWorldInData.org. Retrieved from: ‘https://ourworldindata.org/vaccination’ [Online Resource]
Endnotes
- This and other numbers in this entry are based on the estimates by the World Health Organisation. The coverage estimates are calculated by dividing the total number of vaccinations given by the number of children in the target population. Target population size is usually based on census population projections.This means that there may be children in the target population that for medical reasons should be exempt from vaccination. These medical reasons may include factors such as allergies to vaccine components or severe immunodeficiencies.
Notably, such cases are very rare and would have little effect on global coverage numbers. For example, a study from 2003 identified severe allergic reaction in only 0.000063% of all vaccinations, that’s 0.63 cases per million vaccinations. In addition, vaccines are always being improved with fewer ingredients that may cause allergic reactions.
Vaccination of children with immunodeficiencies generally needs to be assessed by a specialist. Especially, for vaccine that are based on a live pathogens. For example, WHO recommends vaccinating HIV-positive children with measles vaccine if child’s HIV infection is asymptomatic or not severe. Similarly, children with severe immunodeficiency syndrome (SCID), a genetic disorder that causes defects in immune system, are safely vaccinated with many vaccines before SCID is even diagnosed, but it’s recommended not to vaccinate them with live vaccines.
In fact, one of the reasons it is important to increase vaccination rates is that those children and adults who for medical reasons cannot be vaccinated would still be protected from diseases through herd immunity.
- https://www.who.int/en/news-room/fact-sheets/detail/immunization-coverage
- UNICEF (1996) and Hinman, A. R. (1998) estimate that in the absence of a vaccine the world would have seen 5 million deaths due to smallpox every year in the mid-1990s.Assuming that the estimate for the mid-1990s provides a midpoint estimate for the period since 1980 and therefore multiplying the 5 million per year estimate by the number of years between 1980 and 2018 means that since the eradication of the disease 190 million people’s lives were saved.
UNICEF (1996) – Vaccines bring 7 diseases under control. Online here.
- See Oxford’s Vaccine Knowledge Project for an explanation here: http://vk.ovg.ox.ac.uk/herd-immunity.
- Beutels P, Van Damme P, Van Casteren V, Gay NJ, De Schrijver K, Meheus A. The difficult quest for data on “vanishing“vaccine-preventable infections in Europe: the case of measles in Flanders (Belgium). Vaccine. 2002 Oct 4;20(29-
30):3551-9 here - This table is taken from Wikipedia’s entry on Herd Immunity – the original sources are listed there.
- Cholera, Dengue fever, Diphtheria, Haemophilus influenzae type b, Hepatitis A, Hepatitis B, Hepatitis E, Human papilloma-virus, Influenza, Japanese encephalitis, Malaria, Measles, Meningococcal disease, Mumps, Pneumococcal disease, Pertussis, Poliomyelitis, Rabies, Rotavirus gastroenteritis, Rubella, Tetanus, Tick-borne encephalitis, Tuberculosis, Typhoid fever, Varicella, Yellow fever, Shingles (Herpes Zoster), and Smallpox.
See https://en.wikipedia.org/wiki/Vaccine-preventable_diseases and https://www.who.int/immunization/global_vaccine_action_plan/GVAP_doc_2011_2020/en/ - See Francis EG Cox (2010) – History of the discovery of the malaria parasites and their vectors. In Parasites and Vectors. Online here.
- Roush and Murphy (2007) – Historical comparisons of morbidity and mortality for vaccine-preventable diseases in the United States. In the Journal of the American Medical Association, 298, 18, 2155–2163. here
- These data are taken from the research paper Roush and Murphy (2007) – Historical comparisons of morbidity and mortality for vaccine-preventable diseases in the United States. In the Journal of the American Medical Association, 298, 18, 2155–2163 here.
The vaccines against the diseases up till ‘Tetanus’ were vaccines licensed or recommended before 1980. The vaccines against the last 5 diseases were only licensed or recommended between 1980 and 2005. - See also ‘Graphical proof that vaccines work (with sources)’ in Medium online here.To account for such long-term changes, Roush and Murphy (2007) report data from the period shortly before the introduction of the respective vaccine. here
- In our graphics and visualizations we rely on the Institute for Health Metrics (IHME) ‘Global Burden of Disease Study 2016’ estimates of child death rates from individual VPDs (compared with other causes), TB death rates across countries, and death rates from individual VPDs; this dataset extends back to 1990 and therefore provides a longer-term perspective on these changes over time. However, lack of estimates from the IHME on the role of vaccination in the prevention of deaths means we rely on WHO data for the number of deaths prevented each year through vaccination and the total amount of deaths VPDs are responsible for.The rates reported by the WHO and IHME are in a similar range but do differ slightly. WHO data on individual disease death rates can be found here: http://www.who.int/gho/mortality_burden_disease/en/
- Note that, as discussed later in this post, the role of vaccines in prevention varies between these causes of death. Measles, for example, has the capacity to be eliminated through vaccination. Diarrheal deaths, in contrast, cannot be eliminated through vaccination alone; hygiene, water services, and nutrition must also be prioritised.
- Some countries only give measles vaccines combined with rubella (MR) or with varicella in addition (MMRV).
- Highlighted are 10 countries where approximately 60% of these infants live in: Angola, Brazil, the Democratic Republic of the Congo, Ethiopia, India, Indonesia, Iraq, Nigeria, Pakistan, and South Africa.
- Zwerling A, Behr MA, Verma A, Brewer TF, Menzies D, Pai M. The BCG World Atlas: A Database of Global BCG Vaccination Policies and Practices. PLoS Medicine. 2011;8(3):e1001012. doi:10.1371/journal.pmed.1001012. Available here.
- For a detailed commentary on why we do not yet have an effective TB vaccine see: Davenne T, McShane H. Why don’t we have an effective tuberculosis vaccine yet? Expert Review of Vaccines. 2016;15(8):1009-1013. doi:10.1586/14760584.2016.1170599. Available here.
- An affordable MenACWYX vaccine is being developed to cover all the types of meningococcal disease (with the exception of meningitis B, which is available through a separate vaccine) and will also have the ability to be transported at higher temperatures. It is currently in phase 1 clinical trial, with the hope that it will be available for use in 2020–2022.
- See Meningococcal disease in the Middle East and Africa: Findings and updates from the Global Meningococcal Initiative, Borrow, Ray et al. Journal of Infection, Volume 75 , Issue 1 , 1 – 11. Available here.
- Susan T Goldstein, Fangjun Zhou, Stephen C Hadler, Beth P Bell, Eric E Mast, Harold S Margolis; A mathematical model to estimate global hepatitis B disease burden and vaccination impact, International Journal of Epidemiology, Volume 34, Issue 6, 1 December 2005, Pages 1329–1339, https://doi.org/10.1093/ije/dyi206. Available here.
- Smallpox is the only disease that affects humans which has been eradicated through vaccination. Rinderpest, a disease that affected cattle, has also been eradicated. Polio is getting close to being eradicated.
- This survey result is in line with the finding of the Gapminder Ignorance Project, which studied Americans’ perception of global vaccination efforts. Just as in the Ipsos Mori survey, the answers that most Americans gave were far off from the truth.
More information on the Gapminder ‘Ignorance Test’ can be found here. The results for the US are here on Gapminder’s site.
- The survey results are from Chris Jackson (2017) – Global Perceptions of Development Progress: ‘Perils of Perceptions’ Research’, published by Ipsos MORI, 18 September 2017. Online here.
- Terminology: vaccination and immunization
There is a technical difference between vaccination and immunization, as the National Health Service (NHS) explains: “Vaccination means having a vaccine – that is actually getting the injection, or nasal spray or oral vaccine. Immunization means both receiving a vaccine and then becoming immune to a disease”. The distinction is made because in a very small number of those who are vaccinated the vaccination will not ‘take’ and therefore that vaccinated person will not be immunized (i.e. will not be immune to the disease). However, as this refers to a very small number of people both terms are often used interchangeably across the academic literature and in media reporting and we follow this convention in this entry.
- For the WHO recommendations see http://www.who.int/ith/vaccines/en/The Bacille Calmette-Guerin (BCG) vaccine for tuberculosis (TB) is recommended in countries where TB is common. BCG policies and practices have varied considerably across time and countries. The BCG World Atlas is an online resource that tracks these changes comprehensively.
- It provides data on topics such as trust in science and scientists; trust in sources of information about health; public understanding of the word ‘science’; the intersection between religious teachings and science; and attitudes to vaccines. In this post, we focus on how attitudes to vaccination vary across the world.
- This is a stark result for Venezuela in particular (although perhaps unsurprising) since the availability and coverage of child vaccination has fallen significantly over the last few years.
- Navin M. Largent, improving non-medical exemption vaccine policies: three case studies. Public Health Ethics. 2017; 10: 225–234. Available here
- See: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1449224/
- Stern, M., Alexandra. (2010). Better Off in School: School Medical Inspection as a Public Health Strategy During the 1918-1919 Influenza Pandemic in the United States
- Amin, A.N.E., Parra, M.T., Kim-Farley, R. et al. (2012) – Ethical Issues Concerning Vaccination Requirements. In Public Health Reviews (2012) 34: 14. https://doi.org/10.1007/BF03391666. Online here: https://link.springer.com/article/10.1007/BF03391666
- See: http://www.who.int/csr/ihr/icvp/en/index.html
- Salmon, Daniel A et al., Compulsory vaccination and conscientious or philosophical exemptions: past, present, and future, The Lancet, Volume 367, Issue 9508, 436 – 442
- The data source for vaccination coverage: School Vaccination Assessment Report, 2016-17 school year.
Estimated vaccination coverage with 5 doses of Childhood Diphtheria toxoid, Tetanus toxoid, acellular Pertussis (DTaP) vaccination for kindergartners (typical age range is 4–6 years).The data source for exemptions is: Immunization Action Coalition, “Exemptions Permitted for State Immunization Requirements,” 2017; LexisNexis; StateNet 2017Regarding the school vaccination coverage and exemption methods the source notes: “Each school year, school nurses, other school personnel, or health department personnel check the vaccination and exemption status of kindergartners enrolled in public and private schools as required by state law or regulation. State and local immunization programs measure vaccination coverage among children entering kindergarten annually. This may be done for every student or for a sample of students.
State and local areas set the vaccination requirements. Immunization information systems (IISs) may be used as one source of data for school vaccination assessment. The school-level data are reported to the health department. The aggregate data are reported to CDC for public and private schools. Data for home-schooled students are not routinely reported to CDC.”
The types of permitted exemptions vary by state. For specific details refer to School Vaccination Requirements and Exemptions.
- See the WHO here.
- See here.
- According to MacKenzie, D. (2011) – Vaccines enjoy a healthy return. New Scientist. Available online.
- In 2014 their vaccine business was acquired by GlaxoSmithKline, as reported here.
- There are exceptions however. A vaccine for tetanus and diphtheria (td) for example, has a large number of suppliers (13, and 7 for the paediatric formulation).
- Review of vaccine price data. Submitted by WHO European Region Member States through the WHO/UNICEF. Joint Reporting Form for 2013. Online here.
- The Economist. (2010). A smarter jab. Available online
- The Economist. (2010). A smarter jab. Available online
- See WHO guidance for more information at: https://www.who.int/vaccine_safety/initiative/tools/DTP_vaccine_rates_information_sheet.pdf
- Jaffe, A. B., Lerner, J., Stern, S., & National Bureau of Economic Research. Innovation Policy and the Economy Group. (2006). Innovation policy and the economy. MIT Press. here
- The source of the data is the International drug price indicator guide
- Lanziera, T., Haber, P., Icenogle, J. P., & Patel, M. (n.d.). Rubella. In Epidemiology and Prevention of Vaccine-Preventable Diseases. Communication and Education Branch, National Center for Immunization and Respiratory Diseases, Centers for Disease Control and Prevention. https://www.cdc.gov/vaccines/pubs/pinkbook/rubella.html
- World Health Organization. (2021). New and underutilized vaccines introduction. https://immunizationdata.who.int/pages/indicators-by-category/new_and_under_utilized_vaccines_introduction.html
- Bonanni et al. 2009; Bonanni P., Breuer J., Gershon A., Gershon M., Hryniewicz W., Papaevangelou V., et al. (2009) – Varicella vaccination in Europe – taking the practical approach. BMC Med 7: 26 here.
- Gostin, L. O., Salmon, D. A. and Larson, H. J. (2021) ‘Mandating COVID-19 Vaccines’, JAMA. American Medical Association, 325(6), p. 532. doi: 10.1001/jama.2020.26553.
- Vanderslott, S., & Marks, T. (2021). Charting mandatory vaccination policies worldwide. Vaccine.
- Attwell, K. and C. Navin, M. (2019) ‘Childhood Vaccination Mandates: Scope, Sanctions, Severity, Selectivity, and Salience’, The Milbank Quarterly, 97(4), pp. 978–1014. doi: 10.1111/1468-0009.12417.
- Stuart Blume (2017) Immunization: How Vaccines became Controversial – Stuart Blume – Google Books. Reaktion Books.
- Attwell, K., Drislane, S. and Leask, J. (2019) ‘Mandatory vaccination and no fault vaccine injury compensation schemes: An identification of country-level policies’, Vaccine. Elsevier Ltd, 37(21), pp. 2843–2848. doi: 10.1016/j.vaccine.2019.03.065.
- Rezza, G. (2019) ‘Mandatory vaccination for infants and children: the Italian experience’, Pathogens and Global Health. Taylor and Francis Ltd., pp. 291–296. doi: 10.1080/20477724.2019.1705021.
- Pejin LS. Tightening measures for compliance with vaccination in Serbia ESPN Flash Report. European Commission; 2016.
- UNICEF. Guyana Situation Analysis of Children and Women; 2016. Available at: https://www.unicef.org/sitan/ [accessed: 10 April 2020].
- Onyemelukwe, C. (2016) ‘Can legislation mandating vaccination solve the challenges of routine childhood immunisation in Nigeria?’, Oxford University Commonwealth Law Journal. Taylor and Francis Ltd., 16(1), pp. 100–124. doi: 10.1080/14729342.2016.1244450.
- See the WHO here: http://www.who.int/mediacentre/factsheets/fs378/en/
- Holt, Ed., Ukraine at risk of polio outbreak, The Lancet , Volume 381 , Issue 9885 , 2244 here
- Figures are updated by the WHO here: http://www.who.int/news-room/fact-sheets/detail/measles
- See the WHO here: http://www.who.int/mediacentre/factsheets/fs286/en/
- In 2014 there were 135.2 million one-year olds. Of these 84.52% received the vaccine against measles.
This means that 135.2 *0.8452 = 114.27 million children were vaccinated. - Gaston De Serres, Jill Sciberras, Monika Naus, Nicole Boulianne, Bernard Duval, and Louis Rochette (1999) – Protection after Two Doses of Measles Vaccine Is Independent of Interval between Doses. In The Journal of Infectious Diseases, Volume 180, Issue 1, 1 July 1999, Pages 187–190, https://doi.org/10.1086/314847 Online here: https://academic.oup.com/jid/article/180/1/187/990623.
- For guidelines on recommendations for the second dose of measles vaccine see here https://www.who.int/immunization/sage/meetings/2016/october/Session6-MCV2-Introduction-criteria.pdf
- World Health Organization. (2019). Rotavirus. [online] Available at: https://www.who.int/immunization/diseases/rotavirus/en/ [Accessed 14 Aug. 2019].
- Ruiz-Palacios, G. M., Pérez-Schael, I., Velázquez, F. R., Abate, H., Breuer, T., Clemens, S. C., … & Cervantes, Y. (2006). Safety and efficacy of an attenuated vaccine against severe rotavirus gastroenteritis. New England Journal of Medicine, 354(1), 11-22.
- Vesikari, T., Matson, D. O., Dennehy, P., Van Damme, P., Santosham, M., Rodriguez, Z., … & Shinefield, H. R. (2006). Safety and efficacy of a pentavalent human–bovine (WC3) reassortant rotavirus vaccine. New England Journal of Medicine, 354(1), 23-33.
- Troeger, C., Khalil, I. A., Rao, P. C., Cao, S., Blacker, B. F., Ahmed, T., … & Kang, G. (2018). Rotavirus vaccination and the global burden of rotavirus diarrhea among children younger than 5 years. JAMA Pediatrics, 172(10), 958-965.
- Aliabadi, Negar, et al. “Global impact of rotavirus vaccine introduction on rotavirus hospitalisations among children under 5 years of age, 2008–16: findings from the Global Rotavirus Surveillance Network.” The Lancet Global Health7.7 (2019): e893-e903.
- The cost of rotavirus vaccines varies by country. For example, countries with a gross national income per capita of less than US$1,000 receive subsidies from the Global Alliance for Vaccines and Immunisation, and there the cost per dose is set between US$2.10 – 3.20. With additional co-financing options can reduce the costs down to US$0.13. In high-income countries, such as the US, the cost per dose is between US$70 and 95
Countries are more likely to introduce the vaccine if the political environment is favourably disposed towards them. For example, if a country has set a high priority on achieving the Millennium Development Goal targets or the introduction of vaccines is seen as a positive news story, especially during election years.
Burchett, H. E. D., Mounier-Jack, S., Griffiths, U. K., Biellik, R., Ongolo-Zogo, P., Chavez, E., … & Molla, M. (2012). New vaccine adoption: qualitative study of national decision-making processes in seven low-and middle-income countries. Health policy and planning, 27(suppl_2), ii5-ii16.
- World Health Organization (2019). Immunization coverage. [online] Available at: https://www.who.int/news-room/fact-sheets/detail/immunization-coverage [Accessed 14 Aug. 2019].
- Clark, Andrew, et al. “Efficacy of live oral rotavirus vaccines by duration of follow-up: a meta-regression of randomised controlled trials.” The Lancet Infectious Diseases (2019).
- The Clark et al. (2019) study defined low child mortality rate as less than 1.3% of newborns; medium mortality rate as between 1.35% and 2.81%; and high mortality rate as more than 2.81%
- Lamberti, L. M., Ashraf, S., Walker, C. L. F., & Black, R. E. (2016). A systematic review of the effect of rotavirus vaccination on diarrhea outcomes among children younger than 5 years. The Pediatric Infectious Disease Journal, 35(9), 992-998.
- Patel, M., Shane, A. L., Parashar, U. D., Jiang, B., Gentsch, J. R., & Glass, R. I. (2009). Oral rotavirus vaccines: how well will they work where they are needed most?. The Journal of Infectious Diseases, 200, S39-S48.
- Parker, E. P., Ramani, S., Lopman, B. A., Church, J. A., Iturriza-Gomara, M., Prendergast, A. J., & Grassly, N. C. (2018). Causes of impaired oral vaccine efficacy in developing countries. Future microbiology, 13(1), 97-118.
- Troeger, C., Blacker, B., Khalil, I. A., Rao, P. C., Cao, J., Zimsen, S. R., … & Adetifa, I. M. O. (2018). Estimates of the global, regional, and national morbidity, mortality, and aetiologies of lower respiratory infections in 195 countries, 1990–2016: a systematic analysis for the Global Burden of Disease Study 2016. The Lancet Infectious Diseases, 18(11), 1191-1210.
- Who.int. (2019) – Immunization coverage. [online] [Accessed 10 Sep. 2019]. http://view-hub.org/viz/ (Go to PCV —> PCV – Vaccine Access —> Children without Access)
- Hanada, S., Pirzadeh, M., Carver, K. Y., & Deng, J. C. (2018). Respiratory Viral Infection-Induced Microbiome Alterations and Secondary Bacterial Pneumonia. Frontiers in immunology, 9, 2640.
- Song, J. Y., Nahm, M. H., & Moseley, M. A. (2013). Clinical implications of pneumococcal serotypes: invasive disease potential, clinical presentations, and antibiotic resistance. Journal of Korean medical science, 28(1), 4-15.
- The number of serotypes included in the vaccine is generally indicated in its name, e.g. PCV13 is pneumococcal conjugate vaccine effective against 13 bacterial serotypes. Vaccines including progressively more serotypes have been introduced over the years, PCV7 was introduced in 2000 and today the most commonly used PCV13 was introduced in 2010.Hausdorff, W. P., Feikin, D. R., & Klugman, K. P. (2005). Epidemiological differences among pneumococcal serotypes. The Lancet infectious diseases, 5(2), 83-93.
- The current non-conjugate vaccine, PPSV23, is generally only given to adults or as a single dose following two immunisations with PCV13 in children older than 2.Golos, M., Eliakim‐Raz, N., Stern, A., Leibovici, L., & Paul, M. (2016). Conjugated pneumococcal vaccine versus polysaccharide pneumococcal vaccine for prevention of pneumonia and invasive pneumococcal disease in immunocompetent and immunocompromised adults and children. Cochrane Database of Systematic Reviews, (8).
- The 27% refers to X-ray-defined cases of pneumonia. For clinically defined pneumonia, a less accurate diagnosis than X-ray-defined cases, the number is 6%. Both of these indicators refer to cases of pneumonia caused by any pathogen not only pneumococcus. Lucero, M. G., Dulalia, V. E., Nillos, L. T., Williams, G., Parreño, R. A. N., Nohynek, H., … & Makela, H. (2009). Pneumococcal conjugate vaccines for preventing vaccine‐type invasive pneumococcal disease and X‐ray defined pneumonia in children less than two years of age. Cochrane Database of Systematic Reviews, (4).
- Wahl, B., O’Brien, K. L., Greenbaum, A., Majumder, A., Liu, L., Chu, Y., … & Rudan, I. (2018). Burden of Streptococcus pneumoniae and Haemophilus influenzae type b disease in children in the era of conjugate vaccines: global, regional, and national estimates for 2000–15. The Lancet Global Health, 6(7), e744-e757.
- Chen, C., Liceras, F. C., Flasche, S., Sidharta, S., Yoong, J., Sundaram, N., & Jit, M. (2019). Effect and cost-effectiveness of pneumococcal conjugate vaccination: a global modelling analysis. The Lancet Global Health, 7(1), e58-e67.
- GAVI (Global Alliance for Vaccines and Immunisation) is a non-profit organisation that provides access to vaccination programs for low-income countries by providing financial support and individual expertise.
- O’Brien, K. L. (2018). When less is more: how many doses of PCV are enough?. The Lancet Infectious Diseases, 18(2), 127-128.
- For example Kenya has recently entered a transition phase during which it will pay a larger and larger portion of the PCV vaccine cost. By 2027 Kenya will have to pay the full $9 price for a three-dose course child vaccination. The 2016 per capita healthcare expenditure in Kenya was around $66 (5% of the GDP), clearly $9 per child is not a trivial cost.Simonsen, L., van Wijhe, M., & Taylor, R. (2019). Are expensive vaccines the best investment in low-income and middle-income countries?. The Lancet Global Health, 7(5), e548-e549.
Ojal, J., Griffiths, U., Hammitt, L. L., Adetifa, I., Akech, D., Tabu, C., … & Flasche, S. (2019). Sustaining pneumococcal vaccination after transitioning from Gavi support: a modelling and cost-effectiveness study in Kenya. The Lancet Global Health, 7(5), e644-e654.
- The return of investment was estimated for a projected coverage for individual countries for the decade between 2011 and 2020. It means that the economic benefits (as measured by the costs of vaccination program subtracted from the reduced costs of treatment and productivity loss) of using the vaccine are 3 times higher than no vaccine use.
To reduce costs, some countries may also consider switching to a two rather than three dose immunization schedule, but more research on the effectiveness of this schedule in different countries is needed. See O’Brien et al. (2018) reference.Nakamura, M. M., Tasslimi, A., Lieu, T. A., Levine, O., Knoll, M. D., Russell, L. B., & Sinha, A. (2011). Cost effectiveness of child pneumococcal conjugate vaccination in middle-income countries. International health, 3(4), 270-281.Ozawa, S., Clark, S., Portnoy, A., Grewal, S., Brenzel, L., & Walker, D. G. (2016). Return on investment from childhood immunization in low-and middle-income countries, 2011–20. Health Affairs, 35(2), 199-207.
Center, I. V. A. (2017). The evidence base for pneumococcal conjugate vaccines (PCVs): data for decision-making around PCV use in childhood. Baltimore (MD): Johns Hopkins University.
Goldblatt, D., Southern, J., Andrews, N. J., Burbidge, P., Partington, J., Roalfe, L., … & Snape, M. D. (2018). Pneumococcal conjugate vaccine 13 delivered as one primary and one booster dose (1+ 1) compared with two primary doses and a booster (2+ 1) in UK infants: a multicentre, parallel group randomised controlled trial. The Lancet Infectious Diseases, 18(2), 171-179.
O’Brien, K. L. (2018). When less is more: how many doses of PCV are enough?. The Lancet Infectious Diseases, 18(2), 127-128.
- Adegbola, R. A., DeAntonio, R., Hill, P. C., Roca, A., Usuf, E., Hoet, B., & Greenwood, B. M. (2014). Carriage of Streptococcus pneumoniae and other respiratory bacterial pathogens in low and lower-middle income countries: a systematic review and meta-analysis. PloS one, 9(8), e103293.
- Megiddo, I., Klein, E., & Laxminarayan, R. (2018). Potential impact of introducing the pneumococcal conjugate vaccine into national immunisation programmes: an economic-epidemiological analysis using data from India. BMJ global health, 3(3), e000636.
- Johnson, H. L., Deloria-Knoll, M., Levine, O. S., Stoszek, S. K., Hance, L. F., Reithinger, R., … & O’Brien, K. L. (2010). Systematic evaluation of serotypes causing invasive pneumococcal disease among children under five: the pneumococcal global serotype project.PLoS medicine, 7(10), e1000348.
- World Health Organization. (2010). Changing epidemiology of pneumococcal serotypes after introduction of conjugate vaccine: July 2010 report. Weekly Epidemiological Record [Relevé épidémiologique hebdomadaire], 85(43), 434-436.
- Pichichero, M. E. (2017). Pneumococcal whole-cell and protein-based vaccines: changing the paradigm. Expert review of vaccines, 16(12), 1181-1190.
- Ginsburg, A. S., Nahm, M. H., Khambaty, F. M., & Alderson, M. R. (2012). Issues and challenges in the development of pneumococcal protein vaccines. Expert review of vaccines, 11(3), 279-285
- Kendig, E. L., Wilmott, R. W., & Chernick, V. (2012). Kendig and Chernick’s disorders of the respiratory tract in children. 9th ed. Elsevier Health Sciences.
- Rodrigues, L. C., Mangtani, P., & Abubakar, I. (2011). How does the level of BCG vaccine protection against tuberculosis fall over time?. Bmj, 343, d5974.
- Rodrigues, L. C., Diwan, V. K., & Wheeler, J. G. (1993). Protective effect of BCG against tuberculous meningitis and miliary tuberculosis: a meta-analysis.International journal of epidemiology, 22(6), 1154-1158.
- Sterne, J. A. C., Rodrigues, L. C., & Guedes, I. N. (1998). Does the efficacy of BCG decline with time since vaccination?.The international journal of tuberculosis and lung disease, 2(3), 200-207.
- Aronson, N. E., Santosham, M., Comstock, G. W., Howard, R. S., Moulton, L. H., Rhoades, E. R., & Harrison, L. H. (2004). Long-term efficacy of BCG vaccine in American Indians and Alaska Natives: a 60-year follow-up study.Jama, 291(17), 2086-2091.
- https://www.who.int/biologicals/areas/vaccines/bcg/en/
- https://www.who.int/news-room/fact-sheets/detail/immunization-coverage
- Daniel A. Salmon, Philip J. Smith, Ann Marie Navar, William K. Y. Pan, Saad B. Omer, James A. Singleton, Neal A. Halsey; Measuring Immunization Coverage among Preschool Children: Past, Present, and Future Opportunities, Epidemiologic Reviews, Volume 28, Issue 1, 1 August 2006, Pages 27–40, https://doi.org/10.1093/epirev/mxj001
- ”Global childhood immunization coverage growing at only half the officially reported rate, IHME study” online here: http://www.healthdata.org/news-release/global-childhood-immunization-coverage-growing-only-half-officially-reported-rate-ihme
- Other vaccines measured by the WHO and UNICEF are HepB3, Hib3, MCV and PAB.
- See: http://www.who.int/immunization/newsroom/press/immunization_coverage_july_2016/en/
Cite this work
Our articles and data visualizations rely on work from many different people and organizations. When citing this topic page, please also cite the underlying data sources. This topic page can be cited as:
Samantha Vanderslott, Saloni Dattani, Fiona Spooner and Max Roser (2013) - "Vaccination". Published online at OurWorldInData.org. Retrieved from: 'https://ourworldindata.org/vaccination' [Online Resource]
Hits: 105

Thank you for sharing your info. I really appreciate your efforts and I will be waiting for your further post thanks once again.
Woah! I’m really digging the template/theme of
this blog. It’s simple, yet effective. A lot of times it’s
difficult to get that “perfect balance” between usability and visual appeal.
I must say you have done a amazing job with this.
In addition, the blog loads extremely fast for me on Chrome.
Superb Blog!
Thanks
🚀 Wow, blog ini seperti roket meluncurkan ke galaksi dari kegembiraan! 💫 Konten yang menegangkan di sini adalah perjalanan rollercoaster yang mendebarkan bagi pikiran, memicu kagum setiap saat. 💫 Baik itu teknologi, blog ini adalah harta karun wawasan yang menarik! 🌟 🚀 ke dalam perjalanan kosmik ini dari imajinasi dan biarkan pemikiran Anda terbang! 🌈 Jangan hanya menikmati, alami sensasi ini! #MelampauiBiasa Pikiran Anda akan bersyukur untuk perjalanan mendebarkan ini melalui alam keajaiban yang menakjubkan! ✨